
科目: 来源: 题型:
【题目】某实验小组要测定混有氯化钠的纯碱样品中Na2CO3的质量分数。取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至恰好完全反应,共消耗稀盐酸72.4g,测得反应后溶液的质量为80g。请帮助实验小组完成以下计算:
(1)生成二氧化碳的质量为_____克;
(2)该纯碱样品中Na2CO3的质量分数;_____
(3)反应后所得溶液中溶质的质量分数是多少?_____
查看答案和解析>>
科目: 来源: 题型:
【题目】食盐是一种重要的化工原料,回答下列问题
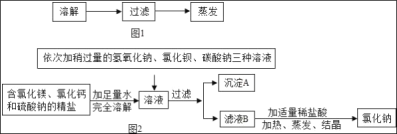
(1)粗盐中含有的难溶性杂质,甲同学在实验室里通过如图1所示的实验步骤将其去除.
①过滤所用的玻璃仪器有:烧杯、漏斗和_____.
②在加热蒸发过程中,当蒸发皿中出现_____固体时,停止加热,利用蒸发皿的余热将滤液蒸干.
③在本实验中,先称取5g粗盐,再量取10ml水,加粗盐至不再溶解为止时称得剩余粗盐质量为1g,通过如图1实验步骤最终得到3.5g精盐,则精盐的产率是_____.
(2)利用上述实验得到的精盐中还含有少量氯化镁、氯化钙、硫酸钠等杂质,乙同学用天平称量一定量的含氯化镁、氯化钙、硫酸钠的精盐,并设计了如图2所示过程进行除杂提纯,实验后得到较纯净的氯化钠固体(此题中微溶物视为可溶物).
①沉淀A中共含有_____种物质(填字母).
A 2 B 3 C 4 D 5
②滤液B中加适量稀盐酸的作用是除去_____.
(3)氯化钠固体与浓硫酸在加热条件下反应生成硫酸钠和氯化氢气体.写出此反应的化学方程式_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线。请回答下列问题。
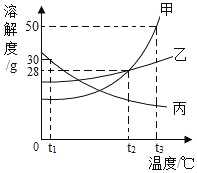
(1)若将丙的饱和溶液从t3℃降温到t2℃时,一定会发生改变的是_____(填序号);
A 溶解度 B 溶质的质量 C 溶质的质量分数
(2)分别将甲、乙、丙三种物质的饱和溶液各100g从t3℃降到t2℃,降温后甲、乙、丙三种溶液的溶剂质量由大到小的顺序是_____。
(3)t3℃时甲的饱和溶液的溶质质量分数是_____(计算结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现代生活中,人们越来越注意微量元素的摄入.血红蛋白中的铁是人体内氧的输送者,缺铁易患贫血.
(1)一种添加了营养剂的“铁强化”酱油已经面市.根据卫生部铁强化剂添加标准,每100mL酱油中铁营养剂添加量是200mg,该营养元素质量分数为12.5%.根据实验测得,酱油中铁只有10%能被人体吸收,以某人一天使用16mL该酱油计算,他一天从酱油中吸收的铁元素是多少毫克?
(2)某贫血患者除正常饮食吸收铁元素外,还需服用含铁元素的某种药物.若治疗一个疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁晶体(FeSO47H2O)多少克?
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某同学设计的实验室制取二氧化碳的装置图。
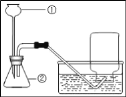
(1)指出图中仪器名称①_____;②_____。
(2)右图中有两处明显错误,请指出并改正①_____,②_____。改正错误后在发生装置内发生的化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组同学用右图所示装置(夹持仪器已略去)做了2个兴趣实验。每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出。请完成下列空白。
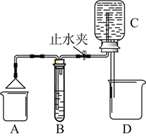
(1)在A处放置燃烧的蜡烛,B中无色溶液变浑浊,写出B中发生反应的化学方程式:___________________________。 蜡烛燃烧生成的气体被吸入B中的原因是________________________。
(2)在A处放置燃烧的蜡烛,若B中盛有紫色石蕊溶液,则变红色,写出B中发生反应的化学方程式:___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Cu可以形成化合价为+2和+1的化合物,其中+l价化合物称为亚铜化合物。
(1)高温时,氧化铜可被木炭还原为铜,反应的化学方程式是_____,该反应属于基本反应类型中的_____反应。
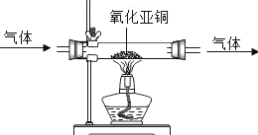
(2)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式是_____;利用这一性质可检验氮气中是否含有氧气(装置如图所示),判断氮气中含有氧气的现象是_____。
(3)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3还是Cu2O或是二者混合物。探究过程如下:
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO;
②Fe3+遇到KSCN试剂变红。
[提出假设]假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;
假设3:_____。
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
①若假设1成立,则实验现象是_____;
②若假设2成立,写出反应的化学方程式:_____。
[探究延伸]若经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物。实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为_____%。
查看答案和解析>>
科目: 来源: 题型:
【题目】小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否为虚假广告.
国内首创
优质硝酸铵
NH4NO3
含氮量全球最高(38%)
国内首创
优质硝酸铵
NH4NO3
含氮量全球最高(38%)
(1)请你写出小强的计算过程和判断依据.计算过程:_____.
结论:该广告_____(“是”或“不是”)虚假广告.
(2)小强认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】自贡市建设乡盛产枇杷,有“枇杷之乡”之美誉。如图是这种枇杷的部分营养成分,请据图回答:
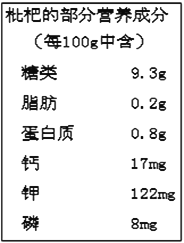
(1)图中的钙.钾.磷是指_____
A分子 B原子 C元素 D单质
(2)图中出现了六大营养素中的_____类,能提供能量的营养素有_____种。
(3)枇杷适宜生长在pH为6左右的土壤中。若某土壤的pH为3,经改良后可种植枇杷。下列物质,既可用来改良土壤酸性,又能给土壤施肥的物质是_____。
A生石灰 B熟石灰 C过磷酸钙 D草木灰(主要成分碳酸钾)
(4)小组在杳阅资料中,还发现了—种新型的食品干燥剂:泡沫铁粉(铁粉包裹在泡沫塑料中)。当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3·nH2O),并有发热现象,说明化学反应除了生成新物质外,还伴随着_____变化。与生石灰比较,泡沫铁粉除了做干燥剂外,还具有的优点是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com