
科目: 来源: 题型:
【题目】如图1A是碳元素在元素周期表中的相关信息,图1B是该元素的原子结构示意图。
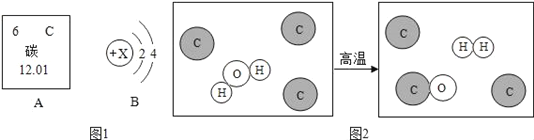
(1)碳元素的相对原子质量为_____.
(2)B图中X=_____.
(3)图2是有关碳单质的化学变化的微观示意图,根据以上示意图,写出该反应的化学方程式_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】(12分)氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图10所示(固定装置省略)。
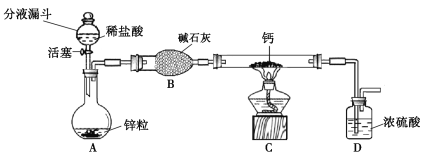
图10
回答下列问题:
(1)装置A中制取氢气的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中制取氢化钙的化学方程式为 。
(4)若不改变温度,整套装置气密性的检查方法是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图11(固定装置省略)所示连接仪器。
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化钙的纯度为 。(结果精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)某固体混合物,已知该混合物中可能含有Na2CO3、NH4Cl、NH4NO3、CuSO4、NaOH五种物质中的两种或多种。按照下图进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
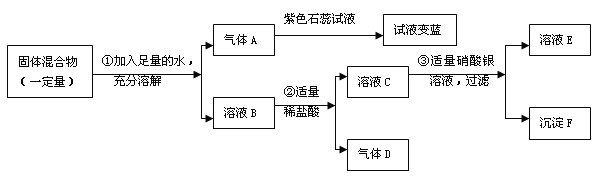
试根据实验过程和发生的现象填写以下空白:
(1)气体A的化学式为_____________,该气体具有_______________气味;
(2)溶液B中的金属阳离子为 ;
(3)过程③发生的有关反应的化学方程式为 ;
(4)根据上述实验现象推测,该混合物中一定没有的物质是 (写化学式) ,判断的理由为____________________________________________________________;
(5)仅根据上述实验现象,还不能确定混合物中含有的物质是 (写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】控制变量法是实验探究的重要方法.利用如图所示的实验不能实现的探究目的是( )
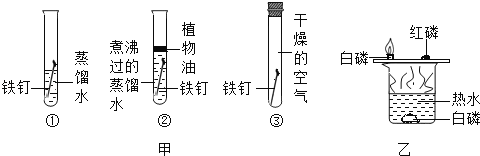
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙可探究可燃物的燃烧是否需要达到一定温度
D.乙可探究可燃物的燃烧是否需要与氧气接触
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
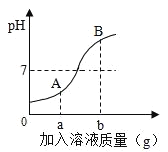
A. 该反应是稀HCl滴入NaOH溶液中
B. A点溶液能使无色酚酞变红
C. A点溶液的溶质只有NaCl
D. 检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对分子、原子、离子的认识,不正确的是( )
A. 水、氯化钠、铜都是由分子构成的
B. 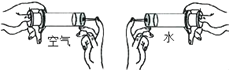 如图,装空气的注射器容易被压缩是因为气体分子间间隔较大
如图,装空气的注射器容易被压缩是因为气体分子间间隔较大
C. 不同的碱化学性质有所差异,是因为解离出的阳离子不同
D. 化学变化中分子可分,原子不可分
查看答案和解析>>
科目: 来源: 题型:
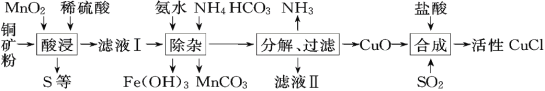
【题目】CuCl常用作有机合成催化剂,实验室以初级铜矿粉(主要成分为硫化亚铜(Cu2S)及少量Fe2O3等)为原料制备活性CuCl。实验过程如下:
(资料)
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②Cu(OH)2可溶于氨水形成深蓝色硫酸四氨合铜[Cu(NH3)4SO4]溶液;
③[Cu(NH3)4SO4]常温稳定,在热水中会分解生成NH3;
④CuCl在空气中易被氧化。
(1)酸浸时,为了提高浸取率可采取的措施有______(任写一点); “酸浸”过程中发生的化学反应有:①Cu2S+2MnO2+4H2SO4=2______+2MnSO4+S+4H2O、②______。从后续生产的角度分析,酸浸时稀硫酸不宜过量太多的原因是______。
(2)除杂过程中加足量氨水的作用①使Fe3+沉淀;②中和过量的硫酸;③______。
(3)①“分解”实验条件及现象如下表所示。
温度/℃ | 压强/kPa | 时间/min | 残液颜色 | |
A | 110 | 101.3 | 60 | 浅蓝色 |
B | 100 | 74.6 | 40 | 很浅 |
C | 90 | 60.0 | 30 | 无色透明 |
则“分解”实验条件应选______(填字母)。
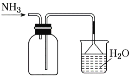
②“分解”生成的NH3可以回收利用。在实验室用如图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是______。
(4)请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、______。
A 真空干燥 B 在氩气中干燥 C 在空气中烘干
(5)若要制得99.5g CuCl,理论上至少需要硫化亚铜含量为60%的铜矿粉多少克______?(请写出计算过程,结果保留到小数点后一位)
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。某研究小组采用如下实验流程用Na2CO3溶液吸收SO2制备Na2SO3。
反应Ⅰ中随着SO2的增加,依次发生如下化学反应:
SO2+H2O+2Na2CO3=Na2SO3+2NaHCO3;
SO2+2NaHCO3=Na2SO3+2CO2↑+H2O;
SO2+H2O+Na2SO3=2NaHSO3

(1)H2SO3的名称为亚硫酸,则Na2SO3的名称为______。
(2)分析反应1提供的资料,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如图1所示。则线1表示______(填化学式,下同)的质量分数的变化情况,线2表示______的质量分数的变化情况。
(3)实验时,“反应Ⅱ”中加入NaOH溶液的目的是将反应I中生成的NaHSO3转化为Na2SO3则该化学反应方程式为______。

(4)常用蒸发结晶的方法分离混合溶液得到Na2SO3,由此可知,Na2SO3的溶解度曲线是与图2中的______(填A或B)物质的溶解度曲线相似。
(5)过滤操作得到的滤液中一定含有的溶质的化学式为______。
(6)实验后,将Na2SO3样品放置在烧杯中,一段时间后,检测发现样品中出现Na2SO4杂质,且放置时间越长产生的Na2SO4越多,则Na2SO3样品变质为Na2SO4的化学反应方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列实验问题:
(1)现提供如图装置
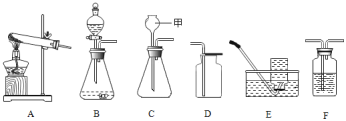
①上图C装置中,甲仪器的名称是______。
②实验室用氯酸钾制取氧气,发生装置是______(填序号),反应的化学方程式为______,若用E装置收集氧气,当有______时,开始收集气体。
③实验室可以按照“B→F→F→真空气囊”的装置顺序制取纯净的CO2气体,B装置中发生反应的化学方程式为______,第一个F装置盛放试剂的作用是______,第二个F装置盛放的试剂为______,检验CO2气体的原理______(用化学方程式表示)。B装置与C装置相比,其优点是______。
(2)实验室用氯化钠固体配制50g15%的氯化钠溶液的步骤有:计算、称取氯化钠、量取水、溶解、转移。
①在溶解过程中,玻璃棒的作用是______。
②下列操作中,可能导致配制氯化钠溶液的溶质质量分数偏大的是______(填序号)。
a称取时,将氯化钠置于托盘天平的右盘 b量取水时俯视读数
c用已有少量水的烧杯溶解氯化钠 d转移时,有少量溶液溅出
(3)化学实验的设计除考虑实验目的外,还要考虑实验安全,减少对环境的污染等因素,据此应将下列实验中的A与______(填“B”、“C”或“D”)归为一类。
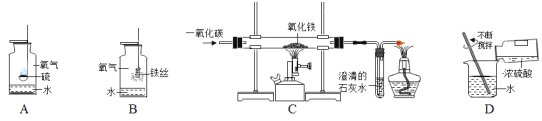
A 硫在氧气中燃烧 B 铁丝在氧气中燃烧
C 一氧化碳还原氧化铁 D 稀释浓硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】端午节是中国传统节日,自古有吃粽子,赛龙舟,挂艾草,喝雄黄酒等习俗。
I.粽子:粽子是端午节的传统美食,其中鲜肉粽子的用料讲究,除了糯米,还有猪肉、蛋黄、食用盐、鸡精、白酒、植物油等,味道香糯可口,食之唇齿留香。
(1)粽子中的糯米富含的营养素是______。
(2)小海同学的午餐是鲜肉粽子,从营养均衡的角度来看,还需增加的食物是______。
A 馒头 B 鸡腿 C 青菜
(3)制作粽子的过程中,下列做法错误的是______。
A 因为粽子经过长时间高温烹煮,所以可用霉变的糯米洗净后制作
B 为使粽叶翠绿鲜亮,可用蓝色的硫酸铜溶液浸泡
C 用棉纱线捆扎包裹粽子
II.龙舟:制作龙舟常用樟木、桧木,现今也有用玻璃钢来制作,既环保又方便。

(4)樟木、桧木由复杂的多种有机物构成,如纤维素、半纤维素,木质素。其中纤维素______(填“属于”或“不属于”)有机高分子化合物。
(5)玻璃钢属于______材料(填序号)。
A 无机材料 B 合成材料 C 复合材料
III.雄黄酒:雄黄酒是用研磨成粉末的雄黄泡制的白酒或黄酒。古语曾说“饮了雄黄酒,病魔都远走”。雄黄的主要化学成分是硫化砷,如As4S4。雄黄加热后会转变为砷的氧化物,也就是剧毒品砒霜。从现代医学角度来看可能会对人体造成危害,不适宜食用。
(6)请写出+3价砷的氧化物的化学式______。
(7)用糯米酿制黄酒时,在酶的作用下,淀粉水解为葡萄糖,葡萄糖又在酶的作用下转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com