
科目: 来源: 题型:
【题目】如图 1 是 A、B、C 三种固体物质的溶解度曲线,请回答下列问题:
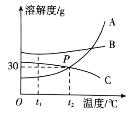
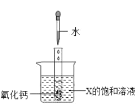
图 1 图 2
(1)t1℃时,A、B、C 三种物质的溶解度大小关系是______________________。
(2)t2℃时,把 30gA 放入 50g 水中,充分搅拌,形成溶液的溶质与溶液质量之比为____。
(3)向图 2 装有氧化钙的试管中滴入2mL 水后,若 X 中有固体析出,则 X为_______(选填“A、B、C”)。
(4)若饱和 C 溶液中混有少量 B,可采用_____________结晶提纯 C。
查看答案和解析>>
科目: 来源: 题型:
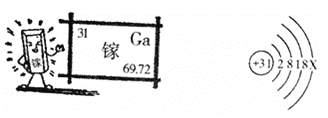
【题目】镓是一种奇妙的金属,放在手心马上熔化,犹如荷时上的水珠流来流去。
请阅读信息后回答:
(1)金属镓_____(填物理性质);
(2)镓原子结构示意图中X的数值______________;
(3)镓的氧化物的化学式______________;
(4)氮化镓(GaN)是第三代半导体材料,般采用GaCl3与NH3在一定条件下反应制得,同时得到另一种化合物。该反应的化学方程式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】使用尿素处理尾气可使重型柴油车达到国IV排放标准。其原理是尿素[CO(NH2)2]与汽车尾气中的氮氧化物(如二氧化氮)反应,生成无污染的气体排出。
(1)求算尿素相对分子质量的计算式:_____。
(2)补全尿素与二氧化氮反应的化学方程式:4CO(NH2)2+6NO2 4CO2+8H2O+_____。
4CO2+8H2O+_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】维生素C泡腾片深受广大消费者喜爱。小林同学查阅了相关资料,了解到泡腾片产生气泡的原因是发生了反应:3NaHCO3+C6H8O7=Na3C6H5O7+3CO2↑+3H2O。他为了测定泡腾片中NaHCO3的质量,进行了如下实验:称量加入水后的饮料瓶及瓶盖中的5片样品的总质量(如图),记录数据为448.50g。将样品加入水中,摇动至无气泡产生,再次称重饮料瓶及瓶盖,记录数据为446.30g。请计算:

(1)生成的CO2的质量为_____。(假设生成的CO2全部逸出)
(2)每片泡腾片中碳酸氢钠的质量。_____(假设泡腾片中的NaHCO3全部参与反应。写出计算过程及结果)
查看答案和解析>>
科目: 来源: 题型:
【题目】据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。

(提出问题)从废旧手机中可以回收到哪些有价值的金属?如何回收?
(查阅资料)
i.手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
市场价格($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。
ii.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。
Iii.2Cu+O2+2H2![]() 2CuSO4+2H2O
2CuSO4+2H2O
(实验方案)
第一步:选择值得回收的金属。
依据资料i中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①它们的市场价格较高;②_____。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | _____ |
III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如图所示装置中,进行实验。
| 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
V | _____ | 得到红色固体 |
(问题讨论)
(1)由步骤I中的现象,可推知的焊锡的物理性质是_____。
(2)步骤II对应的实验现象是_____。
(3)步骤II所得溶液中,一定含有的金属元素是_____。
(4)步骤V的操作是_____。
(反思交流)
为了确认步骤IV中滤纸上的金属成分,应进一步查阅的资料为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究发现燃烧排放的气体中,CO2浓度(用体积分数表示)越高,越容易被收集。与传统的燃料燃烧方式相比,化学链燃烧具有排放CO2浓度更高,易于收集的优点。下图为利用镍元素(Ni)进行化学链燃烧的原理示意图。

(1)空气反应器中,金属镍与氧气在一定条件下发生燃烧反应,其化学方程式为______________。
(2)燃料反应器中发生的部分化学反应如下(在高温下进行):H2+ NiO![]() Ni+H2O CO + NiO
Ni+H2O CO + NiO![]() Ni+CO2 反应前后化合价发生改变的元素有________。
Ni+CO2 反应前后化合价发生改变的元素有________。
(3)与CO、H2直接在空气中燃烧相比,化学链燃烧从燃料反应器排放出的CO2浓度更 高的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学为了探究铁钉生锈条件,设计了如下实验。
序号 | ① | ② | ③ | ④ |
实验内容 |
|
|
|
|
实验现象 | 铁钉无明显变化 | 铁钉生锈 | 铁钉无明显变化 | 铁钉生锈,U型管左侧液面上升,右侧液面下降 |
(1)通过实验①、②对比得出的结论是_____。
(2)增加实验③的目的是_____。
(3)实验④中,导致“U型管左侧液面上升,右侧液面下降”的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国古代就已经掌握了多种金属的冶炼技术,下面三幅图分别描述的是古人炼铁、炼铜、炼锌的场景。

(1)图1中,古人将木炭与铁矿石堆入炉内,并鼓入空气,利用生成的CO将Fe2O3转化为铁单质。CO与Fe2O3反应的化学方程式为_____。
(2)图1中,为了保持炉内高温,需要不断拉动风箱使木炭充分燃烧。不断拉动风箱可以使木炭充分燃烧原因是_____。
(3)图2中,古人将铁片放入富含硫酸铜的小溪中,获取铜单质,该反应的化学方程式为_____。
(4)图3中,古人将炉甘石(主要成分为ZnCO3)和木炭一起密封在泥罐中,在下面垫上煤炭加热,冶炼锌单质。泥罐内发生的化学反应如下:
ZnCO3![]() ZnO+CO2↑;CO2+C
ZnO+CO2↑;CO2+C![]() 2CO;ZnO+CO
2CO;ZnO+CO![]() Zn(气态)+CO2;其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因:_____。
Zn(气态)+CO2;其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用下图所示装置进行实验,研究燃烧的条件。已知:白磷的着火点为40℃,红磷的着火点为240℃。
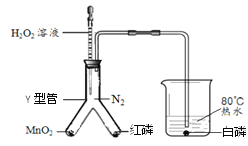
(1)当H2O2溶液与MnO2接触时,发生反应的化学方程式为________。
(2)检查上述装置气密性的实验方案是________。
(3)向Y型管中挤入H2O2溶液后,观察到导管口开始产生气泡时,烧杯中白磷不燃烧;一段时间后,白磷燃烧,此现象能够证明的可燃物燃烧的条件是________;若证明可燃物燃烧的另一个条件,依据的现象是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com