
科目: 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
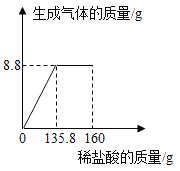
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
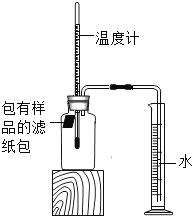
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.
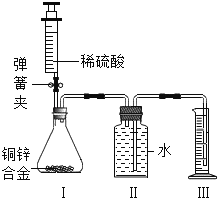
探究过程如下:
①连接实验装置并检查装置气密性.
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL.(注:样品中的杂质不参加反应)
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量1.4g.
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数.
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09g/L.
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为 ,实验过程中须加入稀硫酸至不再产生气体,目的是 .
(2)步骤③中称量剩余固体之前的正确操作是 、洗涤、干燥.
(3)根据实验测定的数据,上述三位同学中 (填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数.
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差.以下因素可能造成偏差的有 (填标号).
A.移出装置Ⅲ时,导管内留存了一部分水
B.实验测量前,没有排除装置Ⅰ中的空气
C.数据处理时,未排除加入稀硫酸所占的体积.
查看答案和解析>>
科目: 来源: 题型:
【题目】某蔬菜工厂欲配制无土栽培植物营养液,所用原料如下:(NH4)3PO4、KCl、NH4NO3、(相对分子质量分别是149、74.5、80)。如图是1000g植物营养液中各种营养元素的含量标准,请回答下列问题。
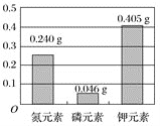
(1)写出配制1000g该植物营养液需要的(NH4)3PO4和NH4NO3的质量的计算式。(NH4)3PO4___。NH4NO3___。
(2)技术人员为了测定某次所配制的营养液是否符合标准,取400g所配营养液放入烧杯中,逐滴加入2%的氯化钡溶液直到不再产生沉淀为止,将沉淀过滤、洗涤、干燥得0.180g白色固体,请你通过计算确定该植物营养液中磷元素含量是否符合标准_____。[2(NH4)3PO4+3BaCl2==Ba3(PO4)2↓+6NH4Cl;Ba3(PO4)2的相对分子质量是601]。
查看答案和解析>>
科目: 来源: 题型:
【题目】请你参与以下2个实验探究活动并回答其中的问题。
Ⅰ SO2和Cl2均能将湿润的有色物质漂白成无色物质。某兴起小组为验证SO2和Cl2的漂白性,设计了如下方案(尾气处理装置未画出)。
(1)如下图所示,通入干燥的Cl2后,同学们发现甲中红色布条不褪色,乙中红色布条褪色了,此实验中控制的变量是_________,该实验中发生了“Cl2+H2O=HCl+HClO”反应,若要说明HClO具有漂白性,需要补充的实验是__________。将乙中的布条取出烘干,发现未变为原来的红色,说明HClO漂白性是_______(填“可恢复的”或“不可恢复的”)。
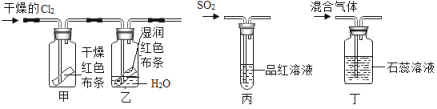
(2)如图丙所示,向品红溶液中通停止通气体,加热试管,发现试液又变为红色,说明SO2漂白的反应原理与Cl2漂白的反应原理是_____________(填“相同的”或“不同的”)
(3)如图丁所示,将干燥的Cl2和SO2按分子数之比1:1混合,通入石蕊试液中,发现石蕊试液变红,却不褪色。试用化学反应方程式作出解释(已知:生成物中氯元素显-1价,硫元素显+6价):__________。
Ⅱ Fenton法常用于处理含难降解有机物的工业废水,其原理是利用Fe2+和H2O2的反应产生能降解污染物的活性成分,现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或者40℃(其余实验条件见下表),设计如下对比试验。
(1) 请完成以下实验设计表(表中不要留空格)
实验编号 | 实验目的 | 温度 ℃ | pH | 浓度/(mgL-1) | |
H2O2 | Fe2+ | ||||
① | 为②③提供参照 | 25 | 3 | 204 | 16.8 |
② | 探究温度对降解反应速率的影响 | ___ | ___ | 204 | 16.8 |
③ | _____________________________ | 25 | 10 | 204 | 16.8 |