
科目: 来源: 题型:
【题目】胃酸的主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g-7.3g。某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用下图所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O。请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是___克?理论上能否使该患者胃液恢复到正常范围?____
xxx牌复方抑酸剂
有效成分:氢氧化镁
作用用途:用于治疗胃酸过重
用法用童:口服,每次2片,每天3次
药物含量:每片含0.145g氢氧化镁
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为实验室用一氧化碳还原氧化铁的实验装置图。
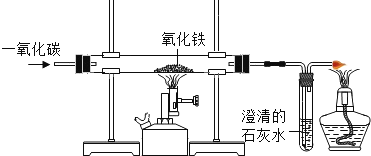
(1)硬质玻璃管中的实验现象是________,该化学反应方程式为_________。
(2)右边试管中的澄清石灰水中产生的实验现象是____,化学反应方程式是_______。
(3)实验过程中,常在装置图的末端的导管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___。
(4)通过此实验,我们可认识到CO和CO2的化学性质有许多的不同。请写出其中的一点:_______。
(5)试从微观的角度分析CO和CO2化学性质不同的原因:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取气体所需的装置如下图所示,请回答下列问题。
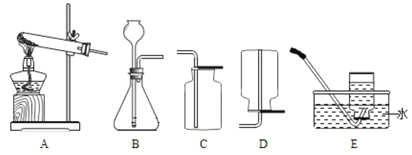
(1)实验室制取二氧化碳所选用的发生装置为__________,收集装置为__________(均填字母);选择气体收集方法时,气体的下列性质:①颜色、②密度、③溶解性、④化学性质,必须考虑的是__________(填序号)。
(2)实验室用A装置制取氧气,最好要在试管口_______________,反应的化学方程式为__________;为了做细铁丝在氧气中燃烧的实验,收集氧气的装置最好用___________,其原因是__________、__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧气的化学性质比较活泼,能支持燃烧。下图是木炭在氧气中燃烧实验的示意图,请对该实验进行分析并回答。

(1)图①中仪器a的名称是_____.
(2)从燃烧条件的角度分析,图②加热木炭的目的是_____.
(3)图②中熄灭酒精灯的规范操作是______.
(4)图③中木炭在氧气里燃烧比在空气里燃烧要剧烈,说明了_____.
(5)图④在整个实验设计中的目的是_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。
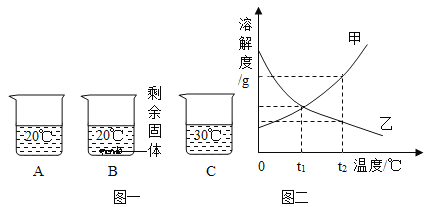
(1)烧杯中的溶液一定属于饱和溶液的是___(填序号);
(2)图二能表示NaNO3溶解度曲线的是___(填“甲”或“乙”);
(3)欲除去混在甲中的少量乙物质将可采用的方法是___;
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的___(填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】水是生命的源泉,也是不可缺少的资源。
(1)人们长期饮用硬水会影响身体健康。生活中常采用____方法将硬水转化为软水。
(2)某学校饮水机可以将自来水净化为饮用水,其中处理步骤如图所示:
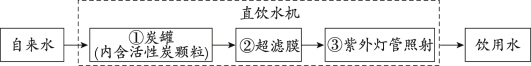
①对应的作用是____。
(3)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气,请写出反应的方程式____,从能量变化角度看,该反应是____转化为化学能。
(4)节约用水和合理开发利用水资源是每个公民应尽的责任和义务,下列做法与之不相符的是____。
A 合理施用农药、化肥 B 工业废水直接排放
C 提倡使用无磷洗衣粉 D 洗菜、淘米的水用来浇花、冲厕所
查看答案和解析>>
科目: 来源: 题型:
【题目】化学方程式的书写是学好化学的关键,但是很多同学在刚刚学习化学方程式书写时常常会犯一些错误,具体概括如下:①生成物化学式书写错误 ②未配平 ③遗漏反应条件 ④“↑”或“↓”使用不当,请你判断下列化学方程式的错误类型(填序号)。
序号 | 化学方程式 | 错误类型 |
(1) | 镁条燃烧:Mg+O2 | ______ |
(2) | 用硫酸铜溶液和氢氧化钠溶液混合: CuSO4+NaOH=Na2SO4+Cu(OH)2↓ | _____ |
(3) | 高炉冶炼赤铁矿:3CO+Fe2O3=Fe + 3CO2↑ | ____ |
查看答案和解析>>
科目: 来源: 题型:
【题目】根据化学式的计算,是所有化学计算的基础,包含了相对分子质量(Mr)、元素质量比、元素质量分数等方面,其计算原理如下:
Ⅰ、相对分子质量计算:化学式中各元素的相对原子质量之和,如:(注:相对原子质量:C—12;O—16,下同)CO2:Mr=12+16×2=12+32=44。
Ⅱ、纯净物中各元素的质量比:化学式中各元素的相对原子质量之和的比值,如:CO2:碳、氧元素的质量比:C∶O=12∶(16×2)=12∶32=3∶8。
Ⅲ、纯净物中某元素的质量分数:化学式中某元素的相对原子质量之和占相对分子质量的百分比,如:CO2:氧元素的质量分数:![]()
![]()
![]() 。
。
结合上述信息,根据化学式:Fe2O3;请计算:(相对原子质量:Fe—56;O—16)
(1)计算Fe2O3的相对分子质量(Mr):_____;
(2)计算Fe2O3,铁、氧元素的质量比:_____;
(3)计算Fe2O3,铁元素的质量分数:_____;
(4)160gFe2O3含有铁元素的质量为_____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】定量分析,是研究化学的一种重要手段,质量守恒定律更是初中化学的重要理论之一,它反映了化学反应前后的总质量是不变的,即:参加反应的各物质(反应物)的质量总和等于反应后生成的各物质(生成物)的质量总和。
请依照上述理论,试计算
(1)用试管加热24.5g氯酸钾和5g二氧化锰的混合物,待其充分反应后称量,试管内剩余固体质量为19.9g,则产生的氧气质量为_____g。
(2)已知:氢气燃烧的产物是水。往某密闭容器中加入3g氢气和16g氧气,用电火花点燃气体,待其充分完全反应后,发现容器内剩下1g氢气,则生成的水的质量为_____g;通过简单计算,发现在这个反应中,氢气、氧气和生成的水三种物质的质量比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:氧化铜[CuO]能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
(猜想)
Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质都不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质都发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____。
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
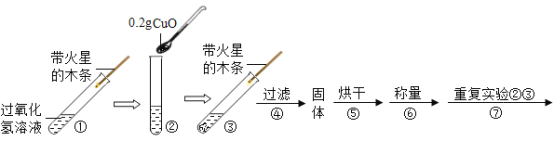
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____,带火星的木条复燃。 | _____ | 溶液中有气泡放出,_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)过氧化氢能被CuO催化分解放出O2的反应式为_____。
(实验拓展):
(3)某同学想比较二氧化锰和氧化铜对过氧化氢分解的催化效果,他需要对某些变量进行控制,其中包括有:_____。(至少三点)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com