
科目: 来源: 题型:
【题目】某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速度很慢,产生的气泡很少。为此,他们进行了如下探究。

(猜想与假设)
① 速度慢、气泡少可能与过氧化氢溶液的浓度有关。
② 速度慢、气泡少可能与MnO2的质量有关。
(进行实验)根据如图进行如下实验。
实验1:用26 mg MnO2与5 mL不同浓度过氧化氢溶液进行实验,压强变化如图1。
实验2:用5 mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如图2。

(解释与结论)
(1)过氧化氢溶液与MnO2制取氧气的化学方程式为______。
(2)实验1得到的结论是_______。
(3)实验2的目的是_______。
(4)欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比______。
(反思与评价)
(5)小组同学在制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是______。
(6)利用上图装置探究“温度对过氧化氢分解速率”的影响,是否合理,理由是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用下列物质和下图所示装置研究燃烧的条件。
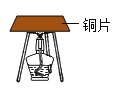
已知:酒精灯火焰的温度约为500℃;一些物质的着火点如下表所示。
物质 | 密胺 | 无烟煤 | 木材 | 红磷 |
着火点/℃ | 790~810 | 700~750 | 250~330 | 240 |
(1)实验1:研究达到着火点是燃烧的条件之一。完成该实验可以选取的两种物质是______。
(2)实验2:将红磷置于薄铜片上,用沙土覆盖,加热一段时间后熄灭酒精灯,再拨开沙土,红磷燃烧。红磷燃烧的原因是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】请从A或B两题中任选1个作答,若两题均作答,按A计分。
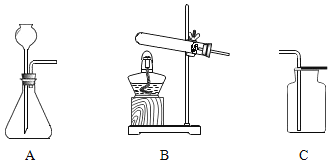
A | B |
(1)实验室制取二氧化碳,选取的发生装置是______。 (2)实验室制取二氧化碳的化学方程式为______。 | (1)实验室用高锰酸钾制取氧气,选取的发生装置是______。 (2)实验室用高锰酸钾制取氧气的化学方程式为______。 |
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文。
2017年5月15日是我国第24个“防治碘缺乏病日”。碘是人体必需的微量元素之一,有智力元素之称。人体内碘70%~80%分布在甲状腺内,缺碘会引起甲状腺肿大,幼儿缺碘会影响生长发育,造成思维迟钝。不同年龄人群对碘的生理需求量如下表所示(数据来自《中国居民膳食营养素参考摄入量》)。
年龄/岁 | 0~4 | 4~11 | 11~14 | >14 |
碘量(μg/d) | 50 | 90 | 120 | 150 |
食用加碘盐是摄入碘的重要途径。所谓加碘盐,就是在食盐中加入碘酸钾(KIO3)、碘化钾(KI)和海藻碘。2012年3月15日起,我国新《食用盐碘含量》规定,碘盐中碘含量平均水平(以碘元素计)为20 mg/kg~30 mg/kg。
碘化钾固体具有浓苦味,易潮解,在常温下久置会变质生成碘(I2)而呈黄色,须避光保存。根据《食盐加碘消除碘缺乏危害管理条例》(中华人民共和国国务院令第163号)第二章第八条的规定,食盐的碘添加剂应主要使用碘酸钾。
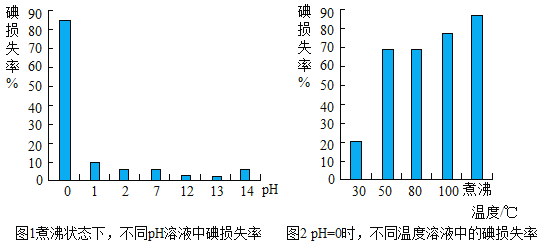
加碘盐要注意正确的使用方法,因烹饪方式不同,碘的损失率会有大幅度的波动。图1和图2是张小林等人对添加碘酸钾食盐的研究结果。
海藻碘盐是新一代的碘盐产品,热稳定性好,海藻碘更有利于人体的吸收,是理想的天然补碘品。
食用碘盐有益于人体的健康,但高碘地区的人群不宜食用碘盐,因为碘补充过量也会引起甲状腺肿大、智力下降等症状。因此,科学补碘意义重大。
依据文章内容,回答下列问题。
(1)7~10岁的儿童每天对碘的生理需求量为______ μg。
(2)KI的物理性质有______(答出一条即可)。
(3)补全碘化钾在常温下久置变质的化学方程式:4KI + O2 + _____ = 4KOH + 2I2。
(4)影响添加碘酸钾的食盐中碘损失率的因素有______。
(5)下列说法正确的是______(填序号)。
A 为了健康,补碘越多越好
B 海藻碘更有利于人体吸收
C 煮沸状态下,pH越大,碘的损失率越大
D 烹饪过程中,不宜在爆炒时放入添加碘酸钾的食盐
查看答案和解析>>
科目: 来源: 题型:
【题目】小明利用以下材料自制汽水。
材料:1.5 g小苏打(NaHCO3)、1.5 g柠檬酸(C6H8O7)、5 g蔗糖、1瓶纯净水
制备过程如下图所示:
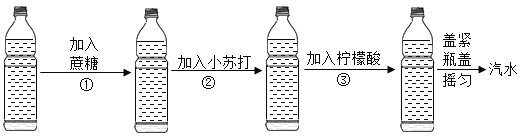
已知:小苏打与柠檬酸发生反应为3NaHCO3+ C6H8O7 = C6H5O7Na3+ 3H2O + 3CO2↑
(1)NaHCO3由________种元素组成。
(2)C6H8O7中碳和氢元素的质量比为________。
(3)自制汽水中,含有的物质有________(至少写出三种)。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用空气制取氮肥的主要流程如下.
![]()
(1)过程Ⅰ是利用空气中各成分沸点不同,分离得到N2,该过程发生的是_____(填“物理”或“化学”)变化.
(2)过程Ⅱ中,N2和H2反应生成NH3,该反应为_____(填“化合”或“分解”)反应.
(3)过程Ⅲ中发生反应的化学方程式为4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
若参加反应的NH3为68kg,理论上生成NO的质量为_____ kg.
(4)过程Ⅳ发生反应的微观示意图如下:
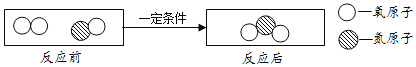
程Ⅳ发生反应的化学方程式为_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】钛(Ti)具有良好的耐热性和耐腐蚀性,其一个原子中质子数为22。以金红石(主要成分是TiO2)为原料生产钛的步骤主要有:① 在高温下,向金红石与焦炭(C)的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;② 在稀有气体环境和加热条件下,用Mg与TiCl4反应得到Ti和MgCl2。下列说法不正确的是
A.一个钛原子中核外电子数为22
B.①中得到的可燃性气体为CO
C.②中稀有气体的作用是隔绝空气
D.②中发生的反应为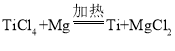
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。
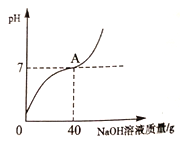
(1)图中A点表示的意义是____________________。
(2)A点消耗氢氧化钠溶液的溶质的质量为___________g。
(3)求石油产品中残余硫酸的质量___________g(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图所示(假设铁片除有Fe2O3外,不含其他杂质)。
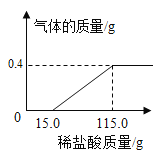
(1)生成氢气的质量为________g;
(2)所用稀盐酸中溶质的质量分数为________;
(3)计算该铁片中Fe2O3的质量分数为_______________(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.

【查阅资料】这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气.【实验1】小明选用如图所示装置中的 (选填序号)进行过碳酸钠与水的反应并收集产生的气体,经检验该气体是氧气,检验方法是
【提出问题】过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
【作出猜想】根据过碳酸钠与水的组成作出三种猜想.
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH.
【实验2】小明取溶液M,滴加CaCl2溶液,观察到有白色沉淀生成,他认为白色沉淀是CaCO3,溶液中一定含有Na2CO3.小刚提出质疑,产生的白色沉淀不一定是CaCO3,他的理由是: .
【实验3】小刚取溶液M,滴加稀HCl,观察到 ,证明溶液中一定含有Na2CO3,从而否定了猜想二.Na2CO3与稀HCl反应的化学方程式为 .
【实验4】为进一步确定溶液M中是否含有NaOH,他们向溶质M中滴加CaCl2溶液至不再产生沉淀为止,取上层溶液,加入 ,无明显现象.证明溶液中无NaOH溶液,猜想一正确.该实验中用CaCl2溶液而不用饱和石灰水,原因是: .
【反思拓展】
(1)根据过碳酸钠的性质,保存时应注意防潮.
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com