
科目: 来源: 题型:
【题目】下图是甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
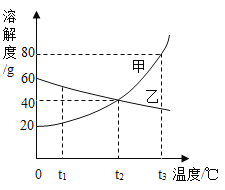
A.![]() 时,甲的溶解度大于乙
时,甲的溶解度大于乙
B.![]() 时,甲、乙两溶液的浓度相等
时,甲、乙两溶液的浓度相等
C.降温均可使甲、乙的不饱和溶液转化为饱和溶液
D.将180g甲的饱和溶液由![]() 降至
降至![]() ,可析出40g甲
,可析出40g甲
查看答案和解析>>
科目: 来源: 题型:
【题目】工业生产的纯碱产品中往往含有少量的氯化钠,某化学兴趣小组的同学通过实验来测定甲、乙两个品牌的纯碱样品中碳酸钠的质量分数。他们设计了如下的实验方案:
(方案一)沉淀分析法
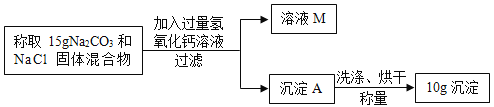
(1)第一组同学采用如上图所示的沉淀法对甲品牌纯碱样品进行测定;该方案中确定氯化钙溶液是否过量的方法是____________________。
(2)请根据上图所示的实验过程和提供的数据,计算甲品牌纯碱样品中碳酸钠的质量分数是______?(写出计算步骤,计算结果精确到0.1%)
(方案二)盐酸滴定法
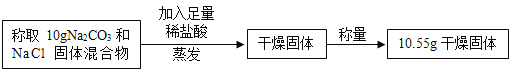
(3)第二组同学采用如上图所示的盐酸滴定法对乙品牌纯碱样品进行测定;用已知溶质质量分数的盐酸滴加到一定质量的混合物中,根据消耗盐酸的量来测定碳酸钠的含量,在实验过程中判断所滴加的稀盐酸恰好与碳酸钠反应的方法是_____________。
(4)请根据上图所示的实验过程和提供的数据,计算乙品牌纯碱样品中碳酸钠的质量分数是_________ (只写出计算结果)。
(方案三)气体分析法
(5)还有同学用设计的右图装置进行测定CO2质量(碱石灰的主要成分是氧化钙和氢氧化钠的混合物)。同学们指出该装置会导致实验结果偏大,请分析导致结果偏大的可能原因是________(选填序号)。
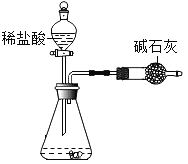
A.发生装置内残留的二氧化碳气体不能全部排到球形干燥管内
B.产生的二氧化碳气体中混有氯化氢气体,同时被碱石灰吸收
C.干燥管与空气相通,碱石灰即吸收发生装置产生的二氧化碳气体中混有的水蒸气,又吸收空气中的二氧化碳和水蒸气
D.发生装置漏气,产生的二氧化碳气体从胶塞处逸出
查看答案和解析>>
科目: 来源: 题型:
【题目】实验设计是化学实验的重要环节,请根据下列实验要求回答相关问题:
(活动与探究一)下图所示是用对比实验方法探究二氧化碳的性质。
实验一 | 实验二 |
|
|
实验一:振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C。其中B瓶石灰水变浑浊,此反应的化学方程式为____________________;对比A瓶与____(选填“B”或“C”)瓶的塑料瓶变瘪的程度,可证明二氧化碳能与氢氧化钠发生反应。
实验二:观察到C装置中发生的现象是:干燥的蓝色石蕊试纸______,湿润的蓝色石蕊试纸_______;此实验可证明二氧化碳能与水发生反应,此反应的化学方程式是_______________________。
(活动与探究二)下图所示是用控制变量法探究影响物质溶解性的因素。
实验三 | 实验四 |
|
|
实验三:该实验的目的是探究____________对硝酸钾溶解性的影响。
实验四:观察到的现象为氯化钠溶解于水中,不能溶解于酒精中。该实验的目的是探究__________________。(活动与探究三)下图所示是定量测定空气中氧气的含量。
实验五 | |
装置一 |
装置二 |
实验五:①装置一和装置二中气球的位置不同,装置一设计优于装置二的理由:_____________________________。
②根据下表提供的实验数据,回答问题:
硬质玻璃管的容积 | 反应前注射器中气体体积 | 反应后注射器中气体体积 | 实验测得空气中 氧气的体积分数 |
30mL | 20 mL | 12 mL | ______%(填写数值) |
③定量实验操作中易产生误差,如果反应前气球中存在少量气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果______(选填“偏小”、“偏大”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】航天科技飞速发展,密闭的飞船舱中是如何获得氧气并净化舱里的空气呢?为探究其反应原理,某化学兴趣小组的同学,在老师的指导下,进行了如下实验探究。
(查阅资料)①常温下,过氧化钠(Na2O2)固体与水反应,生成氢氧化钠和氧气。过氧化钠固体与二氧化碳反应生成碳酸钠和氧气。
②CO2难溶于饱和碳酸氢钠(NaHCO3)溶液。
(实验目的)探究二氧化碳与过氧化钠反应生成氧气,并收集干燥纯净的氧气。
(实验步骤)该小组同学根据实验目的,作出了如下实验设计(装置C、D内都是饱和溶液),请你参与并回答下列问题:
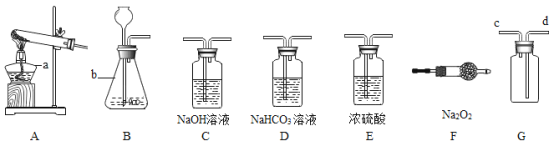
(1)写出上图中标号的仪器名称:a________;b__________。
(2)给A装置试管里的固体物质加热时,应先______,然后集中加热盛有药品的部位。实验室选B装置,用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式为__________________________。
(3)现需要得到纯净干燥的二氧化碳与Na2O2反应,实验装置正确的连接顺序是:B→____→E→F。(选填装置的字母序号,下同)说明你选择该装置的目的是____________________。
(4)若要收集到纯净于燥的氧气,实验装置正确的连接顺序是:F→_____→E→G。请说明你选择该装置的目的是_____________。装置E的作用是_________。证明装置G中氧气已收集满的方法是___。
(实验反思)反应后装置F中的过氧化钠固体是否完全反应?取少量反应后装置F中的固体于试管中,加入少量水后若观察到_______________,说明反应后装置F中的过氧化钠没有完全反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4以及一定量的CuSO4和Na2SO4。为减少污染并将其变废为宝,某学习小组设计以下流程,拟从该废水中回收硫酸亚铁、金属铜,并利用氨碱法原理“制碱”。(除标注外,其余所加药品或试剂均过量,部分产物及反应条件略去)请根据图示回答下列问题:
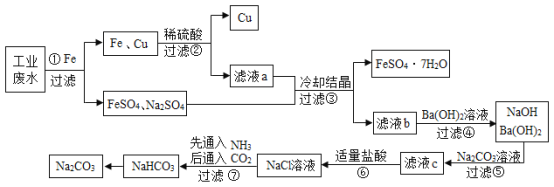
(1)由步骤①可知的金属活动性Fe比Cu___(选填“强”或“弱”)。在步骤①中向废水中加入过量的铁粉,过量的目的是______________。
(2)若向步骤②所得滤液a中滴加几滴紫色石蕊试液,溶液呈____色。
(3)步骤⑤中加入Na2CO3溶液的作用是___________________。
(4) “NaCl+CO2+NH3+H2O= NaHCO3+NH4Cl”是氨碱法制纯碱中重要的反应。
①将氨气通入饱和食盐水中,可制成饱和氨盐水(氨气极易溶于水)。氨盐水比食盐水更容易吸收二氧化碳的原因是:_________________。
②氨盐水吸收二氧化碳生成碳酸氢钠和氯化铵两种物质,更易析出的是NaHCO3,原因是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请从化学的视角认识生产生活中的有关问题,填写下列空格:
(1)现有水、氧化钙、氧气、铁四种物质,其中:(填写化学式)
①可供给生物呼吸的是______。②可作溶剂,对生命活动具有重要作用的是________。
③可用作干燥剂的是_______ 。④应用最广泛的金属是_______。
(2)化石燃料包括天然气、煤和______。木炭也可以做燃料,它在空气中充分燃烧的化学方程式是_______________。倡导“低碳”生活,主要是为了减少________的排放量。请结合生活实际,写出一条符合该主题的具体做法_______________。
(3)在人体所摄入的食物中,除空气、水、食盐等无机物外,其余主要是糖类、油脂、蛋白质和_______等有机化合物。它们为人体生命活动提供能量和物质基础。食物也是人体中各种元素的来源,我们必须均衡膳食,人体缺乏______(选填“铁”、“钙”或“碘”)元素可能导致骨质疏松,食用乳制品、豆类等可摄入该元素。
小资料:“84消毒液”有效成分是次氯酸
(4)“84消毒液”和“洁厕灵”是生活中两种常见的清洁剂请根据下图提供信息分析下列问题:
①用“洁厕灵”除垢对铸铁下水管有腐蚀的原因是_________________________。
②禁止两种清洁剂在一块混合使用的原因___________________。请写出“84消毒液”和“洁厕灵”它们混合,其有效成分之间发生化学反应的化学方程式___________________。
小资料:“84消毒液”有效成分是次氯酸钠(NaClO);“洁厕灵”有效成分是盐酸(HCl);它们混合,其有效成分之间能发生化学反应产生有毒气体氯气(Cl2)和氯化钠、水。氯气(Cl2)呈黄绿色,有刺激性气味,密度比空气大,有毒,吸入后会对上呼吸道黏膜造成伤害,症状严重时会致人死亡。少量氯气可通过碱性溶液除去。
查看答案和解析>>
科目: 来源: 题型:
【题目】2013年1月19日,首个《国际防治汞污染公约》发布.图为元素汞的信息,从图中获得的信息正确的一项是( )
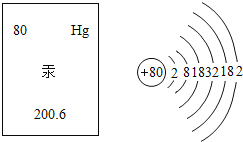
A.汞属于非金属元素
B.汞的核电荷数为80
C.汞的相对原子质量为200.6g
D.在化学反应中,汞原子容易得到电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学用语与其所表达的意义不一致的是
A.2N:两个氮原子B.Ca2-:一个钙离子
C.![]() :氧化镁中镁元素的化合价为+2价D.3H2O2:三个过氧化氢分子
:氧化镁中镁元素的化合价为+2价D.3H2O2:三个过氧化氢分子
查看答案和解析>>
科目: 来源: 题型:
【题目】食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中![]() 代表一个碳原子,
代表一个碳原子,![]() 代表一个氢原子,
代表一个氢原子,![]() 代表一个氧原子。下列说法不正确的是
代表一个氧原子。下列说法不正确的是

A.从类别上乙酸是一种有机化合物
B.从组成上乙酸是由碳元素、氢元素、氧元素组成
C.从构成上乙酸分子由2个碳原子和2个水分子构成
D.从定量上乙酸中碳元素的质量分数(C%)=![]() ⅹ100%=
ⅹ100%=![]() ⅹ100%=40%
ⅹ100%=40%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com