
科目: 来源: 题型:
【题目】建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验;取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。
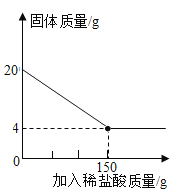
(1)20g赤铁矿石样品中氧化铁的质量为_______g;
(3)该样品中铁元素的质量分数为_______,由此判断出该赤铁矿石______(填“属于”或“不属于”)富铁矿石。
(4)计算试验中所用稀盐酸溶质的质量分数______(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】江西省积极落实化肥减量增效示范项目,并对在售的化肥提出明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取5.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入13%的BaCl2溶液产生沉淀的质量与所加入BaCl2溶液质量的关系如图所示(假定杂质不参加反应)。已知K2SO4+BaCl2=BaSO4↓+2KCl。

(1)恰好反应时,所用BaCl2溶液中所含溶质的质量为_____g。
(2)通过计算判断该钾肥中K2SO4的质量分数是否符合如图的包装说明_____?(写出计算过程)
(3)加入6gBaCl2溶液时溶液中K+和Cl﹣的个数比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某地一辆满载浓硫酸的罐车翻到,导致25t溶质的质量分数为98%的浓硫酸泄漏,并向路基两边蔓延,接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)25t溶质的质量分数为98%的浓硫酸中含H2SO4的质量为_______;
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙_______;
(3)处理一定量的硫酸,理论上既可用m1吨的氢氧化钙粉末,也可选用m2吨的氧化钙粉末,还可用m3吨碳酸钙粉末,则m1、m2、 m3的数值大小关系为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一道作业题:取100 g溶质质量分数为8%的氢氧化钠溶液倒入烧杯中,向其中加入100 g 19.6%的稀硫酸,充分反应后,求所得溶液中硫酸钠的质量分数。批改时老师发现两种答案:
结果编号 | ① | ② |
计算结果 | 14.2% | 7.1% |
请你分析并回答问题:
(1)氢氧化钠与硫酸反应时的质量比为________。
(2)请判断哪个结果是正确的______。(写出计算过程)
(3)反应前后钠元素的质量________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】做电解水实验时,常向水中加入稀硫酸以增强导电性,但硫酸并未参加反应。
(1)小明量取40 mL溶质质量分数为34%的硫酸溶液(密度为1.25 g/mL),其中溶质的质量为________g。
(2)将(1)中量取的硫酸溶液加水稀释成5%的稀硫酸,应加入水的质量为__________g。
(3)取90 g 5%的稀硫酸做电解水实验,通电一段时间后,收集到氢气的质量为2 g,求此时溶液中溶质的质量分数_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:请计算:

(1)20g样品中碳酸钠的质量为 g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水 g.
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用跑题的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图。

(1)上述反应产生二氧化碳的质量为 g;
(2)计算该赤铁矿石中氧化铁的质量分数;
⑶若上述反应后剩余固体质量为m克,写出计算该赤铁矿石中氧化铁质量分数的表达式: (用m表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】现有![]() 的
的![]() 溶液,请按照下面要求计算:
溶液,请按照下面要求计算:
![]() 上述溶液中所含溶质的质量为______。
上述溶液中所含溶质的质量为______。
![]() 上述溶液与足量
上述溶液与足量![]() 的盐酸反应,最多可生成
的盐酸反应,最多可生成![]() 多少克______?
多少克______?
![]() 向106g上述溶液中逐滴加入
向106g上述溶液中逐滴加入![]() 的盐酸并不断搅拌,此时发生的反应为:
的盐酸并不断搅拌,此时发生的反应为:![]() ;当
;当![]() 全部转化为
全部转化为![]() 后,再加入盐酸才开始放出
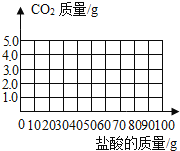
后,再加入盐酸才开始放出![]() 请在图中画出产生气体的曲线______。
请在图中画出产生气体的曲线______。
![]() 另取
另取![]() 溶液边搅拌边加入
溶液边搅拌边加入![]() 的盐酸,有关反应物与生成物的量如表格:
的盐酸,有关反应物与生成物的量如表格:
物质 |
| HCl | x | NaCl |
|
|
质量 |
|
|
|
|
| m |
则x是______;![]() ______。
______。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜片在空气中久置表面会变绿。某小组同学设计并进行实验,探究铜变绿的条件。
(查阅资料)(1)、铜绿的成分是碱式碳酸铜![]() ,碱式碳酸铜能够与盐酸反应。
,碱式碳酸铜能够与盐酸反应。
(2)、浓硫酸具有吸水性,可以作为一些气体的干燥剂。
(猜想与假设)常温下,铜片变绿可能与![]() 、
、![]() 、水蒸气有关。
、水蒸气有关。
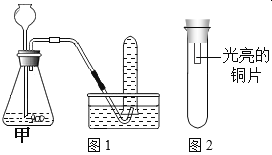
(进行实验)利用下图1装置分别制取并收集气体于试管中,制取气体原理及收集气体等操作见下表。将收集好的气体,用图2所示装置进行4个实验,通过控制与铜片接触的物质,进行实验并持续观察实验现象。
编号 | 主要实验操作 | 实验现象 |
1 | 甲中盛有过氧化氢溶液和二氧化锰,收集一试管气体 | 铜片始终无明显变化 |
2 | 甲中盛有大理石和稀盐酸,收集一试管气体 | 铜片始终无明显变化 |
3 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体 | 一段时间后铜片变绿 |
4 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体,并向气体中加入适量浓硫酸 | 铜片始终无明显变化 |
(解释与结论)
(1)实验1的目的是验证______。
(2)实验2制取气体反应的化学方程式为______。
(3)得出“铜片变绿一定与![]() 有关”的结论,依据的两个实验是______
有关”的结论,依据的两个实验是______![]() 填编号
填编号![]() 。
。
(4)实验4中,试管内的气体主要含有______。
(5)上述实验可推知,铜片变绿的条件是______。
(讨论与交流)
(6)同学们猜想碱式碳酸铜与盐酸反应有二氧化碳生成,证明此猜想所需试剂是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图1是实验室常用气体制备装置,据图回答问题:
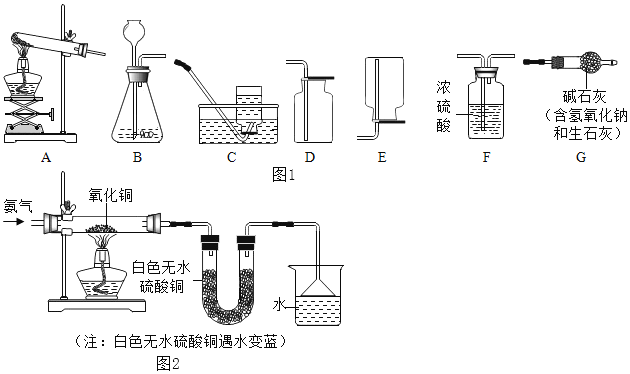
![]() 选择C装置收集氧气是因为______。将带火星的木炭伸入盛有氧气的集气瓶中,实验现象是______。
选择C装置收集氧气是因为______。将带火星的木炭伸入盛有氧气的集气瓶中,实验现象是______。
![]() 实验室制取氨气:
实验室制取氨气:![]() 固
固![]() 固)
固)![]()
![]() 固
固![]() ,要制取并收集干燥的氨气,所选装置正确的连接顺序是______
,要制取并收集干燥的氨气,所选装置正确的连接顺序是______![]() ______
______![]() ______
______![]() 填字母代号
填字母代号![]() 。
。
![]() 为探究氨气的性质,按如图2装置进行实验。观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成。
为探究氨气的性质,按如图2装置进行实验。观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成。
(查阅资料)氧化亚铜![]() 是红色固体,易与稀硫酸反应:
是红色固体,易与稀硫酸反应:![]() 。
。
(提出问题)得到的红色物质是什么?
(猜想)①是Cu;②是![]() ;③是______。
;③是______。
若猜想①成立,玻璃管中发生反应的化学方程式为______,说明![]() 具有还原性。
具有还原性。
(设计实验)请你设计一个简单的实验来验证红色物质中是否存在![]() :______。
:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com