
科目: 来源: 题型:
【题目】不少同学都被蚊虫叮咬过,感觉又痛又痒。同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内释放出蚁酸刺激皮肤,课外兴趣小组同学决定对蚁酸进行探究。
(提出问题)蚁酸的成分是什么?它有什么性质?
(查阅资料)蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
(实验探究一)探究蚁酸的酸性。
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成______色,说明蚁酸溶液显酸性;
(2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是__________(填名称)。
(实验探究二)探究蚁酸分解的两种产物。
(3)小芳同学根据蚁酸中含有_________元素,推测出生成物中含有水;
(4)另一种生成物是气体,小敏提出两种猜想:猜想①:该气体是CO2;猜想②:该气体是_________。他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。
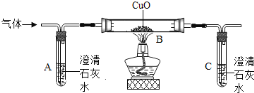
(5)实验时装置A中无明显变化,则猜想①_________(填“成立”或“不成立”);
(6)装置B中的现象是________,装置C中发生反应的化学方程式为________________。
(讨论交流)从环保角度看,该装置的缺陷是_________________。
(拓展延伸)
(7)当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你不会选择的物质是______。
A 牙膏 B 食醋 C 肥皂水 D 烧碱
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下图回答问题(本题的所有夹持仪器均已省略):
(1)写出指定编号仪器的名称:①____________。
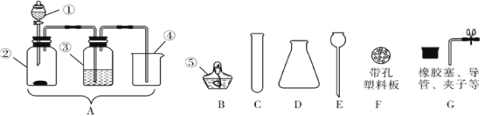
(2)实验室制取氧气,某同学设计了图A的装置,并用仪器④收集干燥的氧气。其中,仪器①中盛放的试剂应为___________ ,此法生成氧气的化学方程式为_________,该装置中有一处错误是:____。
(3)实验室用加热氯化铵(NH4Cl)和氢氧化钙两种固体混合物的方法制取氨气(NH3),同时得到氯化钙和水。该反应的化学方程式是____________。由此可见铵态氮肥不能与_____________物质混合使用。
(4)实验室制取二氧化碳,从B~G 中选择仪器,组装制取二氧化碳的发生装置,要求能方便控制反应的发生和停止,你的正确选择为________________ (填字母)。
查看答案和解析>>
科目: 来源: 题型:
【题目】盐能与许多物质发生复分解反应,请分析下列化学反应,并回答问题:
① BaCl2 + H2SO4 = 2HCl +BaSO4↓
② CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2↓
(1)从反应物的类型①是盐与酸的反应,②是盐与_________的反应。
(2)从复分解反应发生的条件分析,①和②都能反应的原因是生成物中都有__________。
(3)氯化钠俗名食盐,它的溶液也能跟____________ 溶液发生复分解反应,符合盐与盐之间的反应规律。
(4)在生活中纯碱(碳酸钠)是一种重要的盐,它与稀盐酸也能发生复分解反应。如果向5.3g碳酸钠粉末中,缓缓加入100g稀盐酸,若恰好完全反应。试计算:反应前稀盐酸中溶质的质量分数_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铝、铁、铜是我们生活中常见的金属.
(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与有关(填字母)_________。
A 金属的活动性 B 金属的导电性 C 金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是________________。
(3)每年全世界钢铁的产量很高,但钢铁的锈蚀给人类带来了的损失,铁在空气中锈蚀,实际上是铁跟_________和_______ 共同作用的结果;防止铁生锈的方法是______________(写一种);焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为_________。
(4)印发铜制电路板的“腐蚀性”为FeCl3溶液,反应化学方程式分别为①Cu+2 FeCl3=2 FeCl2+CuCl2;②Fe+2 FeCl3=3X.则②中X的化学式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)U形管中是滴有酚酞溶液的蒸馏水,向左、右两管中同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。
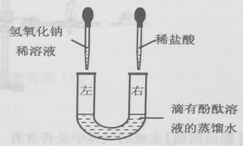
(1)开始时 管溶液呈红色。
(2)充分反应后U形管中溶液全部呈无色,除酚酞外,此时溶液中一定含有的溶质的名称为 ,可能含有的溶质的化学式为 ,写出上述反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】水和溶液在生命活动和生活中起着十分重要的作用。
(1)生活中可以用_________区分硬水和软水,可以通过________的方法降低水的硬度。
(2)海水中含有大量的氯化钠,可以通过_________方法获得粗盐,可用此方法提纯氯化钠的原因是____________ 。
(3)已知20℃时,氯化钠的溶解度为36g,则用18g氯化钠配制100g氯化钠溶液,所得溶液的浓度为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】酸、碱、盐在生产和生活中有着广泛的应用。
(1)氢氧化钠溶液和氢氧化钙溶液都能使酚酞溶液变红,其原因是二者的溶液中均含有相同的粒子________(填粒子符号)。
(2)钠与水反应,生成一种碱和密度最小的气体,该反应的化学方程式为___________。
(3)向一定量的稀盐酸和氯化镁的混合溶液中,逐滴加入10%的氢氧化钠溶液至过量,并测得溶液的pH随加入氢氧化钠溶液质量的变化曲线如图所示。
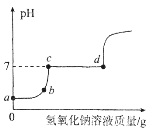
①b点溶液中含有哪些溶质__________________?(写化学式)
②写出c→d段反应的化学方程式__________________。
(4)某同学为了除去食盐水中的MgCl2、CaCl2、Na2SO4等杂质,设计了如图所示的实验方案。
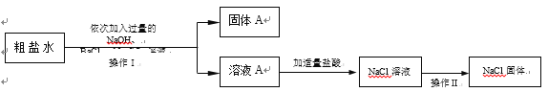
①操作II中玻璃棒的作用是___________?
②加入过量Na2CO3溶液的作用是____________________。
③写出该实验过程中发生的中和反应的化学方程式__________。
(5)为测定某石灰石样品中碳酸钙的质量分数,称取10 g石灰石(杂质不参加反应)放入烧杯中,加入100 g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7 g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数__________。
查看答案和解析>>
科目: 来源: 题型:
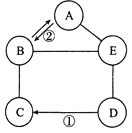
【题目】已知A、B、C、D、E分别为氧化铁、硫酸、氢氧化钠、氯化铁和碳酸钠中的一种,他们之间的反应或转化关系如右图所示(部分物质及反应条件已略去),其中C的溶液显黄色,B和E的反应类型为中和反应。A的俗称为_______。写出反应①、②的化学方程式_________________、_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com