
科目: 来源: 题型:
【题目】化学是一门以实验为基础的科学,请结合如图回答问题:
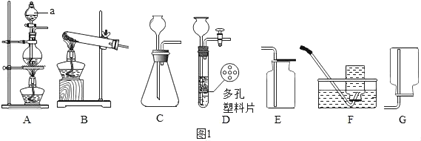
(1)仪器a的名称是___。
(2)在确定实验室制取氧气的化学反应时,不需要考虑的因素是___(填字母)。
a.原料中是否含有氧元素b.原料的产地c.实验装置是否容易装配
d.实验条件是否容易控制e.实验操作是否安全可靠
(3)实验室制取二氧化碳的化学方程式为__。可选用如图中C、D发生装置,D与C相比优点是__,收集二氧化碳可选择__(填装置序号)。
(4)实验室制取氯气。
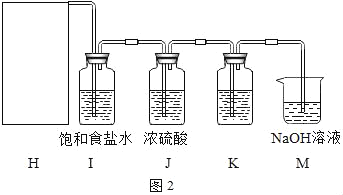
资料:通常情况下,氯气是黄绿色有刺激性气味的有毒气体,可溶于水,密度比空气大;能与金属、非金属、水、氢氧化钠溶液等反应。实验室常用二氧化锰固体和浓盐酸加热制取氯气。
①如图中H处为制备氯气的装置,应该选择如图中的___(填装置序号)。
②M装置的作用是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现,NH3燃烧的产物没有污染,且释放大量能量,有一定的应用前景,其反应的微观示意图如图所示。
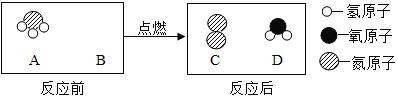
(1)图中B反应物的微观示意图是_____。
(2)该反应的化学方程式为_____,基本反应类型为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回答下列问题:
(1)20°C时,150g水中溶解_________g甲物质恰好形成饱和溶液。
(2)现有60℃的乙的饱和溶液,与该溶液有关的量有:
A.水的质量
B.溶液中溶质的质量
C.溶液的质量
D.乙的质量分数
E.60℃时乙的溶解度
①保持温度不变,将该饱和溶液稀释,不变的量是______(填序号,下同);
②如果将该饱和溶液降温至20℃,不变的量是_____。

查看答案和解析>>
科目: 来源: 题型:
【题目】广东乐昌古佛岩,因洞内的石笋和钟乳石,形状如仙似佛,前人在洞内安放过佛像,在洞口又建有佛寺而得名。石笋和钟乳石是由上亿年前海底沉积的石灰岩形成的,石灰岩的主要成分是碳酸钙。请用化学用语描述下列带点部分:
(1)碳酸钙中的金属元素:_____。
(2)碳酸钙中所含的阴离子:_____。
(3)碳酸钙中碳元素的化合价为+4价:_____。
(4)溶洞中钟乳石的形成是碳酸钙与二氧化碳、水反应生成可溶性的碳酸氢钙,碳酸氢根(HCO3﹣)也是常见的原子团,化合价为﹣1价,则碳酸氢钙的化学式为:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下图,回答下列问题:
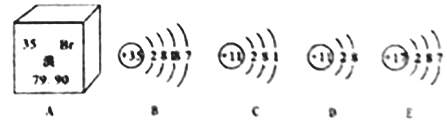
(1)图A所示中溴的相对原子质量是__________________;
(2)与B的化学性质相似的粒子是___(填字母序号);
(3)D的粒子符号为____________________;
(4)B与C形成化合物的化学式为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组同学为回收一块质量为26g的铜锌合金中的铜。将该合金放入烧杯中,滴加稀硫酸至不再产生气泡时,恰好用去稀硫酸100g,过滤,得滤渣和滤液,将滤渣洗涤晾干称重为19.5g。再向反应后的滤液中加入54.7g水进行稀释。请计算:
(1)黄铜中锌的质量_____;
(2)所用稀硫酸中溶质的质量分数_____;
(3)滤液加水稀释后,所得溶液中溶质的质量分数_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】阿司匹林是一种常见的解热镇痛药,其化学式为C9H8O4。
(1)阿司匹林由_____种元素组成。
(2)每个阿司匹林分子由_____个原子构成。
(3)阿司匹林中氢、氧元素的质量比为_____。
(4)阿司匹林中氧元素的质量分数_____(计算结果精确至0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C是初中化学常见的物质。在以下两种情况下,A、B、C中均有两种物质为氧化物。
(1)若向A中加入B物质,则生成C,C溶液pH>7,A、C含有相同的金属元素,该反应的化学方程式为_____。若将A放入饱和的C溶液中,出现白色浑浊,该白色浑浊物为_____。
(2)若A含四种元素,A可以通过发生分解反应同时生成B和C,则A的俗名为_____,该反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁、戊、己六种初中化学常见的物质都是由C、H、O、Na、Ca中的元素组成,其中甲~戊是由两种或三种元素组成的化合物,己是非金属固体单质,甲和乙是常用的灭火剂,丁可发生中和反应。它们转化关系如图一所示(反应条件、部分反应物或生成物略去)。
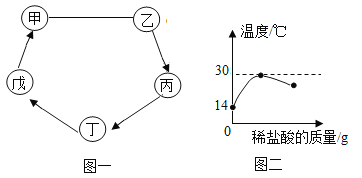
(1)物质乙的化学式为_____。
(2)生成物质丁的化学方程式为_____。
(3)下列物质既能与丙又能与戊发生化学反应的是_____(填序号)。
A 锌 B 稀硫酸 C 氧化铁 D 氯化钡
(4)室温下,将稀盐酸慢慢滴入盛有丁溶液的烧杯中,溶液温度随加入盐酸的质量而变化的曲线如图二所示。
①请解释ab段温度变化的原因_____。
②表示恰好完全反应的点是_____。
(5)现有物质己与氧化铜两种粉末的混合物30g,其中氧元素的质量分数为19%,放入带有气体导管的大试管中,高温加热该混合物一段时间后,产生4.4g二氧化碳,则剩余固体中氧元素的质量分数是_____(计算结果保留至0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】能源、水和溶液与人们的生活息息相关。
(1)目前人们利用最多的化石燃料是煤、_____和石油。
(2)车用乙醇汽油可适当节省石油资源,并在一定程度上减少汽车尾气的污染,乙醇燃烧的化学方程式为_____。
(3)检验水是硬水还是软水,可用的物质是_____,日常生活中使硬水软化的方法是_____。
(4)表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃ | 20 | 40 | 50 | 60 | 80 | |
溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
K2CO3 | 110 | 114 | 121 | 126 | 139 | |
Ca(OH)2 | 0.17 | 0.16 | 0.14 | 0.12 | 0.09 | |
①80℃时,KNO3的溶解度_____K2CO3的溶解度(填“>”、“=”或“<”)。
②50℃时,200g饱和K2CO3溶液蒸发10g水后,再降温到50℃,可析出K2CO3晶体的质量是_____g。
③将100g 60℃的Ca(OH)2饱和溶液降温至20℃,溶液中溶质的质量_____(填“变大”、“不变”或“变小”)。
④40℃时,向两个分别盛有相同质量的KNO3和K2CO3的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图所示。下列有关说法中,正确的有_____(填序号)。
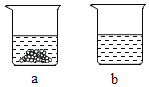
A 烧杯a中溶质是KNO3,烧杯b中溶质是K2CO3
B 烧杯b中溶液一定是不饱和溶液
C 降低温度或蒸发都有可能使烧杯b中析出固体
D 若将烧杯a中的溶液变为不饱和溶液,溶液中溶质质量分数定会减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com