
科目: 来源: 题型:
【题目】选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数为10%的氯化钠溶液。下列说法正确的是( )
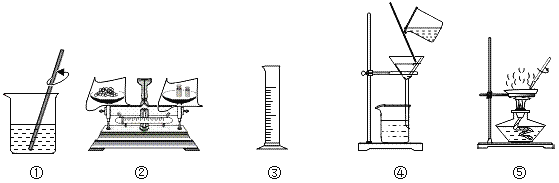
A. 操作①和⑤中玻璃棒的作用是相同的
B. 甲实验和乙实验都要用到的实验操作①
C. 甲实验在操作⑤时,将水全部蒸发后停止加热
D. 乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小
查看答案和解析>>
科目: 来源: 题型:
【题目】我国约在南北朝时就开始冶铸黄铜,黄铜是铜和锌的合金,它可用来造机器,电器零件及日用品,为了测定某黄铜样品中铜的质量分数,取10g黄铜加入到50g稀硫酸中,恰好完全反应,产生氢气0.1g。试求:
(1)该黄铜样品中铜的质量。
(2)反应完毕后溶液中溶质的质量分数(结果保留一位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图,表示某些物质间的转化关系(反应条件均略去).其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属。B、D、E均为无色气体。请回答:
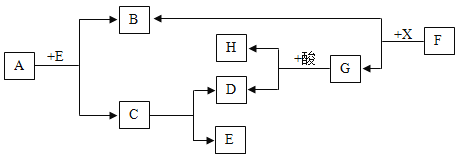
(1)X是_____或_____(填化学式)。
(2)B物质固态时的名称是_____,该固态物质在实际生活中的一种用途是_____。
(3)写出下列反应的化学方程式:
①A+E→B+C_____。
②C→D+E_____。
③G与E的反应_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是A、B、C三种固体物质的溶解度曲线如图所示,请回答:
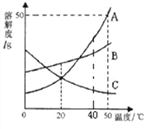
(1)20℃时,A、B、C三种物质的溶解度大小关系是______;
(2)50℃时,向50g水中加入50g A固体,所得溶液中溶质的质量为_______g。
(3)下列说法不正确的是___________。
①将50℃时A、B、C的饱和溶液降温到20℃,溶质质量分数从大到小的顺序是B A=C
②将50℃的C的不饱和溶液变为饱和溶液,溶液质量、溶剂质量、溶质质量分数不一定发生变化
③A中含有少量的B可采用海水晒盐的原理提纯A
④50℃时,将等质量的A、B、C三种物质分别加水完全溶解配制成饱和溶液,A所需要的水最少
⑤分别将40℃时三种物质的饱和溶液降温到20℃,A溶液中析出的晶体最多,C溶液中无晶体析出
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置图,回答有关问题:
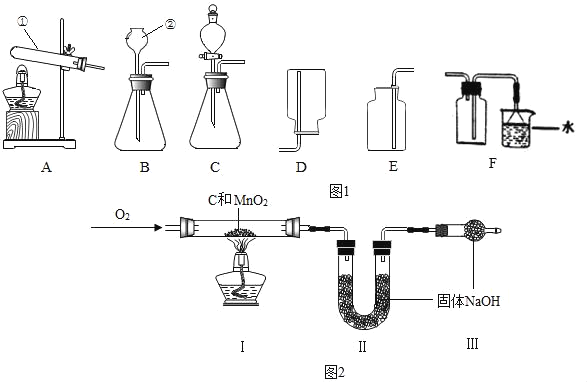
(1)写出图1中标号仪器的名称:①_____,②_____。
(2)实验室用高锰酸钾制氧气时发现水槽中水变红了,可能原因是_____。
(3)用双氧水制取氧气的化学方程式是_____,为得到平稳的氧气选用的发生装置是_____。用如图2装置从废旧干电池中回收MnO2并测定其含量,假设各步均完全反应,下列数据中可以计算样品中MnO2的含量的是_____。
a.反应前后氧气发生装置的质量
b.反应前后装置Ⅰ中固体的质量
c.反应前后装置Ⅱ中固体的质量
d.反应前后装置Ⅲ中固体的质量
(4)已知氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。实验室加热氯化铵和熟石灰固体制取并收集一瓶氨气,最佳的实验装置组合是_____。
(5)你认为实验室制取气体的反应,共同点是_____。
a.需要加热 b.反应物中没有气体参加
c.需要催化剂 d.反应物中必须含有要制取物质的元素。
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁是重要的金属材料,在生产、生活中有广泛的用途。建造北京奥运会主体育场“鸟巢”,就用了大量的钢铁。
(1)钢铁属于________________。(填“纯净物”或“混合物”)
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的________和____________共同作用的结果。
(3)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法。这些方法都能防止锈蚀的共同原理是___________________________。
(4)写出赤铁矿炼铁的主要反应的化学方程式___________________________。
(5)金属矿物的储量有限,而且不能再生。目前世界上已有50%以上的废钢铁得到回收利用,其目的是_____________。(填“合理开采矿物”或“节约金属资源”)
查看答案和解析>>
科目: 来源: 题型:
【题目】为保护哈市的空气质量,降低汽车尾气的污染,哈市再次推出了气电混合动力公交车。目前,哈市电车公司101、102、103路公交线路的80台气电混合动力公交车齐上道。 混合动力公交车节油和节气,时速23公里内“静音”不烧气,减少尾气的排放。请回答下列问题:

(1) 该公交汽车车体外表的铁质外壳喷涂一层黄色漆,其目的是___________。
(2)该公交车在时速低于23公里行驶时,此过程中的能量转化是(用“―”表示转化)___________________。
(3) 该公交车的轮胎中的材料含有合成橡胶、炭黑和钢丝,该材料为_______(填字母)。
A.金属材料 B.复合材料 C.合成材料
(4) 在生活生产中,人们经常利用的能源有①______________________________等;随着科学技术的发展,人们正在利用开发其他新能源如太阳能等,新能源的使用的意义②______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】粗盐中含有多种可溶性杂质(SO42﹣、Mg2+、Ca2+等)和难溶性杂质(泥沙等),以下是粗盐提纯思维导图,下列有关说法中不正确的是

A. ①通过溶解、过滤操作,除去粗盐中难溶性杂质
B. ②、③、④通过加入相应试剂沉淀杂质离子,是因为相应离子在溶液中不能大量共存
C. 任意交换②、③、④中加入试剂的顺序并不影响杂质的除去
D. ⑤加入适量稀盐酸,调节溶液pH为7
查看答案和解析>>
科目: 来源: 题型:
【题目】下列应用及相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
A.用小苏打治疗胃酸过多2NaHCO3+H2SO4=Na2SO4+H2O+CO2↑ 复分解反应
B.用红磷测定空气中氧气含量4P+5O2![]() 2P2O5 氧化反应
2P2O5 氧化反应
C.用木炭还原氧化铜2CuO+C![]() 2Cu+CO2↑ 化合反应
2Cu+CO2↑ 化合反应
D.用盐酸除铁锈Fe2O3+6HCl=2FeCl3+3H2O 复分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气是一种无色有刺激性气味的气体,密度比空气_____,是氮肥工业的重要原料。
(1)实验室常用浓氨水和氢氧化钠固体混合制取少量氨气,产生氨气的原因有:
①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,化学方程式为:_____![]() NH3↑+H2O。
NH3↑+H2O。
②氢氧化钠固体溶于水放热,使氨气在水中的_____,有利于氨气逸出。
(2)某化学兴趣小组为探究分子的运动情况,在玻璃管两端同时放入蘸有溶液的棉花,做了图1所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端。
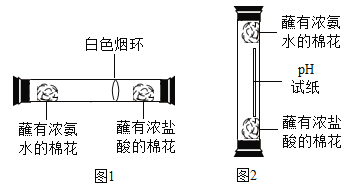
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是_____;
②写出该反应的化学方程式:_____。
(3)为了获得更好的视觉效果,该小组同学设计了图2所示实验。
(实验步骤)从玻璃管顶部将蘸有浓盐酸的棉花投入底部(过程中棉花不接触管壁),pH试纸迅速变为红色;再将蘸有浓氨水的棉花固定在玻璃管顶部,用摄像机记录实验现象。
(查阅资料)图3所示是本实验所用的pH试纸的显色范围。

(现象分析)图4所示是摄像机记录下来的pH试纸每15s的显色情况。
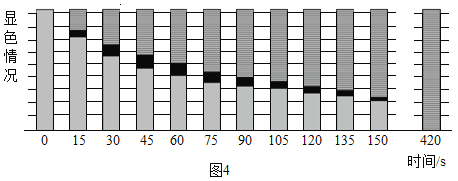
420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、_____和_____。
(拓展探究)上述实验中,若上下棉花颠倒,即玻璃管底部是蘸有浓氨水的棉花,顶部是蘸有浓盐酸的棉花,则pH试纸几乎直接变为绿色,玻璃管内迅速充满白烟,解释产生这种现象的原因:_____。
(4)氯化铵是一种常见的氮肥。某氯化铵化肥的含氮量经测定是25.2%,已知杂质不含氮元素,则此化肥中氯化铵的质量分数为_____(计算结果保留一位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com