
科目: 来源: 题型:
【题目】如图是元素周期表的一部分,试回答下列问题:
第一周期 | 1 H | 2 He | ||||||
第二周期 | 3 Li | 4 Be | 5 B | ① | 7 N | 8 O | 9 F | 10 Ne |
第三周期 | ② | 12 Mg | 13 Al | 14 Si | 15 P | ③ | 17 Cl | 18 Ar |
(1)写出①所示原子结构示意图_____。
(2)氯离子的最外层电子数是_____。
(3)②所示元素与③所示元素形成化合物的化学式是_____。
(4)地壳中含量最多的金属元素位于周期表的第_____周期,与地壳中含量最多的元素组成的化合物是_____(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是
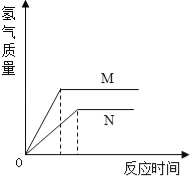
A. 金属的活泼性N>M
B. 两个反应生成H2的体积相等
C. 相对原子质量N>M
D. 两个反应消耗盐酸的质量一定相等
查看答案和解析>>
科目: 来源: 题型:
【题目】下列装置能达到对应实验目的是( )
A. 确认CO2和NaOH已发生反应
确认CO2和NaOH已发生反应
B.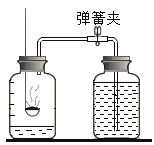 红磷燃烧测定空气中氧气的含量
红磷燃烧测定空气中氧气的含量
C.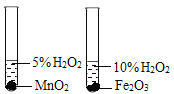 比较MnO2和Fe2O3的催化效果
比较MnO2和Fe2O3的催化效果
D.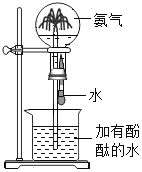 形成蓝色喷泉
形成蓝色喷泉
查看答案和解析>>
科目: 来源: 题型:
【题目】为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】 实验小组对甲酸的分解产物提出了猜想:
猜想1. H2和CO2; 猜想2. CO和H2O。
【设计实验】20℃时,甲酸的状态为______;从图一装置中选择合适的装置______(填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。
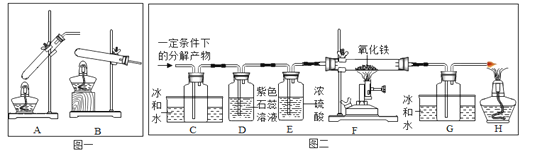
【实验预测】若猜想l成立,则D中的实验现象应为___________________________,所发生反应的化学方程式为__________________________________。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为_____________,所发生反应的化学方程式为__________________________________。甲酸分解的化学方程式为___________________________________。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3. H2O和CO2;猜想4.CO和H2。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E、F、I、X是初中化学中常见的物质,它们相互转化的关系如下图所示(图中反应条件已略去)。其中A、B含有相同的元素,B、D、E、X为氧化物,F是蜡烛;另外,I是一种黑色固体单质,在充足的气体单质C中燃烧生成气体D,在不充足的气体C中燃烧生成物质E(气体化合物CO)。请回答:
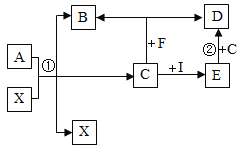
(1)A的化学式是________,X在反应①中起的作用是_________
(2)反应中,将气体D通入澄清石灰水中的现象是_________
(3)写出反应②的化学方程式:_________
查看答案和解析>>
科目: 来源: 题型:
【题目】氧气是人类无法离开的物质。在不同的生活、生产环境中对氧气浓度的要求不同,人类常采用不同的方法制取氧气。请根据下列信息及实验装置图回答有关问题。
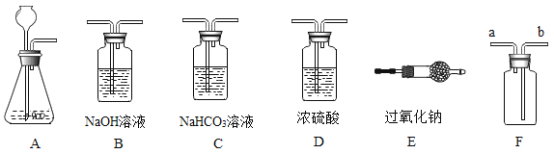
(1)工业上一般采用分离净化后的液态空气制取氧气。在生产中应控制温度的范围是_______。(已知在1.01×105Pa时,O2的沸点为-183℃,N2的沸点为-196℃)
(2)实验室可用双氧水制氧气,发生反应的化学方程式为__________
(3)过氧化钠(Na2O2)能与CO2反应生成一种碳酸盐和氧气,常用作呼吸面具中的供氧剂。
①实验室要得到纯净干燥的CO2与Na2O2反应制氧气,选择装置组合顺序是A→______→D→E (填装置编号) 。请写出你所选装置中发生反应的化学方程式:______。
②若要收集到纯净干燥的氧气还需将上述所得氧气先通装置B、D,最后用装置F来收集,其中装置B中反应的化学方程式为_________。检验装置F中氧气已收集满的方法是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种固体(均不含结晶水)的溶解度曲线如图所示,请回答:
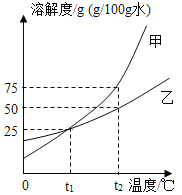
(1)t1℃时,甲的饱和溶液中溶质质量分数是________
(2)t2℃时,80g乙放入100g水中充分溶解,可以得到该温度时乙的________(填“饱和”或”不饱和”)溶液,溶液质量为_______
(3)将t2℃时等质量的甲、乙的饱和溶液降温至t℃(t1<t<t2)相关分析正确的是_______(填编号)
a t2℃时,甲、乙两溶液的溶质质量分数之比为75:50
b降温过程中,甲、乙两溶液的溶剂质量之比不变
c降温至t℃时,甲、乙两溶液的溶质质量可能相等
d降温至t℃时,甲、乙两溶液的质量可能相等
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表是化学学习和研究的重要工具。下图是元素周期表的一部分,请依据该表信息回答问题。
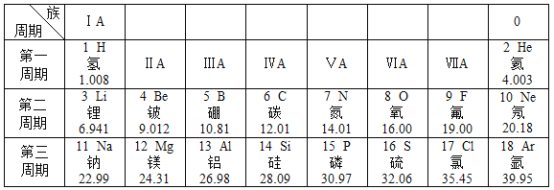
(1)表中不同种元素最本质的区別是________(填序号);
A质子数不同
B中子数不同
C相对原子质量不同
(2)某元素原子结构示意图为 ,该元素原子核内有_____个质子,原子最外电子层上有_____个电子,该元素符号为________。
,该元素原子核内有_____个质子,原子最外电子层上有_____个电子,该元素符号为________。
(3)请用表中的元素符号写出符合要求的化学反应方程式:有金属参加的化合反应是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com