
科目: 来源: 题型:
【题目】以下是实验室制取和收集气体的装置图:
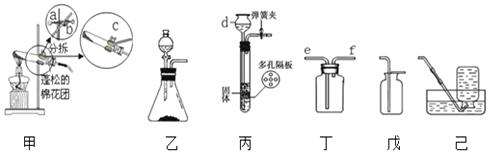
(1)仪器d的名称是_____,作用是_____。
(2)加热KMnO4制取O2,写出反应的化学方程_____;当用铁夹固定好试管后,要使试管口略低于试管底部,应调节螺旋_____(选填“a”“b”或“c”)。试管口放一团棉花的目的是_____,用戊装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?_____。
(3)实验室用锌和稀硫酸制取氢气,写出反应的化学方程式:_____;为使反应随开随制随关随停,应选用的发生装置是_____(选填装置编号)。若用装置丁作收集装置,收集时气体应从导管的_____(填“e”或“f”)端通入,若用装置丁作干燥装置,则应添加_____(填药品名称),气体应从导管的_____(填“e”或“f”)端通入。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是A、B、C三种物质在水中的溶解度曲线,根据图回答:
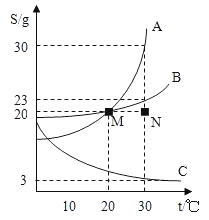
(1)在10℃至20℃之间,三种物质的溶解度大小顺序是_____。
(2)M点的意义:_____,该温度下30gA的饱和溶液溶质质量分数是_____(只列式不计算),N点是30℃B物质的_____溶液。
(3)若要从A中含少量B的混合物中分离出A,则可采用_____的方法进行。
(4)10℃时,三种物质的饱和溶液升温至30℃有晶体析出的是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】地球上水的分布是:海洋咸水97%,淡水3%,而淡水的分布又如图所示。
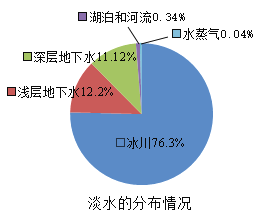
(1)淡水资源很有限,为了从海水中获得淡水,可采用的方法是_____(选填“过滤”或“蒸发”)。
(2)为了判断井水是硬水还是软水,可用_____进行检验。
(3)自来水生产中加氯气的反应原理是:氯气(Cl2)与水反应生成盐酸和次氯酸(HClO),请写出该反应的化学反应方程式_____;与净水器接通电源时产生紫外线类似,其作用是_____。
(4)春播时旱情严重,为缓解旱情,可使用液氮(N2)作为增雨剂实施人工降雨。根据你现有的知识推测下列说法中正确的是_____(填标号)。
A 液氮是一种溶液
B 液氮是由分子构成的
C 液氮气化时吸收热量
D 使用液氮会污染环境,应严格控制使用
(5)请你写出一条保护水资源的措施:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】非接触红外人体测温仪,对人体体温的检测能及时发现新冠病毒。按要求回答下列问题:

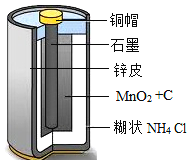
(1)其中属于有机合成材料的是_____。
(2)硫酸铜和锌发生反应的化学方程式为_____,说明金属活动性:铜比锌_____(填“强”或“弱”)。
(3)写出NH4Cl中氮元素的化合价_____,该物质在农业上可用作_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量变化趋势如图所示,下列说法正确的是( )

A.a点溶液中溶质只有AgNO3和Cu(NO3)2
B.b~c段之间的溶液中溶质只有Cu(NO3)2和Zn(NO3)2
C.取b~c段之间的溶液,滴加稀盐酸,一定有白色沉淀产生
D.取d点的固体,加入稀盐酸,一定无气泡产生
查看答案和解析>>
科目: 来源: 题型:
【题目】如图甲是铝元素在周期表中的信息,乙是氧元素的原子结构示意图。下列说法正确的是( )
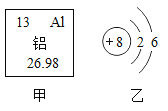
A.氧原子最外电子层易失去电子形成稳定结构
B.铝原子的相对原子质量是26.98克
C.铝原子核内含有13个质子
D.甲、乙两元素形成化合物的化学式为Al2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱工业是指用电解饱和NaCl溶液的方法来抽取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,电解饱和NaCl溶液的化学方程式为: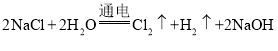 ,请计算:
,请计算:
(1)烧碱中三种元素的质量比m(Na):m(O): m(H)= 。
(2)用这种方法制备40t烧碱,需要NaCl的质量为 。
(3)若用25%的NaCl溶液按照上述方法电解并制取40t烧碱,完全电解后所得溶液的质量分数。( 假设生成的烧碱全溶,计算时若除不尽保留到1%) .
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钙可用于预防和治疗钙缺乏症。某实验小组同学要测定一种钙片中碳酸钙的含量。
[查阅资料]补钙剂中常加入糖类、维生素D等改善口感或增强药效。这些物质不与稀盐酸反应,高温灼烧时会燃烧或分解。
[设计实验]根据资料和已学知识,该小组同学设计如下两种实验方案进行测定。
方案①:根据下图所示装置实验。
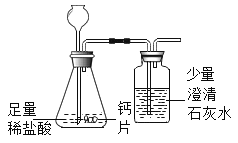
(1)锥形瓶中发生反应的化学方程式为___________________。
(2)长颈漏斗下端插入液面下的目的是___________________。
(3)记录数据如下:
钙片质量 | 空洗气瓶质量 | 澄清石灰水质量 | 反应后洗气瓶及瓶内物质总质量 |
25g | 100g | 50g | 150.4g |
方案②:将钙片粉碎,加入足量的稀盐酸充分反应,根据放出气体的量计算碳酸钙的含量。记录数据如下(空烧杯质量为100g, 加入钙片质量为25g):
加入稀盐酸的总质量 | 100g | 200g | 300g | 400g |
充分反应后烧杯及杯内物质总质量 | 222.8g | 320.6g | 418.4g | 518.4g |
[分析评价]
方案①和方案②中合理是方案___________________,原因是___________________。
[得出结论]经过计算,该钙片中碳酸钙的质量分数是___________________。
[反思回顾]该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】控制变量法是对比实验中的重要方法,我们在初中化学的学习过程中,做了如下含有对比思想的化学实验,回答下列问题。
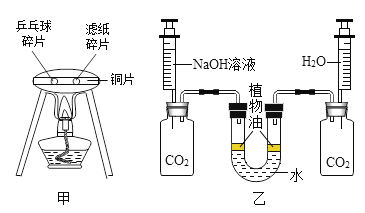
(1)实验甲的目的主要是对比出乒乓球碎片和滤纸碎片的_______________不同;
(2)实验乙利用对比实验排除了水对实验的干扰,若观察到U形管左端的液面_____________(填“升高”或“降低”),则证明溶液中的氢氧化钠能与二氧化碳反应,其反应的化学方程式为___________________。
(3)实验丙中,只有A中铁钉生锈了,对比铁钉不同的现象,可推知铁生锈的条件是铁与________________同时接触。下图的对比实验丙和丁能实现探究目的的是___________________(填序号)。
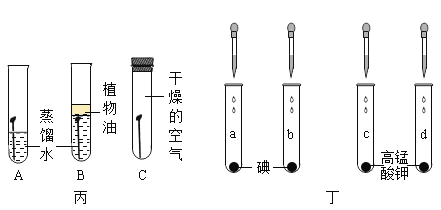
A 实验丙中A. B对比可探究铁的锈蚀与植物油是否有关
B 实验丙中A、C对比可探究铁的锈蚀与水是否有关
C 实验丁中a、b对比可探究物质溶解性与溶质种类是否有关
D 实验丁中b、d对比可探究物质溶解性与溶剂种类是否有关
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸钙转化为K2SO4和CaCl2的工艺流程如图:
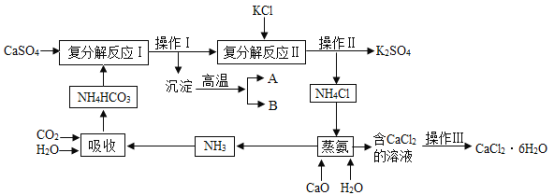
(1)吸收过程中发生了化学反应,其化学方程式为___________________。
(2)操作Ⅲ所需的玻璃仪器有___________________。
(3)蒸氨过程中一定没有涉及的反应类型是___________________(填序号)。
A 复分解反应
B 化合反应
C 分解反应
D 置换反应
(4)可循环利用的物质除了NH3外,还有_________________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com