
科目: 来源: 题型:
【题目】原子M的结构示意图如下,关于该原子的说法正确的是( )
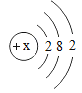
A.x可以是10
B.M为非金属元素
C.原子M在化学反应中不易得失电子
D.原子M与氧原子形成的氧化物的化学式是MO
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有一包食盐,已经过初步提纯,除去了难溶性杂质,但仍含有CaSO4、MgSO4、CaCl2、MgCl2杂质。现取该食盐样品20.000g,测得其中含有Ca、Mg两种元素共0.300g,S元素0.064g(其他杂质忽略不计)。
(1)该食盐中CaSO4与MgSO4的物质的量之和为mol。
(2)计算该食盐中NaCl的质量分数的范围。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工业生产流程如图所示:
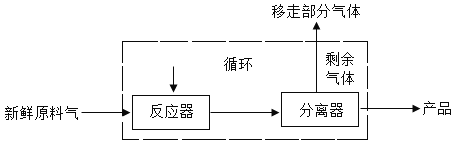
每生成1t 产品,需要通入含有0.2%(体积分数,下同)的惰性杂质CH4的新鲜原料气2800m3。
经分离器分离产品后,剩余气体中含有大量未充分反应的原料与 3%的CH4。在连续生产的条件下,可对剩余气体采用部分循环、部分移走的操作,一方面能提高原料的利用率,节省成本,另一方面也避免装置中CH4越来越多而对生产造成不利影响。已知在此生产条件下,CH4在每吨产品中的溶解量为2.3m3,。计算每生产 1t 产品需要移走气体的体积。
查看答案和解析>>
科目: 来源: 题型:
【题目】高炉炼铁所需的原料有铁矿石、焦炭、石灰石等,其过程可用下图简要表示:
已知气体①、气体②和固体③均属于氧化物。
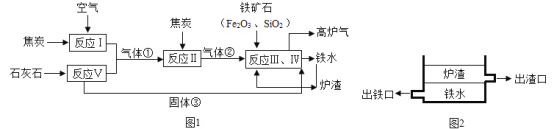
(1)气体②的化学式为_____。根据氧化物的性质推测炉渣的主要成分为_____(填化学式)。
(2)炼铁高炉底部通过不同高度的出口分离铁水与炉渣(如图2所示)。能实现渣铁分离的原因是是因为炉渣具有_____、_____的性质。
(3)反应Ⅰ~Ⅴ中属于化合反应的有_____个,属于分解反应的有_____个,属于置换反应的有_____个。
(4)高炉气体中含有多种成分,其中含量最高(占55%~60%)的是_____(填化学式),此外还含有25~30%的可燃性气体_____(填化学式),以及9~12%左右的_____(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2 和H2O(g)。半水煤气经过下列步骤转化为合成氨的原料N2和H2。
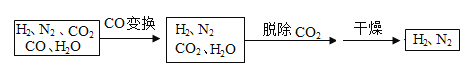
(1)在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了 CO 变换,其化学方程式为:________。
(2)吸收法是脱除CO2的方法之一。已知:
溶质 | Na2CO3 | K2CO3 |
20℃1L饱和溶液中溶质的物质的量mol | 2.0 | 8.0 |
溶质价格(元/kg) | 1.25 | 9.80 |
若选择Na2CO3溶液作吸收液,其优点是_;缺点是_。如果选择K2CO3溶液作吸收液,用某种方法可以降低成本,写出这种方法涉及的化学方程式:_。
(3)将一定体积半水煤气依次通过装置Ⅰ~Ⅴ(最后通入氮气确保反应、吸收完全),可以 测定其中H2以及 CO 的物质的量。
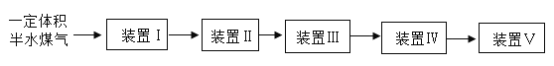
可供选用的装置如下所示(省略夹持仪器):
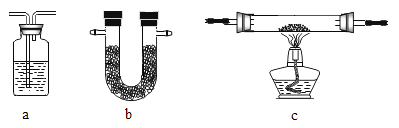
为装置Ⅰ~Ⅴ选择合适的装置与试剂:
装置 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
a | a | _ | _ | b | |
试剂 | _ | 浓硫酸 | CuO | _ | _ |
装置Ⅰ、Ⅱ的作用是____________。要确定半水煤气中H2物质的量,应测量的数据是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在图中的烧杯中盛有65℃的热水,杯底放有一小粒足够量的白磷,然后将一支有刻度的空试管垂直插入烧杯中,试管口罩住白磷。(已知白磷熔点 44℃,着火点为 40℃)。
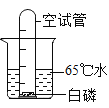
(1)写出实验过程中发生的现象_。
(2)该实验说明了_。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学研究亚硫酸钠(化学式为 Na2SO3)热分解反应时,作了两种假设:
假设一:它按 CaCO3 受热方式来分解。
假设二:它按 KClO3 受热分解方式来分解。
(1)假设一对应的化学方程式是________。确认假设二是否成立的简单实验操作是_____。
(2)该同学将取一定质量的样品置于坩埚中充分灼烧,发现最终得到固体质量较原样品质量增加了大约 12.7%。据此他认为_(选填编号)。
a 假设一成立
b 假设二成立
c 两种假设均不成立
固体质量增加可能的原因是________。
(3)在查阅资料后,该同学再次进行了实验。他将一定质量样品置于密闭真空容器中充分加热,最终得到固体质量与原样品相同。但进一步分析表明,该固体组成为两种新的钠盐,其物质的量之比为 1:3。请写出相应的化学方程式_。
(4)该同学想要进一步探究次氯酸钠(化学式 NaClO)的分解反应。他查阅资料后,得知NaClO 有多种热分解方式(每种分解方式的产物仅有两种)。若其中一种产物为 NaCl,则另一种产物可能是:________(选填编号)。
a Cl2
b O2
c Na2O
d NaClO3
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究某物质 X 对钢铁在潮湿环境下的腐蚀的影响作用,某同学进行了如下实验:
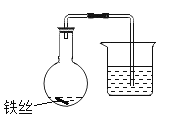
① 选择 6 个容量相同的烧瓶,分别编号为 1~6,加入规格、质量相同的铁丝。
② 向 1~3 号瓶中放入 2mL 清水,向 4~6 号瓶中放入 2mL10%X 的水溶液,将铁丝润湿。
③ 塞上带有导管的塞子,将导管末端浸入盛有水的烧杯中,记录导管内液面的初始位置(如图所示)。
④ 放在室温环境下,每隔一小时测量一次,周期为 3 小时,记录数据。结果如下表所示:
时间(小时) | 1 号瓶 | 2 号瓶 | 3 号瓶 | 4 号瓶 | 5 号瓶 | 6 号瓶 |
0 | 0 | 0 | 0 | 0 | 0 | 0 |
1 | 0 | 0.1 | 0 | 1.2 | 1.4 | 0 |
2 | 0.8 | 0.7 | 0.9 | 5.6 | 5.7 | 0.1 |
3 | 3.5 | 3.2 | 3.7 | 9.8 | 10.0 | 0.1 |
注:放置过程中导管内液面上升情况(单位:cm)
(1)在该项探究中,要取同样处置的 3 只烧瓶的目的是_。
(2)6 号瓶的数据明显与 4、5 号瓶不同,可能原因是_。
(3)通过本实验,可初步得出的结论是_。
(4)该项探究的设计是否存在不足_?如何改进_?
查看答案和解析>>
科目: 来源: 题型:
【题目】已知 CuS、Cu2S 粉末的颜色和 CuO 相似,且都不溶解于水。在空气中煅烧时,CuS 和Cu2S 都转化成 CuO 和 SO2。
(1)请写出 CuS、Cu2S 在空气中煅烧时发生反应的化学方程式:________、________。
(2)根据叙述,设计一个不用其他化学试剂鉴别 CuO、CuS、Cu2S三种粉末的实验方案(写明步骤与结论)________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物中某一种元素的原子短缺可形成非整比化合物,这类化合物中各类原子的相对数目不能用简单整数比表示,如Fe0.9O、PbO1.9等。非整比化合物是新型的功能材料,具有很大的科技价值。
(1)PbO1.9中铅元素具有+2、+4 两种价态,其中+4 价铅占铅总量的_______。
(2)如图所示,Fe0.9O可用于CO2的综合利用。
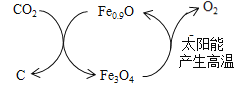
①请写出该转化的两个优点:___________、__________。
②若用1mol Fe0.9O与足量的CO2完全反应可生成_g C(碳)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com