
科目: 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线请认真分析并回答:
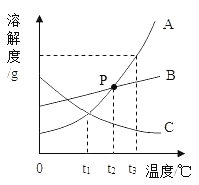
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为__________。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是________。
(3) P点表示的含义是_______。
(4)当A中含有少量的B,可采用_______(填“降温”或“蒸发”)结晶的方法提纯A物质。
(5)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A_______B(填“>”,“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列所示的四个图像,能正确反映对应变化关系的是
A.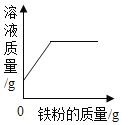 向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.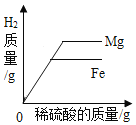 等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
C.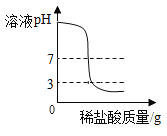 向一定量的氢氧化钠溶液中 滴加pH=3的稀盐酸
向一定量的氢氧化钠溶液中 滴加pH=3的稀盐酸
D.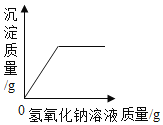 向一定量的含有 盐酸的氯化铜溶液中滴加氢氧化钠溶液
向一定量的含有 盐酸的氯化铜溶液中滴加氢氧化钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】2022 年第24届冬季奥运会将在我国举行。如图“五环”中,甲、乙、丙、丁、戊分别代表镁、水、二氧化碳、硫酸亚铁溶液、氢氧化钡溶液五种物质中的一种。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且乙的相对分子质量小于丁。下列说法错误的是
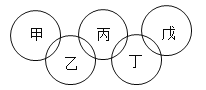
A.甲是水
B.乙和丙反应有白色沉淀生成
C.丁和戊反应后溶液质量增大
D.上述没有涉及的基本反应类型是分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】聚丙烯[分子式为(C3H6)n,缩写为PP]是生产口罩、防护服、注射器等医疗器材的原材料,工业上常用丙烯(C3H6)在一定条件下发生聚合反应生产聚丙烯,下列说法错误的是
A.聚丙烯和丙烯均属于有机物
B.聚丙烯中碳、氢元素的原子个数比为1:2
C.丙烯中碳元素的质量分数约为85.7%
D.1个丙烯分子由3个碳元素和6个氢元素构成
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某化学反应的微观示意图,下列有关说法正确的是
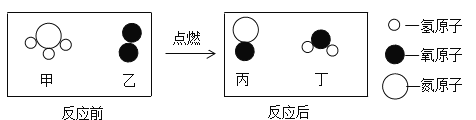
A.该反应属于置换反应
B.甲物质由一个氮原子和三个氢原子构成
C.生成的丙、丁两种物质的分子个数比为2:3
D.参加反应的甲、乙两种物质的质量比为17:32
查看答案和解析>>
科目: 来源: 题型:
【题目】2017 年5月,中国科学院发布了115号元素的部分信息如图所示,有关该元素的说法正确的是
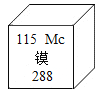
A.电子数为288
B.属于非金属元素
C.相对原子质量为288g
D.中子数为173
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环。
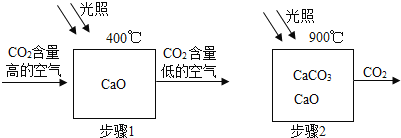
①步骤2的化学方程式为__________。
②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量_______溶液,若观察到试管内_______,则分解不完全。
③上述设想的优点有_______(填字母序号)。
A原料易得且可循环利用B充分利用太阳能C可全地域全天候使用
④CO2是宝贵的碳氧资源。CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2反应的化学方程式为_______,若要测定1%甲酸水溶液酸碱度,选用_______(填字母序号)测定。
A无色酚酞溶液 B紫色石蕊溶液 CpH试纸
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究人员按下图所示流程进行“燃煤烟气的脱硫研究”。实验中,先一次性分别在相应装置中加入水和铁,然后连续通入含有CO2、SO2的燃煤烟气和O2混合气体,反应液多次循环,但过量的铁仍在反应装置中与循环进入的反应液不断反应。经过多次循环后,导出的反应液可用于制备FeSO42H2O。

(1)吸收装置中总反应的化学方程式为2SO2+2H2O+O2=2X,则X的化学式为________
(2)反应装置中的反应化学方程式为________。
(3)经过多次循环以后导出溶液:经_______(填操作名称)、降温结晶、过滤,得到硫酸亚铁晶体。在过滤操作中常用到的玻璃仪器有玻璃棒、烧杯、_______,其中玻璃棒的用途是_______,经过两次过滤后滤液仍浑浊,可能原因是_______
A滤纸破了 B滤液低于滤纸边缘 C盛滤液的烧杯不干净
(4)下图为“FeSO4·7H2O脱水干燥曲线图”,据此可确定:得到FeSO4·2H2O,适宜的工艺条件为_______、________(分别指出时间t和温度T)。

查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(CaO2)在生产中具有广泛的应用
(一)过氧化钙的性质与用途
鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_______,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因________。
(二)过氧化钙晶体的制备
(资料)过氧化钙晶体(CaO2·yH2O),常温为白色,能溶于酸,难溶于酒精。制备原理:CaCl2+H2O2+NH3+H2O![]() CaO2·yH2O↓+NH4Cl,装置如下。
CaO2·yH2O↓+NH4Cl,装置如下。

(1)装置A中试管内发生反应的化学方程式为____
(2)B装置的作用是______。
(3)装置C需要控制温度在0℃左右,采用的简单易行的办法是____,控制温度在0℃左右可能的原因主要有:
Ⅰ该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ______。
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是______。
②检验晶体已洗涤干净的试剂为________。
(三)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水)
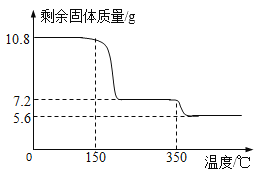
(1)0—150℃质量不发生改变的原因是__________。
(2)根据图可知y = ____。(写出计算过程)
(3)350℃时发生反应的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com