
科目: 来源: 题型:
【题目】钼是一种重要的金属,用它制成的合金有良好的机械性能,在工农业生产和国防上都有广泛的应用,下图是利用钼矿石(主要成分为MoS2)制备金属钼的流程图:(信息:MoO3+3H2![]() Mo+3H2O)
Mo+3H2O)
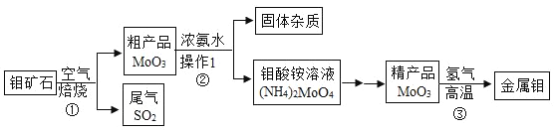
请回答下列问题:
(1)反应①常将钼矿石粉碎,目的是___;MoO3中钼元素的化合价为____。
(2)操作Ⅰ的名称是___;写出反应①的化学方程式____。
(3)制得19.2t金属钼,理论上至少需含MoO380%的粗产品____t?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】小刚在商场发现点燃后怎么也“吹不灭”的蜡烛,他买回来和学习小组同学进行了下列探究。(查阅资料)普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
(请教老师)老师告诉同学们,蜡烛芯内打火石中的某种金属是镁、铁、铜三种金属中的一种。
(进行实验)为确定该金属的成分,大家设计了以下实验方案。(不考虑打火石中的稀土元素对金属性质的探究)。
实验操作步骤 | 实验现象 | 实验结论 |
1.切开蜡烛,取出打火石,用砂纸打磨。 | 打火石呈银白色。 | 该金属一定不是___。 |
2.取少量打磨后的打火石于试管中,滴加____。 | 有无色气体产生,反应后的溶液呈____色。 | 该金属一定不是铁,而是镁。 |
(反思交流)
(1)实验2中反应的化学方程式为____。
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?_____;当吹灭蜡烛时,烛芯中的金属燃烧的化学方程式为_____。
(3)这种“吹不灭”的蜡烛实际上也可以熄灭,你采用的方法是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G是初中化学常见的物质,它们之间的转化关系如图所示。其中A、B、C、D都是氧化物,E、G都是金属单质,且E为应用最广泛的金属,A和G均为红色固体 (其中部分反应条件、反应物及生成物已略去)。请回答下列问题:
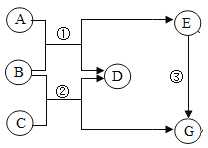
(1)写出下列物质的名称:A___。
(2)写出D物质的一种用途___。
(3)写出反应①的化学方程式___,该反应在工业上用于____。
(4)反应③的方程式为____,属于____反应(填基本反应类型)。
(5)从微观角度解释B和D两种物质化学性质不同的原因____。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)结合如图所示实验装置,回答下列问题。
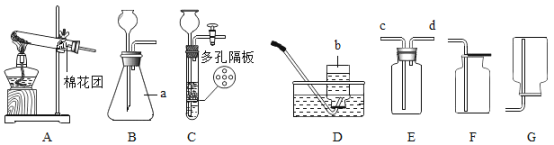
①图中仪器a的名称:____;
②用A、D装置制取并收集氧气,反应方程式为____;装置D收集氧气时,当观察到____时,判断集气瓶中气体已收集满;
③若用B装置制取氧气,反应方程式为___;若用B装置制取二氧化碳,反应方程式为____;
④实验室用装置C制取氢气,与装置B相比,其优点为___,如用E装置收集H2,气体由导管__(填c或d)通入。
(2)结合如图所示实验回答有关问题。
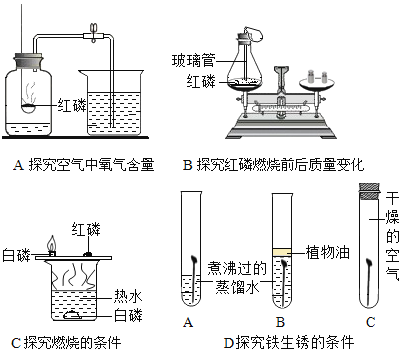
①A实验伸入红磷速度过慢导致进水量___;
②C实验热水作用____(写一点即可);
③B实验气球的作用是____;
④D实验需要用“刚煮沸并迅速冷却的蒸馏水”的原因___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)用化学用语填空
①空气中含量最多的元素___;②缺___可能会导致侏儒症;③构成氯化钠的阴离子___;④地壳中含量最多的金属元素___。
(2)随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。
①在汽车电路中,常用铜做导线,利用了铜的___性;
②车体多用钢材制造。其表面喷漆不仅美观,而且可有效防止与___接触而生锈;
③由铝材制造的零件不易锈蚀的原因是___(用方程式表示);
④生铁和钢的性能不同主要是因为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家利用下图所示循环体系(部分生成物已略去),减缓温室效应。下列结论不正确的是
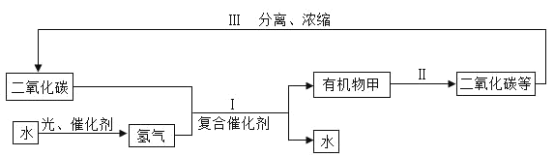
A.有机物甲可能含碳、氢、氧三种元素
B.Ⅰ、Ⅱ、Ⅲ中都消耗了二氧化碳
C.循环过程中需要吸收能量
D.催化剂在反应前后质量和性质都保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像不能正确反映对应的变化关系的是
A.电解水时生成两种气体的质量
B.给氯酸钾和二氧化锰的混合物加热,剩余固体中二氧化锰的质量分数与时间的关系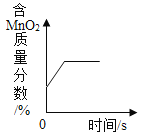
C.用等质量的等质量分数过氧化氢溶液制取氧气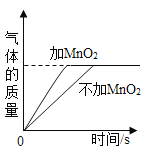
D.向等质量等质量分数足量的稀硫酸中加入等质量的铁和锌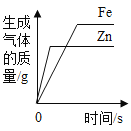
查看答案和解析>>
科目: 来源: 题型:
【题目】(双选)在密闭容器内有一种未知物W、氧气、二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,则下列说法中正确的是( )
物质 | W | 氧气 | 二氧化碳 | 水蒸气 |
反应前质量/ | 46 | 128 | 1 | 0 |
反应后质量/ | 0 | 待测 | 89 | 54 |
A.根据质量守恒定律,待测的值应为30
B.反应后生成二氧化碳和水的分子个数比为![]()
C.物质W只含碳、氢两种元素
D.物质W一定含碳、氢、氧三种元素
查看答案和解析>>
科目: 来源: 题型:
【题目】煤是一种化石燃料,用煤作燃料生成的SO2气体会造成环境污染。有一种煤每燃烧1 t就会释放出53.3 kg SO2。如果将产生的SO2用熟石灰来完全吸收,其反应的化学方程式为:SO2+Ca(OH)2====CaSO3+H2O,那么燃烧5 t这种煤产生的SO2在理论上需用多少千克的Ca(OH)2来吸收?(计算结果取整数)__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com