
科目: 来源: 题型:
【题目】化学与我们的生活密切相关。
(1)用化学用语表示
①氯化钠中的阳离子___;②保持水化学性质的微粒___;③天然气的主要成分____;④标出过氧化氢中氧元素化合价___。
(2)合理利用化学知识,生活更科学、更美好。
①八月桂花飘香,是因为____(用微粒的观点解释),活性炭可以去除冰箱中的异味,说明它具有___性。
②炒菜时若锅中油不慎着火,可以采取的灭火方法是____(写出一种即可)。
③在燃烧的煤炉中洒少量水,火不但不灭,反而燃烧更旺。这是因为在高温条件下,碳与水蒸气反应生成氢气和一种有毒气体,写出该反应的化学方程式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像能正确反映对应变化关系的个数是
①在装有空气的密闭容器中点燃金属镁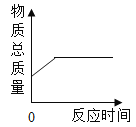
②将等质量的块状和粉末状碳酸钙分别与足量的等质量、等浓度的稀盐酸反应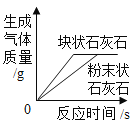
③加热一定质量的高锰酸钾固体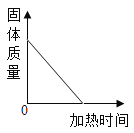
④加热一定质量的氯酸钾和二氧化锰的混合物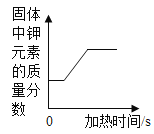
A.1个B.2个C.3个D.4个
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案中,不能达到相应实验目的的是。
A.探究分子在不断运动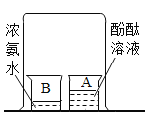
B.探究温度对分子运动快慢的影响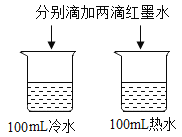
C.探究二氧化锰能否加快过氧化氢的分解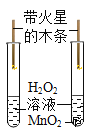
D.验证质量守恒定律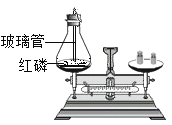
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家最新研制出一种新型石墨烯-铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如右图,有关说法正确的是
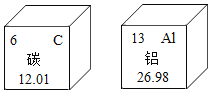
A. 它们的化学性质相同
B. 碳在地壳中含量最高
C. 铝的原子序数为13
D. 铝的相对原子质量为26.98g
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下列实验装置图,回答问题。
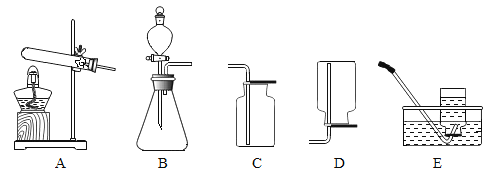
(1)实验室用双氧水和二氧化锰制取氧气的化学方程式为________________,发生装置为________(填字母序号)。若反应过于剧烈,从实验安全角度考虑,可以采取的措施有______________(写一种即可)。
(2)实验室用高锰酸钾制取氧气,为进一步研究高锰酸钾的分解产物,某兴趣小组查阅资料,并取一定质量的高锰酸钾加热使之完全分解,进行下表所示的实验。
(实验内容):
编号 | 实验内容 | 实验现象 | 实验结论 |
1 | 取反应后固体剩余物0.2g加入5mL%的H2O2溶液 | 剧烈反应,放热,产生大量气泡 | 生成物中的MnO2催化分解H2O2 |
2 | 取0. 2g MnO2加入5mL_____(填H2O2溶液的溶质质量分数)的H2O2溶液 | 平稳反应,放热,持续产生气泡 | MnO2催化分解H2O2 |
3 | 取反应后固体剩余物1. 0g,加入足量水,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无_____ |
(实验分析):
①完善上表中的填空内容:实验2________,实验3________。
②实验2的目的是________。
③经讨论,实验1的结论不正确,理由是________。
(资料):在43.9℃~377.9℃范围中,KMnO4受热分解时,会发生以下两个反应:
a.![]()
b.![]()
④取8.0g KMnO4加热使之完全分解,生成O2的质量可能为________(填字母序号);
A0.81 g B1.08 g C1.42 g D1.62 g
⑤资料显示,KMnO4在43.9℃~377 .9℃范围中的失重率(O2与KMnO4的质量比)为18.0%。结合资料分析,在43.9℃~377.9℃范围中,KMnO4分解反应主要以____(填“a”或“b”)为主。
查看答案和解析>>
科目: 来源: 题型:
【题目】盐酸是重要的无机化工产品,广泛用于染料、医药、食品、冶金等行业。
(1)实验室使用的稀盐酸通常都是将浓盐酸用水稀释而成的。现欲用溶质质量分数为37%的浓盐酸(密度为1.189·mL![]() )配制14.6%的稀盐酸100g。步骤为:计算、________、稀释。经过计算可知需要浓盐酸的体积为_______,量取水时应选用规格(从10mL、50mL、100mL中选取)为_______mL的量筒。最后将稀盐酸转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是________(填字母序号)。
)配制14.6%的稀盐酸100g。步骤为:计算、________、稀释。经过计算可知需要浓盐酸的体积为_______,量取水时应选用规格(从10mL、50mL、100mL中选取)为_______mL的量筒。最后将稀盐酸转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是________(填字母序号)。
A100g B14.6% C稀盐酸
(2)该稀盐酸还可用来测定镀锌铁皮锌镀层的质量。将该铁皮与足量稀盐酸反应,待产生的气泡明显减少时取出(此时可认为锌己反应完全,铁还未参与反应),洗涤,烘干,称量,减少的质量即为锌镀层的质量。下列实验操作对测定结果的影响,判断错误的是__________(填字母序号)。
A铁皮未及时取出,会导致测定结果偏小
B铁皮未洗涤干净,会导致测定结果偏大
C烘干时间过长,会导致测定结果偏小
D把稀盐酸换成稀硫酸,会导致测定结果偏大
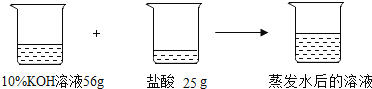
(3)取用上述所配稀盐酸25g与56g溶质质量分数为10%的氢氧化钾溶液相混合(含2滴酚酞试液),混合液刚好由红色变为无色,可认为恰好完全反应。将反应后所得溶液蒸发6.5g水(此过程中无晶体析出),求此时溶液的溶质质量分数。(写出具体计算过程,注意格式)__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化钠是重要的调味品,是舌尖上最不可缺少的味道。下面三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。
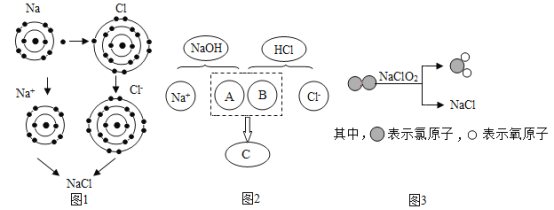
(1)图1是金属钠与氯气反应生成氯化钠的微观示意图,氯化钠由______构成(填微粒符号)。由图1可知,元素的化学性质与原子结构中的______(填字母序号)有密切的关系。
A最外层电子数 B内层电子数 C质子数
(2)图2描述了NaOH溶液与盐酸反应的微观实质,图中A、B、C处应填入的化学符号依次为__________。
(3)图3所示的四种物质中属于氧化物的是________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硝酸钾与氯化钾的溶解度曲线如图所示,请回答下列问题。
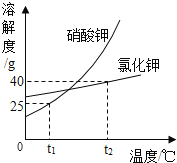
(1)![]() ℃时,两物质中溶解度较大的是________;
℃时,两物质中溶解度较大的是________;
(2)![]() ℃时,两物质的等质量饱和溶液降温至
℃时,两物质的等质量饱和溶液降温至![]() ℃,析出固体质量较大的是__________的溶液;
℃,析出固体质量较大的是__________的溶液;
(3)![]() ℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的_______(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数________(填“变大”、“不变”或“变小”);
℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的_______(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数________(填“变大”、“不变”或“变小”);
(4)欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与人类生活息息相关。请回答下列问题。
(1)烧水的锅底有一层水垢,可用厨房中的__________将其除去。
(2)氢气作为一种新能源,普遍被人们重视并加以研究。但氢气作为燃料也有它的缺点。请写出一条__________。
(3)生活中常讲的“烧开水”,是指利用__________的方法,获得可以饮用的水,这样既可以降低水的硬度,又可以除去水中的细菌。
(4)要将石油液化气(主要成分C4H10)灶改为天然气(主要成分是CH4)灶,对灶具改进的操作是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列化学方程式,并回答相关问题。
(1)天然气燃烧:__________,该反应__________(填写“放热”或“吸热”)。
(2)稀硫酸除铁锈:__________,溶液由无色变为__________.
(3)少量硫酸铵固体与熟石灰混合研磨:__________;检验该气体可用__________试纸。
(4)将光亮的铁丝插入装有硫酸铜溶液中:________,反应所得溶液的质量________(填“大于”或“等于”或“小于”)反应前溶液的质量。
(5)若不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的水冲洗,然后涂上3%~5%的NaHCO3溶液__________;该反应的基本类型是__________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com