
科目: 来源: 题型:
【题目】化学兴趣小组在鲁老师的指导下进行课外探究实验,他们将剪断的火柴头置于酒精灯灯芯上,点燃酒精灯,意外的发现灯芯上的火柴头居然没烧着!这是什么原因呢?请你随他们一起探究。
【猜想与假设】猜想1:灯芯与焰心交界处温度低于火柴头的着火点。猜想2:灯芯与焰心交界处氧气浓度太低,不支持火柴头的燃烧。猜想3:两者均是影响因素。
【查阅资料】①火柴头主要由KClO3、MnO2、易燃物及粘合剂等组成,用红外线测温仪测得火柴头的着火点约是303.4℃。②火柴头在氧气浓度为12.2%的气体中不能燃烧。

【实验验证1】为了验证猜想1,小明利用高温传感器测定酒精灯灯芯和焰心交界处的温度(如图),得到的数据如下:
测量次数 | 第1次 | 第2次 | 第3次 |
温度/℃ | 236 | 243 | 240 |
(1)小明进行多次测量的目的是___________。
(2)仅由上表可知,灯芯上火柴头未烧着的原因是________________________。
(3)请写出火柴头擦燃过程中发生反应的化学方程式(根据资料提供物质)_______________,联想到火柴燃烧时出现的白烟,小明推测白烟的成分可能是______________。
【实验验证2】为了验证猜想2,小红用注射器抽取酒精灯灯芯和焰心交界处的气体,并利用氧气传感器测量氧气的体积分数,数据如表。
测量次数 | 第1次 | 第2次 | 第3次 | 平均值 |
氧气的浓度/% | 5.93 | 5.29 | 6.53 | 5.92 |
(4)根据实验1、2探究内容,可知猜想______________正确。
(5)小红测出的几组氧气浓度存在差异的原因可能是__________________。
【反思评价】如图是小组同学将火柴头置于装有空气的密闭的容器中燃烧,并用氧气传感器在容器项端测量整个过程容器内氧气浓度变化,那么在_______________(填“A、B、C、D”)点时火柴头熄灭;
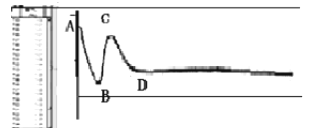
请你根据所学推理并解释曲线A8段、BC段、CD段氧气浓度变化的原因。①_____________________;②______________________;③_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在“质量守恒定律”的课堂教学中,教师引导学生进行“化学反应中,反应物与生成物的质量关系”的实验探究。下图中实验装置和选用药品均为教材图示,现有A、B、C、D四个实验分别由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
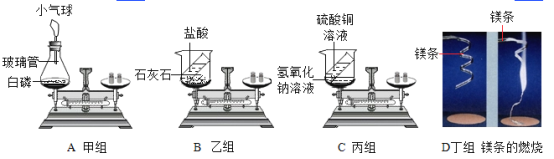
(1)A实验:白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡,结论是质量不守恒.等锥形瓶冷却后,重新放到托盘天平上称量,天平平衡,结论是质量守恒.你认为结论正确的是____(填“前一种”或“后一种”),而导致另一种结论错误的原因是___。
(2)乙、丁两组同学得到的错误结论是“B、D两个实验说明质量不守恒” 。教师引导学生分析了B、D两个实验的原因。你认为要用如图B装置继续探究质量守恒定律,若药品不变改变装置的方法是____;若装置不变,改变药品,可选用的一组药品是____(举一列)。
(3)写出实验C中发生的化学反应_____________________________。
(4)D实验不平衡的原因是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人类的生活和工农业生产都离不开水。如图所示是自来水厂净水过程示意图。
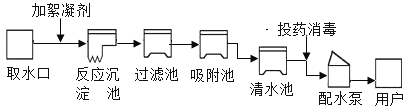
请根据图回答下列问题。
(1)自来水厂生产自来水时,使用的净水方法有_____。
A 沉淀 B 过滤 C 煮沸 D 蒸馏 E 吸附
(2)取水后加入絮凝剂的目的是_____;次氯酸钙也常用作净水剂,化学式为Ca(ClO)2,其中氯元素的化合价为_____。
(3)实验室中过滤用到的玻璃仪器有烧杯、玻璃棒和_____。其中玻璃棒的作用是_____。
(4)请写出电解水的化学反应方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下图回答问题。
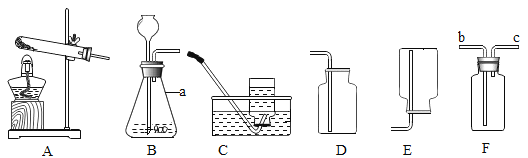
(1)装置图中仪器a的名称:_____。
(2)实验室用氯酸钾和二氧化锰混合加热制取较纯净氧气,可选用的装置组合是_____,反应的化学方程式是_____。
(3)若用装置F采用排空气法收集氢气,氢气从_____(填“b”或“c”)端进入。
(4)B装置中长颈漏斗下端要液封的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学符号或图示表示:
(1)构成氯化钠的微粒是_____和_____;
(2)碳酸钠_____;
(3)氩气_____;
(4)4个硫酸根_____;
(5)铝离子的结构示意图_____;
(6)保持水的化学性质的最小微粒是_____;
(7)镁元素的化合价为+2价_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下甲、乙、丙、丁四种物质在密闭容器中充分反应,测得反应前后各物质的质量如下表中所示。下列说法正确的是
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量(g) | 120 | 90 | 6 | 5 |
反应后质量(g) | 86 | 108 | 22 | a |
A.表中a的值为10B.该反应为分解反应
C.丁一定是催化剂D.反应中乙、丙变化的质量比为15:1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是电解水实验的装置图,下列说法错误的是

A.a 管的电极是负极,b 管的电极是正极
B.在水中加入少量氢氧化钠以增强导电性
C.a 管的气体能被点燃,b 管的气体使燃着的木条燃得更旺
D.反应一段时间后,a、b 玻璃管中产生的气体质量比约为 2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式碳酸盐广泛应用于工农业生产。
(1)某碱式碳酸盐样品M(OH)2·MCO3,为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响)。
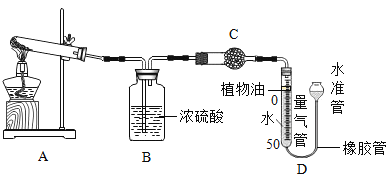
①连接装置并检查装置气密性;
②准确称量样品的质量;
③装药品,调节量气装置两边液面相平,读数;
④加热至样品质量不再减少;
⑤冷却到室温;
⑥________(请将实验步骤补充完整),读数、列式计算。
(2)装置B中的试剂是_________(填字母序号),其作用是________,C中的试剂是________(填字母序号),其作用是________。
a碱石灰 b浓硫酸 c硫酸铜
(3)步骤⑥中调节液面相平的操作是将水准管________(填“缓慢上移”或“缓慢下移”)。
(4)若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是________(填字母序号);
a反应前量气管水面在0刻度处,反应后俯视读数
b样品未分解完全即停止实验
c量气管中水面加一层植物油
(5)实际生产中的碱式碳酸铜可表示为Cu(OH)2·mCuCO3,某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示。
组别 | 样品质量 | CO2体积 |
第1组 | 0.21 g | 22.41 mL |
第2组 | 0.21 g | 22.39 mL |
第3组 | 0.21 g | 22.40 mL |
取3组数据的值得到CO2的体积为_________mL,又知常温常压下CO2的密度为1.964 g/L,据此计算m的值。__________(写出计算m的过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某药片中CaCO3含量,化学兴趣小组设计以下两种方案(药片中其它成分与HCl和NaOH溶液均不反应)。请回答有关问题:
(方案一)利用CO2的体积测定
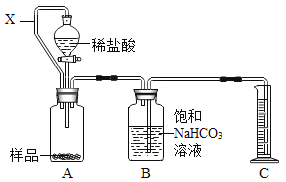
(1)图中仪器名称:①_________;②_________。
(2)装置A中发生的反应方程式是_________,装置B中发生的反应方程式是___________,其目的是___________,装置A中连通管X的作用是_________和_________。
(3)最终测得CaCO3的含量偏低,原因可能是_________。
(方案二)利用酸碱中和滴定法测定
实验步骤:取一粒0.1 g药片研碎,加入适量蒸馏水,再用一定质量、一定质量分数的足量HCl溶液溶解,充分反应后,滴加酚酞作指示剂,再用一定质量分数NaOH溶液中和过量的HCl溶液。
(4)当最后一滴NaOH溶液滴入时,溶液的颜色由_________色变为_______色,且半分钟内不褪去,即完全中和。
(5)进行含量测定除了样品质量外,还需要的数据有_________(填字母序号)。
A滴定所需要的时间 B参加反应的HCl溶液和NaOH溶液的体积
CHCl溶液和NaOH溶液的密度 DHCl溶液和NaOH溶液的质量分数
查看答案和解析>>
科目: 来源: 题型:
【题目】某化工厂为综合利用FeSO4,设计了以下工艺流程:
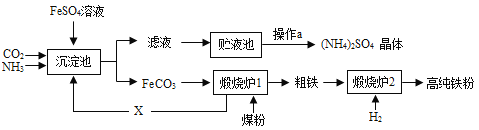
煅烧炉1中发生的部分化学反应有:FeCO3![]() FeO + CO2↑,C +CO2
FeO + CO2↑,C +CO2![]() 2CO
2CO
(1)煤粉、H2既是重要的化工原料又是重要的能源,煤燃烧主要将化学能转化为________能,氢氧燃料电池可以将________能转化为电能。
(2)X气体的化学式是________,循环利用X的优点是_______。
(3)下列金属能从FeSO4溶液中置换出Fe的是_______。
aCu bZn cAg
(4)实验室模拟操作a的过程是蒸发浓缩、________、过滤干燥。
(5)请设计实验证明(NH4)2SO4是铵态氮肥:
实验步骤 | 实验现象 | 实验结论 |
________ | _________ | 样品为铵态氮肥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com