
科目: 来源: 题型:
【题目】化学是一门以实验为基础的科学,想要学好化学一定要重视实验。 下列实验都是基于教材上基础实验的创新,请根据下列所示的实验示意图回答问题。
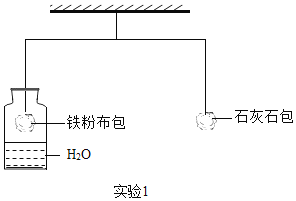
(1)某课外活动中,学生利用实验Ⅰ所示的材料完成探究实验,杠杆已调至平衡。较长时间后,左边铁粉布包下降,将铁粉换成下列物质中的_____ (填序号), 杠杆也会出现相似现象。
A NaCl B NaOH C CaO
(2)三峡博物馆中展出了大量曾侯乙墓青铜器,一件件铜器精美得让人叹为观止。下图是探究铜片生锈条件的实验,会出现明显现象的是试管D,说明铜生锈实际上是铜与_____发生反应(填化学式)。
实验装置 |
A |
B |
C |
D |
实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面 附近锈蚀最严重 |
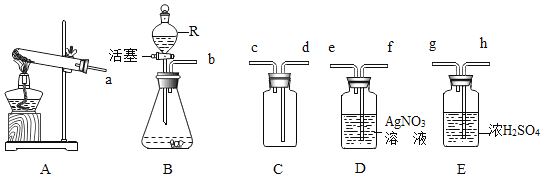
(3)根据下图所给装置回答问题
①如果用装置A制氧气,则所用药品为_____(填化学式)。
②实验室用锌跟稀盐酸反应来制取氢气,其化学方程式为_____。
用这种方法制得的氢气常带有少量的HCl气体和水蒸气。若要制取一瓶纯净干燥的氢气,装置正确的连接顺序是B_____(填C、D和E)。
查看答案和解析>>
科目: 来源: 题型:
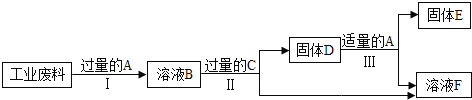
【题目】金属矿物资源有限,所以回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和氯化亚铁溶液,主要流程如下。
已知:![]()
(1)过程Ⅱ、III充分反应后进行的实验操作是_____。
(2)过程I中氧化铜发生反应的化学方程式是_____。
(3)过程III中加入适量A后现象是_____。
(4)溶液B中含有的阳离子有_____。
(5)若最后得到铜32kg,则原工业废料中含氧化铜的质量是_____ kg。
查看答案和解析>>
科目: 来源: 题型:
【题目】酸、碱、盐在生产和生活中有广泛的应用。
(1)如图1是氢氧化钠溶液与硝酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是向_____(填“氢氧化钠溶液”或“硝酸”)中滴加另一种溶液。
②滴入溶液体积为V2ml时,溶液中的溶质为_____。
(2)为除去粗盐水中的可溶性杂质MgSO4、CaCl2,某化学小组设计了如图2方案:
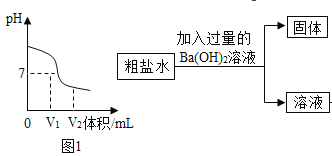
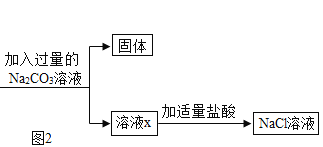
①写出加入Ba(OH)2溶液时反应的化学方程式:_____。
②加入适量盐酸的目的是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】重庆轨道交通环线东北半环于2018年12月28开通试运营,是重庆轨道交通我网中的骨干线路和唯一的闭合环状线路。
(1)下列车厢上使用的物品中,属于合成材料的是_____(填序号)。
A 不锈钢座椅
B 塑料扶手
C 玻璃车窗
D 铝合金车厢
(2)乘坐轻轨、公共汽车等公共交通工具,是践行“低碳生活”的途径之一。“低碳生活”中的“碳”指的是_____(填序号)。
A 碳元素
B 碳单质
C 一氧化碳
D 二氧化碳
(3)车窗玻璃中含有硅元素。如图为硅的原子结构示意图。下列说法正确的是_____ (填序号)。
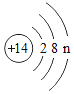
A 硅元素属于金属元素
B n的值为6
C 硅的相对原子质量为14
D 硅的化学性质与碳相似
(4)硅酸(H2SiO3)是一种很弱的酸。玻璃中的氧化硅(SiO2) 与二氧化碳化学性质相似,能与碱溶液反生成硅酸盐和水。请写出二氧化硅与氢氧化钠溶液反应的化学方程式:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像关系合理的是( )
A.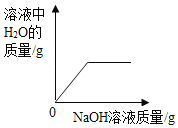 向一定量稀盐酸中加入氢氧化钠溶液
向一定量稀盐酸中加入氢氧化钠溶液
B.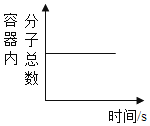 甲烷和足量的氧气在密闭容器中完全反应
甲烷和足量的氧气在密闭容器中完全反应
C.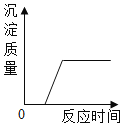 往Na2SO4和HC1的混合溶液中加入Ba(OH)2溶液
往Na2SO4和HC1的混合溶液中加入Ba(OH)2溶液
D.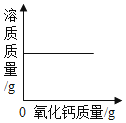 向一定量饱和的石灰水中加氧化钙
向一定量饱和的石灰水中加氧化钙
查看答案和解析>>
科目: 来源: 题型:
【题目】以下关于实验室用燃烧法测定空气中氧气的含量的实验说法正确的是( )
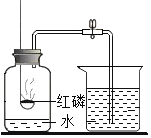
A.历史上通过实验得出空气是由氧气和氮气组成这一重要结论的是阿伏伽德罗
B.实验中的红磷需加过量,这样可以将气体全部消耗完
C.实验中可以用过量的硫代替红磷,但是必须将瓶内预留的水换成氢氧化钠溶液
D.该实验得出空气中氧气质量占空气质量的五分之一
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
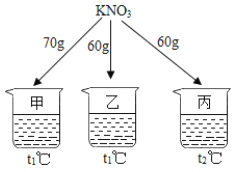
A. 甲、乙混合后为t1℃的不饱和溶液
B. 乙升温至t2℃,溶液质量增加
C. 乙、丙溶液中溶质质量相等
D. 丙降温至t1℃,有晶体析出
查看答案和解析>>
科目: 来源: 题型:
【题目】华裔科学家高锟因提出“以高纯度的石英玻璃制造光纤”,获得2009年诺贝尔奖。从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料。回答问题:
(1)地壳里各种元素的含量(质量分数)如图所示,其中表示Si元素的含量为_____。
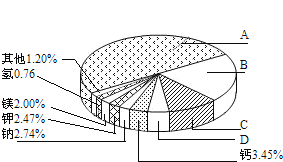
(2)根据元素周期表可知,原子序数为6的碳原子和原子序数为14的硅原子最外层电子数均为4。常温下,硅的化学性质______(填“活泼”或“不活泼”)。
(3)制备硅半导体材料必须先得到高纯硅,工业上以石英砂(主要成分SiO2)制取高纯度石英玻璃的生产原理如下。请回答:
![]()
![]()
①已知反应①的另一产物是有毒气体,其化学式为____,此副产物的用途是_______。
②已知反应②为化合反应,该反应的化学方程式为________________。
③反应③的化学方程式为SiCl4+O2![]() SiO2+2Cl2,该反应的基本类型为______。
SiO2+2Cl2,该反应的基本类型为______。
④将反应③中的氧气换成氢气,可制得生产计算机芯片的高纯硅,则另一产物的化学式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。用工业氧化锌(含有FeO、CuO杂质)生产纯氧化锌的流程如下:
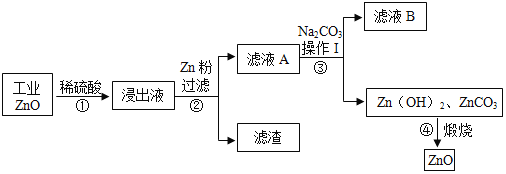
请回答下列问题:
(1)写出浸出液中的阳离子:______;
(2)步骤②中发生了两个反应,都属于______(填基本反应类型)。
(3)从除杂原理分析,步骤②中得到的滤渣含有的金属有______种。
(4)步骤③操作I中用到的玻璃容器为_______(填仪器名称)。
(5)已知步骤④中发生分解反应,写出有二氧化碳气体产生的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com