
科目: 来源: 题型:
【题目】实验小组用传感器研究等量水或NaOH溶液分别吸收CO2的效果,实验装置及测定结果如下图所示。下列说法不正确的是
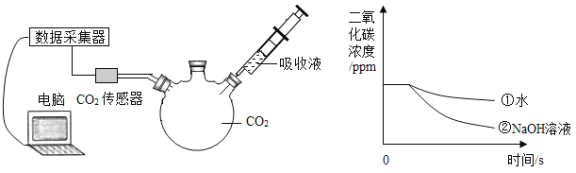
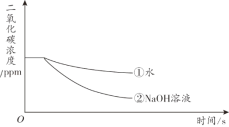
A. 曲线①是CO2溶解和CO2与水反应的综合结果
B. 对比曲线①和②,可说明CO2能与NaOH反应
C. NaOH溶液吸收CO2的效果比水好
D. 若选用等量饱和石灰水进行实验,其曲线在①上方
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,某化学小组在白色点滴板上进行的有关“碱的化学性质“的探究实验。
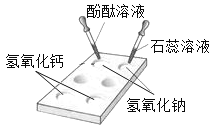
(1)使用白色点滴板进行实验的优点是________________(答一点);
(2)氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞试液变成____色,
是因为在不同碱的溶液中都含有相同的________离子;
(3)写出氢氧化钠与下列物质反应的化学方程式:
①与二氧化碳反应: _______________;
②与硫酸溶液反应: _________________;
③与硫酸铜溶液反应: _________________;
(4)请写出氢氧化钙的一种合理用途为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国约在南北朝时就开始冶铸黄铜,黄铜是铜和锌的合金,可用来制造机器、电器零件及日用品。某探究小组为了测定黄铜样品中铜的质量分数,取黄铜样品20g放入烧杯中,向其中加入100g稀硫酸,恰好完全反应,反应后烧杯中剩余物的总质量为119.8g。则通过计算回答:
(1)反应产生氢气的质量是_____________g;
(2)该黄铜样品中铜的质量分数__________(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国早三千年前的商代就制造出了精美的青铜器。青铜具有良好的铸造性、耐磨性和耐腐蚀性。则回答下列问题:
(1)人类最早进入青铜器时代,继而进入铁器时代,而人类利用铝的历史仅100多年,这个先后顺序跟下列因素有关的是(_______)
A金属的活动性顺序 B金属的导电、导热性
C金属的延展性 D地壳中金属元素的含量
(2)青铜是铜锡合金,明代宋应星所著《天工开物》曾记载下列炼锡方法,相关的化学方程式可表示为:SnO2+2C![]() Sn+2CO↑,则该反应的基本类型为____________。
Sn+2CO↑,则该反应的基本类型为____________。
(3)取青铜样品8.1g,经分析知其中含锡0.9g,则此青铜中铜和锡的质量比为________。
(4)请用化学方法区分青铜和纯铜,写出其中的操作、现象和结论:________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2020年春节前后,我国大面积爆发武汉肺炎疫情。过氧乙酸是一种医疗上常用的广谱高效消毒剂,对公共场所进行消毒时使用过氧乙酸消毒液。过氧乙酸的分子结构如图所示。通过计算回答:
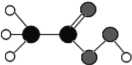
(其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,
代表氢原子,![]() 代表氧原子)
代表氧原子)
(1)过氧乙酸的相对分子质量是____,氧元素的质量分数为_____(精确到0.1%)。
(2)过氧乙酸是一种无色的液体,有辛辣味,具有强氧化性,温度稍高即分解放出氧气,并生成醋酸(C2H4O2)。请写出过氧乙酸分解的化学方程式为___________________,该反应的基本类型为_________。
(3)过氧乙酸能杀灭病毒的主要原理是具有强氧化性,让病毒表面的蛋白质外壳变质,致使病毒死亡。强氧化性属于______(填“物理”或“化学”)性质。
(4)溶质质量分数为0.5%的过氧乙酸溶液常用于空气和地面消毒。某小区要配制0.5%的过氧乙酸消毒溶液200kg,需要10%的过氧乙酸溶液_____kg,加水_____kg。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示装置,向试管里的水中加入某种物质后,U型管中红墨水出现下列三种情形,请填入适当物质:
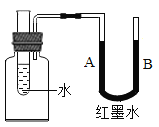
(1)若U型管中液面A降低B升高,则加入的物质可能是_____(填物质名称或俗称);
(2)若U型管中液面A升高B降低,则加入的物质可能是_____(填物质的化学式),该物质中氮元素的化合价有______。
查看答案和解析>>
科目: 来源: 题型:
【题目】若用如图所示密闭装置进行实验,使固体与液体接触,能够观察到气球先膨胀,过一段时间又恢复到原状的一组固体和液体是( )
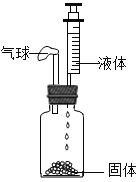
A.固体为硝酸铵;液体为水B.固体为铁粉;液体为稀硫酸
C.固体为氯化钠;液体为水D.固体为生石灰;液体为水
查看答案和解析>>
科目: 来源: 题型:
【题目】防治空气污染、改善生态环境已成为全民共识。
近年来,一些城市空气中出现可吸入悬浮颗粒物与雾形成“雾霾”天气。粒径不大于2.5um的可吸入悬浮颗粒物(PM2.5)富含大量有毒、有害物质。
(1)下列行为可能会导致“雾霾”加重的是_____(填字母序号)。
a.燃煤脱硫 b.植树造林
c.静电除尘 d.燃放鞭炮
(2)为了减少雾霾、降低大气中有害气体含量,研究机动车尾气中CO、NO2及CxHy的排放意义重大。机动车尾气污染物的含量与“空/燃比”(空气与燃油气的体积比)的变化关系如图所示。

①利用氨气可将汽车尾气中的氮氧化物(NOx)在一定条件下转化为对空气无污染的物质。请将该反应的化学方程式补充完整: _____。
_____。
②随“空/燃比”增大,CO和CxHy的含量减少的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水晒盐得到的粗盐除去杂质后,除可做调料,还可以作为工业原料。某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的方程式为:2NaCl + 2H2O![]() 2NaOH + Cl2↑ + H2↑),这种工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。某兴趣小组同学对存放的该厂生产的烧碱样品产生兴趣,对该样品的成分进行了如下探究:
2NaOH + Cl2↑ + H2↑),这种工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。某兴趣小组同学对存放的该厂生产的烧碱样品产生兴趣,对该样品的成分进行了如下探究:
(提出问题)该烧碱样品中可能含有哪些杂质?
(猜想)甲同学:可能含有NaCl
乙同学:可能含有Na2CO3,乙同学猜想的依据是_________________。
(实验探究)为探究该烧碱样品的成分及样品的纯度(氢氧化钠在样品中所占的质量分数),甲、乙两同学通过思考分别设计了如下实验:
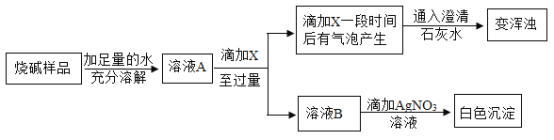
甲同学设计如下方案对烧碱样品的组成进行探究,请回答:
(1)试剂X应选用_________(填化学式)才能依据相应的现象得出正确结论。
乙同学设计了如下方案测定该烧碱样品的纯度:
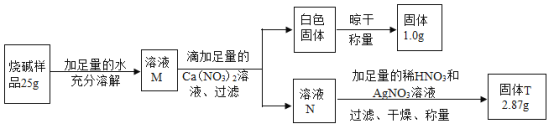
(2)滴加足量Ca(NO3)2的目的是__________________。
(3)请利用乙同学的实验数据,计算该样品中碳酸钠的质量,写出计算过程______________。
(4)该烧碱样品中氢氧化钠的质量分数为_____。(不写计算过程,结果精确到0.1%)
(5)实验结束后,两同学发现测得的该烧碱样品纯度低于工厂样品纯度,请从实验操作的角度分析,原因可能是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com