
【题目】汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3![]() K2O+5Na2O+16N2↑。下列说法正确的是
K2O+5Na2O+16N2↑。下列说法正确的是
A.KNO3是还原剂,其中氮元素被氧化
B.生成物中的N2是氧化产物,K2O是还原产物
C.每转移1 mol 电子,可生成标准状况下N2的体积为35.84 L
D.若有65 g NaN3参加反应,则被氧化的N的物质的量为3.2 mol
科目:高中地理 来源: 题型:
【题目】A、B两种有机物的分子式相同,都可用CaHbOcNd表示,且a+c=b,a-c=d。已知A是天然蛋白质水解的最终产物;B是一种含有醛基的硝酸酯。试回答:
(1)A和B的分子式是________________。
(2)光谱测定显示,A的分子结构中不存在甲基,则A的结构简式为_______________________。
(3)光谱测定显示,B的烃基中没有支链,则B的结构简式为_____________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目: 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为 L。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、![]() 、
、![]() 、
、![]() 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气
体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有 ,可能存在的离子有 ;
(2)原溶液中c(![]() )为 ,c(
)为 ,c(![]() ) c(
) c(![]() ) (填“>、<或=”);
) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl) c(![]() ) (填“>、<或=”)。
) (填“>、<或=”)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】常温下有浓度均为0.5 mol/L的四种溶液:
①Na2CO3、②NaHCO3、③HCl、④NH3·H2O
(1)上述溶液中,可发生水解的是_________(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为:_____________________________________。
(3)向④中加入少量氯化铵固体,此时c(![]() )/c(OH-)的值________(填“增大”“减小”或“不变”)。
)/c(OH-)的值________(填“增大”“减小”或“不变”)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是____________________________________。
(5)取10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=_______________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】[2016上海](1)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填编号)
a.[H+]>[HC2O4-]>[![]() ]>[
]>[![]() ]
]
b.[![]() ]>[HC2O4-]>[C2O42-]>[
]>[HC2O4-]>[C2O42-]>[![]() ]
]
c.[H+]>[HC2O4-]>[C2O42-]>[![]() ]
]
d.[H2CO3] >[![]() ]>[HC2O4-]>[
]>[HC2O4-]>[![]() ]
]
(2)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3-![]() H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
____________________________________________________________________________________
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某同学以清水、缓冲液(含Na2HPO4、KH2PO4的溶液,pH=7)和血浆分别为实验材料进行实验,探究“血浆是否具有维持pH稳定的功能”,主要实验步骤如下:
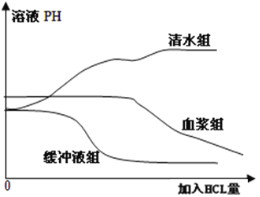
分别加入25mL实验材料 →测pH →滴加5 mL 0.1mol/L的HCl、摇匀 →测pH →倒去烧杯中溶液后充分冲洗 →重复实验并记录。试回答下列有关问题:
(1)实验开始时都应测量三种材料的pH,其目的是 。
(2)该同学用如图所示曲线来预期探究结果,试回答:①预期结果中明显不符合科学的
是 组,理由是 。
②实验中清水组和缓冲液组起 作用。实验可以得出的结论是
(3)如果要证明血浆确实具有维持pH稳定的功能,本探究实验还应该补充 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
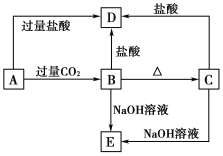
请回答下列问题:
(1)写出化学式:A__________,B__________,C__________,D______,E________。
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com