
����Ŀ��ij��Һ�п��ܺ�������6�������е�ij���֣�Cl��![]() ��
��![]() ��
��![]() ��K+��Na+��Ϊȷ����Һ��ɽ�������ʵ�飺
��K+��Na+��Ϊȷ����Һ��ɽ�������ʵ�飺
��200 mL������Һ����������BaCl2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó���4.30 g��������м�����������ᣬ��2.33 g�������ܡ�
����������Һ�м���������NaOH��Һ�����ȣ������ܴ�ʹʪ���ɫʯ����ֽ��������
��1.12 L(�ѻ���ɱ�״�����ٶ�����������ȫ���ݳ�)��
(1)��Һһ�����ڵ������� �����ܴ��ڵ������� ��
(2)ԭ��Һ��c(![]() )Ϊ ��c(
)Ϊ ��c(![]() ) c(
) c(![]() ) (���������=��)��
) (���������=��)��
(3)�������6�����Ӷ����ڣ���c(Cl) c(![]() ) (���������=��)��
) (���������=��)��
���𰸡�(1)![]() ��
��![]() ��
��![]() (2��) Cl��K+��Na+ (2��)
(2��) Cl��K+��Na+ (2��)
(2)0.05 mol/L(2��) ��(1��)
(3)��(2��)
����������ȡ��������Һ����BaCl2��Һ�а�ɫ�������ɣ��ټ�������������������ܽ⣬�����������ɣ�˵����ɫ����ΪBaCO3��BaSO4������һ����4.3 g������Һ�к���![]() ��
��![]() ��������м�����������ᣬ��2.33 g�������ܣ������ᱵ��������2.33 g��������������ӵ����ʵ�����
��������м�����������ᣬ��2.33 g�������ܣ������ᱵ��������2.33 g��������������ӵ����ʵ�����![]() =0.01 mol������̼�ᱵ��������4.3 g2.33 g=1.97 g��
=0.01 mol������̼�ᱵ��������4.3 g2.33 g=1.97 g��![]() �����ʵ�����
�����ʵ�����![]() =0.01 mol������������Һ�м���������NaOH��Һ�����ȣ�������ʹʪ���ɫʯ����ֽ�����������ǰ��������ʵ�����
=0.01 mol������������Һ�м���������NaOH��Һ�����ȣ�������ʹʪ���ɫʯ����ֽ�����������ǰ��������ʵ�����![]() =0.05 mol��˵����Һ����
=0.05 mol��˵����Һ����![]() �����ʵ�����0.05 mol���ۺ����Ϸ�����
�����ʵ�����0.05 mol���ۺ����Ϸ�����
(1)��Һһ�����ڵ������У�![]() ��
��![]() ��
��![]() �����ܴ��ڵ������У�Cl��K+��Na+��
�����ܴ��ڵ������У�Cl��K+��Na+��
(2)���ݼ���ó�c(![]() )=
)=![]() =0.05 mol/L��
=0.05 mol/L��![]() Ϊ0.01 mol��
Ϊ0.01 mol��![]() Ϊ0.05 mol����c(
Ϊ0.05 mol����c(![]() )��c(
)��c(![]() )��
)��
(3)������Һ������ԭ���趼���ڣ���ô0.05 mol+n(Na+)+n(K+)=2��0.01 mol+2��0.01 mol+n(Cl)���ݴ˵ó�n(Cl)=n(Na+)+n(K+)+0.01 mol��0.01 mol��


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ��ijҺ̬���ķ���ʽΪCmHn����Է�������ΪH2��39����������ʹ����KMnO4��Һ��ɫ������ͬ������Ȼ�̼��Һ��Ӧ��ʹ����ɫ���ڴ�������ʱ��7.8 g ��������0.3 mol H2�����ӳɷ�Ӧ������Ӧ�ı�����CmHp����
(1)m��n��p��ֵ�ֱ���m��________��n��________��p��________��
(2)CmHp�Ľṹ��ʽ�ǣ�________��
(3)CmHn�ܺ�Ũ���ᡢŨ����Ļ���ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽ��________________���÷�Ӧ����__________��Ӧ���л������������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ��ָ������ԭ�ӵ��ӻ�������ͼ����ӵĽṹʽ�����幹�͡�
(1)CS2�����е�Cԭ�Ӳ�ȡ �ӻ�,���ӵĽṹʽΪ ,���幹��Ϊ ;
(2)CH2O�е�Cԭ�Ӳ�ȡ �ӻ�,���ӵĽṹʽΪ ,���幹��Ϊ ;
(3)CCl4�����е�Cԭ�Ӳ�ȡ �ӻ�,���ӵĽṹʽΪ ,���幹��Ϊ ;
(4)H2S�����е�Sԭ�Ӳ�ȡ �ӻ�,���ӵĽṹʽΪ ,���幹��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ��(1)��������ԭ�ĽǶȷ���ˮ�����л�ѧ��Ӧ�е�����(������������ԭ���Ƕȷ���)��
�����ˮ��_____________________________________________________��
���ƺ�ˮ�ķ�Ӧ(2Na+2H2O![]() 2NaOH+H2��)��_______________________________��
2NaOH+H2��)��_______________________________��
��������ˮ��Ӧ(2F2+2H2O![]() 4HF+O2)��_______________________________��
4HF+O2)��_______________________________��
��������ˮ��Ӧ(Cl2+H2O![]() HCl+HClO)��______________________________��
HCl+HClO)��______________________________��
(2)ijһ��Ӧ��ϵ���з�Ӧ��������ﹲ5�����ʣ�S��H2S��HNO3��NO��H2O���÷�Ӧ��ϵ�л�ԭ������________������Ӧ��ת����0.3 mol���ӣ������������������________g��
(3)������Cl2ͨ��FeBr2����Һ�У���Ӧ�����ӷ���ʽΪ2Fe2++Cl2![]() 2Fe3++2Cl�������ʵ˵�����л�ԭ�Ե����ӻ�ԭ��ǿ��˳��Ϊ____________������Cl2ͨ��FeBr2��Һ��������Ӧ�����ӷ���ʽΪ________________��
2Fe3++2Cl�������ʵ˵�����л�ԭ�Ե����ӻ�ԭ��ǿ��˳��Ϊ____________������Cl2ͨ��FeBr2��Һ��������Ӧ�����ӷ���ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ��(1)���ݷ�Ӧ8NH3+3Cl2![]() 6NH4Cl+N2���ش��������⣺
6NH4Cl+N2���ش��������⣺
���÷�Ӧ���������� ������������ ��
���÷�Ӧ�б������������뱻��ԭ���������ʵ���֮��Ϊ ��
(2)ijһ��Ӧ��ϵ�д�������6�����ʣ�NO��FeSO4��Fe(NO3)3��HNO3��Fe2(SO4)3��H2O����֪��������ת����ϵ��HNO3��NO����������и��⣺
���÷�Ӧ���������� ����ԭ���� ��
���÷�Ӧ��1 mol������ (��õ�����ʧȥ��) mol���ӡ�
������0.1 mol HNO3����ԭ����ʱ���ɱ�״����NO������� L��
����Ѹ�������������ո�����ƽ��
��______+��______![]() ��______+��______+��______+��
��______+��______+��______+��
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ���ס��ҡ��������ֱ���Na2CO3��Һ��AgNO3��Һ��BaCl2��Һ������������ɫ��Һ�е�һ�֣��ֽ�������ͼ1��ʾ��ʵ�顣
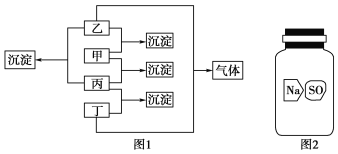
(1)ͨ������ʵ���жϳ������ʣ���________����________����________����________��д�������ҷ�Ӧ�����ӷ���ʽ______________________��
(2)ʵ������һƿ��ǩ����(��ͼ2��ʾ)�Ĺ����Լ���ijͬѧӦ��(1)�е�BaCl2��Һ���飬ȡ�Լ�ƿ�еĹ����������Թ��У�����������ˮ�ܽ⣬��������Һ�м������BaCl2��Һ���õ���ɫ�������ɴˣ���ͬѧ�ƶ���ƿ�Լ��������ơ�����Ϊ���Ľ����Ƿ���ȷ��________������ȷ����д����Ӧ�����ӷ�Ӧ����ʽ��������ȷ����˵�����ܵĽ��ۣ���������һ����֤��ʵ�鷽��(Ҫ�������Լ�ֻ�ܴӼס��ҡ���������ѡ��)��__________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ������������ײʱ����ȫ�����з�����Ӧ��10NaN3+2KNO3![]() K2O+5Na2O+16N2��������˵����ȷ����
K2O+5Na2O+16N2��������˵����ȷ����
A��KNO3�ǻ�ԭ�������е�Ԫ�ر�����
B���������е�N2���������K2O�ǻ�ԭ����
C��ÿת��1 mol ���ӣ������ɱ�״����N2�����Ϊ35.84 L
D������65 g NaN3�μӷ�Ӧ����������N�����ʵ���Ϊ3.2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ�������ӹ���ķ�����Һ�к���2%~5%��NaNO2������һ�ֻ�����Ⱦ�������NH4Cl��Һ�������˷�����Һ��ʹ��������ת��Ϊ�����ʡ��÷�Ӧ���������У�
��һ����NaNO2+NH4Cl===NaCl+NH4NO2
�ڶ�����NH4NO2![]() N2��+2H2O
N2��+2H2O
���жԵڶ�����Ӧ����������ȷ����
��NH4NO2����������
��NH4NO2���ǻ�ԭ��
��NH4NO2�����˷ֽⷴӦ
��ֻ�е�Ԫ�صĻ��ϼ۷����˱仯
��NH4NO2�������������ǻ�ԭ��
A���٢ܢ� B���ڢۢ� C���٢ۢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����е��� ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У����ǻ��Ϸ�Ӧ����������ԭ��Ӧ����
A�������������������������2SO2+O2![]() 2SO3
2SO3
B������ͨ���廯����Һ�У�Cl2+2NaBr![]() 2NaCl+Br2
2NaCl+Br2
C��ϡ��������������Һ��Ϸ�Ӧ��HCl+AgNO3![]() AgCl��+HNO3
AgCl��+HNO3
D�������Ƹ�ˮ��Ӧ��Na2O+H2O![]() 2NaOH
2NaOH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com