
【题目】The secretary arranged a(n)___time and place for the applicants to have an interview
A.important
B.spare
C.public
D.convenient
科目:高中地理 来源: 题型:
【题目】浙江卫视超人气综艺节目《奔跑吧,兄弟》12月5日来到甘肃月牙泉(周围为沙丘)上演大漠公主争夺战。读大气热力作用示意图和月牙泉地区景观图完成下列问题。
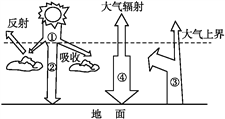

【1】【1】月牙泉附近出现的绿洲体现了( )
A. 纬度地带分异规律 B. 经度地带分异规律
C. 垂直分异规律 D. 地方性分异规律
【2】【2】节目拍摄过程中,队员感觉当地昼夜温差明显较大,其合理的解释是 ( )
A. ②弱、③强 B. ①强、③弱 C. ②强、④强 D. ②强、④弱
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO![]() 被还原为NO)。下列说法正确的是( )
被还原为NO)。下列说法正确的是( )
A.反应后生成NO的体积为28 L
B.所得溶液中c(Fe2+)∶c(Fe3+)=1∶1
C.所得溶液中c(NO![]() )=2.75 mol·L-1
)=2.75 mol·L-1
D.所得溶液中的溶质只有FeSO4
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】已知X、Y、Z、W是短周期界素中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置, 它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)请写出Z在元素周期表中的位置为第 周期、第 族。
(2)气体分子YW2的电子式为 。
(3)由X、Y、Z、W四种元素可组成酸式盐,该化合物的水溶液与足量NaOH溶液在加热条件下反应的离子方程式为 。
(4)在一定条件下,由X单质与单质Z可化合生成E,工业上用E检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质Z生成,写出化学方程式 。该反应中被氧化的E与参与反应的E的质量之比 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】将某溶液逐滴加入Fe(OH)3胶体中,开始产生沉淀,继续滴加时沉淀又溶解,该溶液是
A.2 mol·L1 KOH溶液
B.2 mol·L1 HCl溶液
C.2 mol·L1 Na2SO4溶液
D.FeCl3溶液
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下列物质的分类不正确的是
A.水、过氧化氢和干冰都属于氧化物
B.H2SO4、HNO3、H2CO3都属于酸
C.烧碱、纯碱、熟石灰都属于碱
D.NaHSO4、CuSO4和KMnO4都属于盐
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读下列材料,回答问题。
材料一 2015年1月27日-28日,湖北省江汉平原受较强冷空气南下与暖湿气流交锋影响,出现了“雨凇”的天气。“雨凇”是天空洒下的冷雨,一接触树枝、电缆、屋脊等,便迅速 冻结成晶莹的冰层。下左图为江汉平原附近区域图,下右图为当地此次雨凇形成的气温垂直分布图。
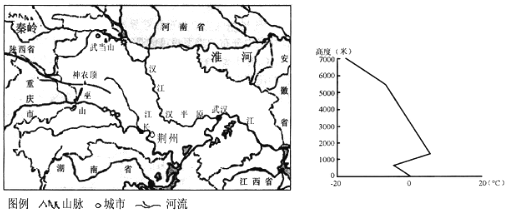
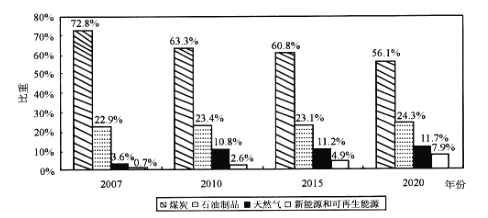
材料二 20世纪50年代,在能源奇缺背景下,周恩来总理提出以秦岭、淮河为界,来划定北方集中供暖区,划定理由是多年日平均气温稳定≤5℃的日数≥90天被界定为集中供暖 的地区。近年来,每逢供暖期,呼吁“南方集中供暖”的话题都会成为热点。据了解,北方墙体砖层厚度一般为37厘米,俗称“三层砖”;南方墙体厚度一般为24厘米,俗称“两层砖” 。下图为2007~2020年我国能源消费结构统计图。
(1)分析江汉平原此次出现“雨凇”天气的原因。
(2)指出2007~2020 年我国能源消费结构的变化特点。
(3)你是否赞同南方集中供暖?请表明态度并说明理由。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是( )
A.①③⑤⑦⑧ B.②④⑦ C.①⑥ D.②④⑥⑧
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】钛白粉(金红石晶型 TiO2)被广泛用于制造高级白色油漆。工业上以钛铁矿(主要成分为 FeTiO3,含有 Fe2O3 和 SiO2 等杂质)为原料制钛白粉的主要工艺如下:
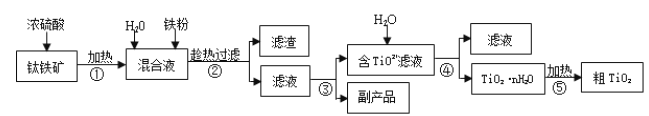
回答下列问题:
(1)第②步所得滤渣的成分是________。
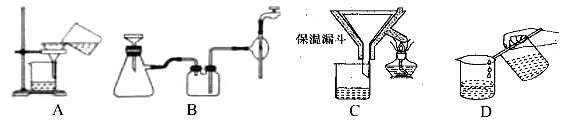
(2)操作④中需要控制条件以形成 TiO2·nH2O 溶胶,该工艺过程若要在实验室里完成,其中的“过滤”操作,可选用下列装置________(填选项)。
(3)第③步的实验操作是______、过滤,从而获得副产品 FeSO4·7H2O。
(4)为测定操作③所得滤液中TiO2+的浓度,取待测滤液10 mL 用蒸馏水稀释至100 mL,加入过量铝粉,充分振荡,使其完全反应:3TiO2+ + Al + 6H+ = 3Ti3+ + Al3+ + 3H2O。过滤后,取出滤液20.00 mL(加铝粉时引起溶液体积的变化忽略不计),向其中滴加2~3 滴KSCN溶液作指示剂,用 0.1000 mol·L-1NH4Fe(SO4)2 标准溶液滴定至溶液出现红色,此时溶液中 Ti3+全部被氧化为 Ti4+,消耗标准液30.00mL。回答下列问题:
①下列操作会使所测 TiO2+浓度偏高的是______。
A. 在配制标准液的过程中,未洗涤烧杯和玻璃棒
B. 在配制标准液定容是俯视刻度线
C.用蒸馏水洗涤后未经润洗的滴定管取待测液
D.在滴定终点读数时仰视滴定管刻度线
②求得待测滤液中 TiO2+的物质的量浓度是______。
(5)科学家从电解冶炼铝的工艺中得到启发,找出了冶炼钛的新工艺—TiO2 直接电解法生产钛,电解质为熔融的氯化钙,原理如图所示。

写出阴极电极反应式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com