
【题目】试用离子方程式和简要文字表述以下事实:
(1)盛纯碱溶液的试剂瓶有玻璃塞,时间久了不易打开________________。
(2)盛NH4F试剂要用塑料瓶而不用玻璃瓶____________________。
(3)铵态氮肥不能与草木灰混用_____________________________。
(4)实验室配制的CuSO4溶液,常常出现浑浊的原因是________________(写出离子方程式),可采取在配制时加入少量________防止浑浊。
(5)某同学想把AlCl3(aq)和Na2S(aq)混合制取Al2S3,但最后得到一种白色絮状沉淀,而且混合液中有臭鸡蛋气味的气体放出。试解释造成此结果的原因,写出反应的离子方程式,并指出制取硫化铝的正确方法________________。
【答案】(1)CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-、SiO2+2OH-===SiO
+OH-、SiO2+2OH-===SiO![]() +H2O,Na2CO3水解生成的NaOH与玻璃的主要成分SiO2反应生成黏性的Na2SiO3,会把瓶塞与瓶口黏在一起
+H2O,Na2CO3水解生成的NaOH与玻璃的主要成分SiO2反应生成黏性的Na2SiO3,会把瓶塞与瓶口黏在一起
(2)NH![]() +F-+H2O
+F-+H2O![]() HF+NH3·H2O,由于F-与NH
HF+NH3·H2O,由于F-与NH![]() 的水解互相促进,生成较高浓度的氢氟酸,使HF与SiO2反应而将玻璃腐蚀4HF+SiO2===SiF4↑+2H2O。
的水解互相促进,生成较高浓度的氢氟酸,使HF与SiO2反应而将玻璃腐蚀4HF+SiO2===SiF4↑+2H2O。
(3)CO![]() +H2O===HCO
+H2O===HCO![]() +OH-、NH
+OH-、NH![]() +H2O
+H2O![]() NH3·H2O+H+、H++OH-===H2O,草木灰的主要成分K2CO3与铵态氮肥中的NH
NH3·H2O+H+、H++OH-===H2O,草木灰的主要成分K2CO3与铵态氮肥中的NH![]() 水解相互促进,生成NH3·H2O分解而挥发,降低了氮肥的肥效。
水解相互促进,生成NH3·H2O分解而挥发,降低了氮肥的肥效。
(4)Cu2++2H2O![]() Cu(OH)2+2H+ H2SO4
Cu(OH)2+2H+ H2SO4
(5)因为S2-和Al3+水解相互促进,使反应较彻底2Al3++3S2-+6H2O===2Al(OH)3↓+3H2S↑,因生成H2S逸出,闻到臭鸡蛋气味。用硫粉与铝粉的混合物在干态时共热制Al2S3,2Al+3S![]() Al2S3
Al2S3
【解析】(1)碳酸根离子水解显碱性,能和玻璃的主要成分二氧化硅反应生成黏合剂硅酸钠你。(2)氟化铵水解产生的氢氟酸和玻璃中的二氧化硅反应,故不能用玻璃容器盛放。(3)氨态氮肥水解显酸性,草木灰水解显碱性,两者相互反应,肥效减弱。(4)硫酸铜中的铜离子水解生成氢氧化铜沉淀,故溶液显浑浊,加入稀硫酸可以抑制铜离子水解。(5)铝离子和硫离子发生双水解,相互促进,生成氢氧化铝沉淀和硫化氢气体。


科目:高中地理 来源: 题型:
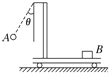
【题目】如图所示,带支架的平板小车沿水平面向左做直线运动,小球A用细线悬挂于支架前端,质量为m的物块B始终相对于小车静止地摆放在右端。B与小车平板间的动摩擦因数为μ。若某时刻观察到细线偏离竖直方向θ角,则此刻小车对物块B产生的作用力的大小和方向为( )
A.mg![]() ,斜向右上方
,斜向右上方
B.mg![]() ,斜向左上方
,斜向左上方
C.mgtan θ,水平向右
D.mg,竖直向上
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】来自质子源的质子(初速度为零),经一加速电压为800kV的直线加速器加速,形成电流强度为1mA的细柱形质子流。已知质子电荷e=1.60×10-19C。这束质子流每秒打到靶上的质子数为 。假定分布在质子源到靶之间的加速电场是均匀的,在质子束与质源相距L和4L的两处,各取一段极短的相等长度的质子流,其中的质子数分别是n1和n2,则![]() = 。
= 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(1)pH=2的某酸稀释100倍,pH________4,pH=12的某碱稀释100倍,pH________10。
(2)室温时,将pH=5的H2SO4溶液稀释10倍,c(H+)∶c(SO42-)=________,将稀释后的溶液再稀释100倍,c(H+)∶c(SO42-)=________。
(3)
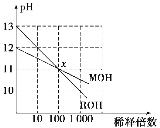
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如上图所示。下列叙述中不正确的是( )
A.MOH是一种弱碱
B.在x点,MOH完全电离
C.在x点,c(M+)=c(R+)
D.稀释前ROH溶液中c(OH-)是MOH溶液中c(OH-)的10倍
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(15分)高速公路上甲、乙两车在同一车道上同向行驶,甲车在前,乙车在后,速度均为v0=30 m/s,相距x0=100 m。t=0时甲车遇紧急情况,之后甲、乙两车的加速度随时间变化的关系分别如图甲、乙所示,以运动方向为正方向。
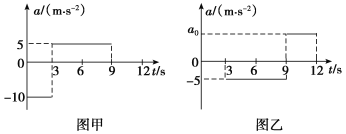
(1)两车在0~9 s内何时相距最近?最近距离是多少?
(2)若要保证t=12 s时乙车在甲车后109 m,则图乙中a0应是多少?
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】“84消毒液”与硫酸溶液反应可以制取氯气,反应方程式为NaClO+NaCl+H2SO4![]() Na2SO4+Cl2↑+
Na2SO4+Cl2↑+
H2O。为探究氯气的性质,某同学设计了如下所示的实验装置。
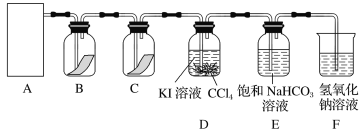
请回答:
(1)在该实验中,制取氯气的装置是________(填字母)。
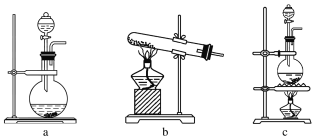
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是________________________________________________,请提出合理的改进方法_______________________________________________。
(3)D中的现象是_____________________,反应的离子方程式为_________________________________,
分离D中液体的方法是___________________________________________。
(4)写出氯气与NaOH溶液反应的离子方程式______________________________,该反应中氧化剂与还原剂的物质的量之比为________。为验证尾气吸收后的溶液中存在Cl,正确的操作是____________________。
(5)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明Cl2与H2O反应的产物中含有________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示;
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO42-、OH- |
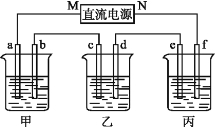

上图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了16 g。常温下各烧杯中溶液的pH与电解时间(t)的关系图如上。据此回答下列问题;
(1)M为电源的 (填“正”或“负”)极,电极b上发生的电极反应为 。
(2)计算电极e上生成的气体在标准状况下的体积 。
(3)写出乙烧杯的电解总反应; 。
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行,为什么?
(5)要使丙恢复到原来的状态,操作是 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】分析下列有机化合物的结构简式,完成下列填空。
①CH3CH2CH2C(CH3)3
②HCOOCH2CH3
③CH3CHClCH2CH3
④CH3CHClCH===CHCH3
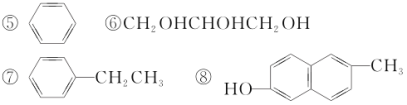
⑨(CH3)2CHCOOH ⑩CH3CHO
对以上有机化合物进行分类,其中:
(1)含有羟基(—OH)的是____________。
(2)含有羟基但不属于醇的是____________。
(3)属于烯烃的是____________。
(4)属于芳香烃的是____________。
(5)属于羧酸的是____________。
(6)属于醛的是____________。
(7)属于卤代烃的是____________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某元素的氯化物化学式为MCl2,现将11.1 g该氯化物溶于水配成溶液后,需用200 mL 1 mol·L-1 AgNO3溶液才能把溶液中氯离子完全沉淀。已知该M原子中有20个中子,则:
(1)计算M的质量数并写出其原子组成符号。
(2)指出M元素在周期表中的位置(周期、族)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com