
【题目】已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4![]() 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________。
(2)As2O3在上述反应中显示出来的性质是____________(填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为___________。
【答案】(1) 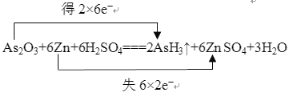
(2)A
(3)ZnSO4 AsH3
(4)1.2NA
【解析】(1)在As2O3+6Zn+6H2SO4![]() 2AsH3↑+6ZnSO4+3H2O中,As的化合价由+3降为3,共得到6×2=12个电子,Zn的化合价由0升高为+2,共失去2×6=12个电子。
2AsH3↑+6ZnSO4+3H2O中,As的化合价由+3降为3,共得到6×2=12个电子,Zn的化合价由0升高为+2,共失去2×6=12个电子。
(2)As2O3中As元素的化合价降低,发生还原反应,作氧化剂,所以表现为氧化性。
(3)该反应中Zn被氧化,氧化产物是ZnSO4,As被还原,还原产物是AsH3。
(4)由双线桥可知,生成2 mol AsH3,转移电子12 mol,若生成0.2 mol AsH3,则转移电子的物质的量是1.2 mol,电子数是1.2NA。


科目:高中地理 来源: 题型:
【题目】利用实验室常用的物品,根据电化学原理,可以设计原电池。请填写下列空白:
(1)实验原理:Fe+2H+= 。
(2)实验用品:电极( 、 )(填所用电极的名称)、稀硫酸、烧杯、导线、耳机(或电流计)。
(3)实验装置如图所示。
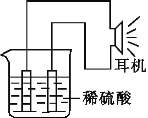
(4)原电池工作原理分析:
该原电池工作时,负极为 (填化学式),发生 (填“氧化”或“还原”),其电极反应式为 ,另一电极为正极,发生 反应,其电极反应式为 ,外电路中电子流动方向为 。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、![]() 、
、![]() 、
、![]() 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气
体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有 ,可能存在的离子有 ;
(2)原溶液中c(![]() )为 ,c(
)为 ,c(![]() ) c(
) c(![]() ) (填“>、<或=”);
) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl) c(![]() ) (填“>、<或=”)。
) (填“>、<或=”)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】HIO4主要以H5IO6形式存在,H5IO6是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
__________Mn2++________H5IO6![]() __________
__________![]() +________
+________![]() +________H++________
+________H++________
(2)根据以上离子方程式判断H5IO6是________电离物质(填“易”或“难”)。
(3)上述反应,被氧化的元素是________(填元素符号),当1 mol Mn2+参加反应时,转移电子的物质的量为________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某离子晶体晶胞结构如图所示,(![]() )X位于立方体的顶点,(○)Y位于立方体的中心,试分析:
)X位于立方体的顶点,(○)Y位于立方体的中心,试分析:
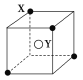
(1)晶体中每个Y同时吸引着________个X,每个X同时吸引着________个Y,该晶体的化学式为________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有________个。
(3)晶体中距离最近的2个X与一个Y形成的夹角∠XYX=________(填角的度数)。
(4)若该立方体的棱长为a cm,晶体密度为ρ g·cm-3,NA为阿伏加德罗常数,则该离子化合物的摩尔质量为________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】纯净物可根据其组成和性质进行分类。
(1)如图所示的分类方法属于________(填字母)。
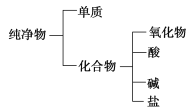
A.交叉分类法 B.树状分类法
(2)以H、O、S、N、K、Ba六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填在下表相应类别中:
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 |
(3)从上表中选出一种酸和一种氧化物,写出其反应的化学方程式:________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】金属加工后的废切削液中含有2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl![]() NaCl+NH4NO2
NaCl+NH4NO2
第二步:NH4NO2![]() N2↑+2H2O
N2↑+2H2O
下列对第二步反应的叙述中正确的是
①NH4NO2仅是氧化剂
②NH4NO2仅是还原剂
③NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A.①③ B.①④
C.②③④ D.③④⑤
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
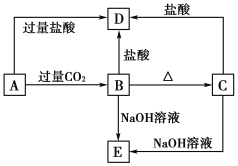
请回答下列问题:
(1)写出化学式:A__________,B__________,C__________,D__________,E__________。
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com