
【题目】烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见图。
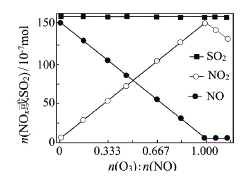
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是__________。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是 _________。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:___________。
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=________[用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是_________。
【答案】(1)-317.3;(2)①O3将NO2氧化成更高价氮氧化物;②SO2与O3的反应速率慢;(3)SO32-+2NO2+2OH-=SO42-+2NO2-+H2O;(4)Ksp(CaSO3)×c(SO42-)/Ksp(CaSO4),CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加快SO32-与NO2的反应速率。
【解析】(1) 前两式变形①+②×2得出:3NO(g)+O3(g)=3NO2(g) △H=-200.9-58.2×2kJ·mol-1=-317.3kJ·mol-1;(2)①n(O3):n(NO)>1,臭氧过量,NO2减少,可能利用O3的强氧化性,把NO2转化成更高价态;②增加n(O3),O3氧化SO2的反应几乎不受影响,可能是此反应速率较慢;(3)pH约为8,说明溶液显碱性,配平氧化剂(产物)、还原剂(产物),根据原子个数守恒和所带电荷数守恒,配平其他,SO32-+2NO2+2OH-=SO42-+2NO2-+H2O;(4)溶液中Ca2+、SO42-、SO32-,Ksp(CaSO4)=c(Ca2+)×c(SO42-),c(Ca2+)=Ksp(CaSO4)/c(SO42-),同理,c(SO32-)=Ksp(CaSO3)/c(Ca2+),推出c(SO32-)=Ksp(CaSO3)×c(SO42-)/Ksp(CaSO4),利用反应向着更难溶方向进行,溶液中c(SO32-)的增加,加快反应速率,故提高NO2的吸收速率。


科目:高中地理 来源: 题型:
【题目】将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是( )
A.①③⑤⑦⑧ B.②④⑦ C.①⑥ D.②④⑥⑧
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】钛白粉(金红石晶型 TiO2)被广泛用于制造高级白色油漆。工业上以钛铁矿(主要成分为 FeTiO3,含有 Fe2O3 和 SiO2 等杂质)为原料制钛白粉的主要工艺如下:
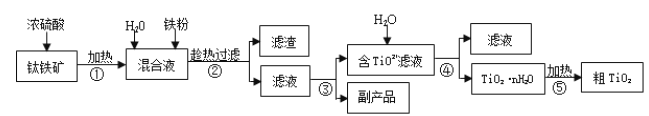
回答下列问题:
(1)第②步所得滤渣的成分是________。
(2)操作④中需要控制条件以形成 TiO2·nH2O 溶胶,该工艺过程若要在实验室里完成,其中的“过滤”操作,可选用下列装置________(填选项)。
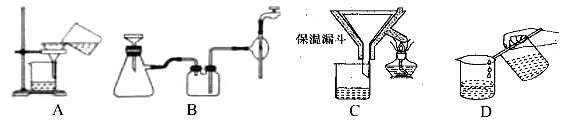
(3)第③步的实验操作是______、过滤,从而获得副产品 FeSO4·7H2O。
(4)为测定操作③所得滤液中TiO2+的浓度,取待测滤液10 mL 用蒸馏水稀释至100 mL,加入过量铝粉,充分振荡,使其完全反应:3TiO2+ + Al + 6H+ = 3Ti3+ + Al3+ + 3H2O。过滤后,取出滤液20.00 mL(加铝粉时引起溶液体积的变化忽略不计),向其中滴加2~3 滴KSCN溶液作指示剂,用 0.1000 mol·L-1NH4Fe(SO4)2 标准溶液滴定至溶液出现红色,此时溶液中 Ti3+全部被氧化为 Ti4+,消耗标准液30.00mL。回答下列问题:
①下列操作会使所测 TiO2+浓度偏高的是______。
A. 在配制标准液的过程中,未洗涤烧杯和玻璃棒
B. 在配制标准液定容是俯视刻度线
C.用蒸馏水洗涤后未经润洗的滴定管取待测液
D.在滴定终点读数时仰视滴定管刻度线
②求得待测滤液中 TiO2+的物质的量浓度是______。
(5)科学家从电解冶炼铝的工艺中得到启发,找出了冶炼钛的新工艺—TiO2 直接电解法生产钛,电解质为熔融的氯化钙,原理如图所示。

写出阴极电极反应式___________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】电解CuSO4溶液时,若要达到以下三点要求:①阳极质量减少;②阴极质量增加;③电解液中c(Cu2+)不变,则可选用的电极是( )
A.含Zn、Ag的铜合金作阳极,纯铜作阴极
B.纯铜作阳极,含Zn、Ag的铜合金作阴极
C.用纯铁作阳极,用纯铜作阴极
D.用石墨作阳极,用惰性电极(Pt)作阴极
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜袋中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是
A.加入BaCl2溶液产生白色沉淀 B.加入碘水不变蓝
C.加入BaCl2溶液没有白色沉淀产生 D.加入碘水变蓝
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】John may phone tonight.I don’t want to go out___he phones
A.as long as
B.in order that
C.in case
D.so that
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读下面两图,完成下列各题。
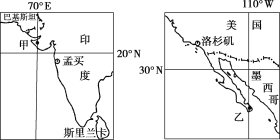
【1】孟买位于洛杉矶的( )
A.西南方 B.东南方 C.东北方 D.西北方
【2】一架飞机由甲地飞往乙地,其最短航线的航向是( )
A.先向正北再向正南
B.先向东北再向东南
C.先向西北再向西南
D.先向东南再向东北
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )

A.在t℃时,AgBr的Ksp为4.9×l0-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br-(aq) ![]() AgBr(s)+Cl- (aq)的平衡常数K≈816
AgBr(s)+Cl- (aq)的平衡常数K≈816
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
资料:氰化钠化学式NaCN(C元素+2价,N元素﹣3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢.
I、(1)NaCN水溶液呈碱性,其原因是____________(用离子方程式解释).
(2)双氧水氧化法除NaCN:碱性条件下加入H2O2,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为____________________________.
(3)非金属性N______C(填“<”、“>”或“=”),请设计实验证明:_____________。
II、某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放.
[实验一]实验室通过如图装置制备Na2S2O3.
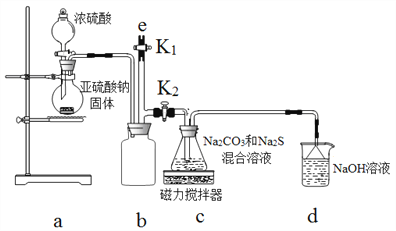
(4)b装置的作用是_______________.
(5)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有__.
(6)实验结束后,在e处最好连接盛__(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1防止拆除装置时污染空气.
[实验二]测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量.
己知:①废水中氰化钠的最高排放标准为0.50mg/L.
②Ag++2CN—=[Ag(CN)2] —,Ag++I—=AgI↓,AgI呈黄色,且CN —优先与Ag+反应.
实验如下.取25.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10﹣4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50mL.
(7)滴定终点的判断方法是_______________.
(8)处理后的废水中氰化钠的含量为_______________mg/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com