
【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是( )
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是( )

A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】
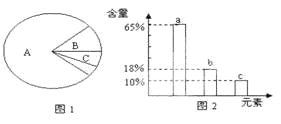
A. 若图1表示正常细胞,则A、B化合物共有的元素中含量最多的是a
B. 若图1表示细胞完全脱水后化合物含量扇形图,则A中含量最多的元素为图2的b
C. 上图2中数量最多的元素是碳元素,这与细胞中含量最多的化合物有关
D. 若图1表示正常细胞,则B化合物具有多样性,其必含的元素为C、H、0、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定不变的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H= —92.4 kJ·mol-1,下列结论正确的是
2NH3(g) △H= —92.4 kJ·mol-1,下列结论正确的是
A.该反应达到平衡时,放出的热量等于92.4kJ
B.达到平衡后向容器中通入1mol氦气,平衡不移动
C.降低温度和缩小容器体积均可使该反应的平衡常数增大
D.若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组研究镉、铜对河蚌过氧化氢酶活性的影响,用一定浓度的镉、铜处理河蚌一段时间后,测得河蚌过氧化氢酶活性如表所示.

请回答下列问题:
(1)表中a应是 .
(2)请列举本实验需要控制的两个无关变量: .
(3)进行过氧化氢酶活性测定时,选过氧化氢为底物,用一定条件下单位时间的 来表示.
(4)若测定镉和铜对河蚌过氧化氢酶活性的综合影响作用,本实验应如何完善? .
(5)若比较过氧化氢酶和Fe3+的催化效率,需利用河蚌的新鲜的软体组织制成研磨液.研磨河蚌软体组织的目的是 .能否用河蚌过氧化氢酶作为实验材料来探究温度对酶活性的影响? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A. 100C时,1L pH=6纯水中含H+数目为10-6NA
B. 0.1mol·L-1 Na2CO3溶液中,Na+的数目为0.2NA
C. 常温常压下,17g羟基(—18OH)所含中子数为9NA
D. 标准状况下,22.4L CHCl3中所含C—Cl键的数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(s)+nB(g)![]() eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是( )
eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是( )

A. 达到平衡后,若使用催化剂,C的体积分数将增大
B. 当平衡后,若温度升高,化学平衡向逆反应方向移动
C. 化学方程式中,n>e+f
D. 达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合所学知识,回答下列有关核酸的问题:

(1)DNA大多是由 条 链构成,RNA通常是由 条 链构成的。
(2)若图为脱氧核苷酸链,则从碱基组成上看,还应有的碱基是 ;图中①是 ,②是 ,③是 ,④是 。
(3)若图为核糖核苷酸链,则从碱基组成上看,还应有的碱基 ;图中②是 ,④是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“HI(s)→HI(g)→H2和I2”的变化过程中,被破坏的作用力依次是( )
A. 范德华力、范德华力 B. 范德华力、共价键
C. 共价键、离子键 D. 共价键、共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com