


分析 酸性条件下硝酸根离子具有氧化性,可氧化海绵铜(主要成分是Cu和少量CuO)生成硫酸铜,过滤后在滤液中加入亚硫酸铵发生氧化还原反应生成CuCl,发生2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+,得到的CuCl经硫酸酸洗,水洗后再用乙醇洗涤,可快速除去固体表面的水分,防止水解、氧化,步骤②、④、⑤、⑧都要进行固液分离,根据混合的水溶性进行分离,没有发生化学变化,可用离心机以及框式压滤机,以得到滤饼,醇洗可快速除去固体表面的水分、防止水解,烘干得到CuCl,以此来解答该题.
解答 解:酸性条件下硝酸根离子具有氧化性,可氧化海绵铜(主要成分是Cu和少量CuO)生成硫酸铜,过滤后在滤液中加入亚硫酸铵发生氧化还原反应生成CuCl,发生2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+,得到的CuCl经硫酸酸洗,水洗后再用乙醇洗涤,烘干得到氯化亚铜.
(1)步骤①中由于酸性条件下硝酸根离子具有氧化性,可氧化Cu生成CuSO4,反应为4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O;溶解温度应控制在60-70℃,原因是温度低溶解速度慢,温度过高铵盐分解,
故答案为:4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O;温度低溶解速度慢,温度过高铵盐分解;
(2)步骤③中铜离子与亚硫酸铵发生氧化还原反应生成CuCl,发生2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+,(NH4)2SO3要适当过量,目的有:保证Cu2+的还原速率,防止CuCl被空气氧化;当氯化铵用量增加到一定程度后氯化亚铜的沉淀率减少,原因是生成的氯化亚铜又溶解于氯化铵溶液中,
故答案为:2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+;防止CuCl被空气氧化;生成的氯化亚铜又溶解于氯化铵溶液中;
(3)步骤⑥为醇洗,因乙醇沸点低,易挥发,则用乙醇洗涤,可快速除去固体表面的水分,防止水解、氧化,
故答案为:醇洗有利于加快去除CuCl表面水,分防止其水解氧化.
点评 本题考查物质的制备实验,为高频考点,侧重于学生的分析能力、实验能力的考查,注意把握物质的性质以及反应流程,题目难度中等,注意习题中信息应用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
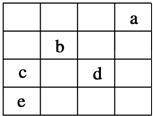 如图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
如图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )| A. | 元素c和d的最高价氧化物对应水化物的酸性:c>d | |
| B. | 五种元素中,元素e的性质最稳定 | |
| C. | 元素b位于ⅥA族,有+6、-2两种常见化合价 | |
| D. | 元素c和e的气态氢化物的稳定性:c>e |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1 的AlCl3溶液中,含Al3+数小于NA | |
| B. | 标准状况下,将2.24L 氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| C. | 1mol NaBH4中含的离子的数目为6NA | |
| D. | 30g甲醛(HCHO)和醋酸的混合物中含碳原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
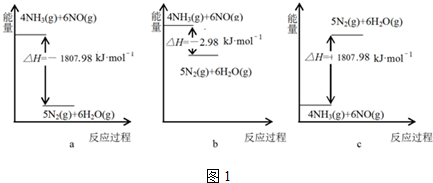
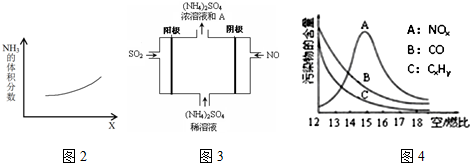
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
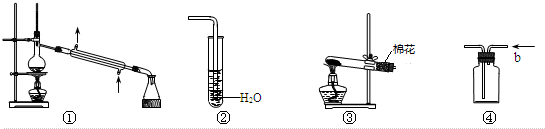
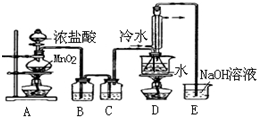
| A. | 装置①可用于除去乙醇中微量的食盐 | |
| B. | 装置②可用于检验CO2气体 | |
| C. | 以KMnO4为原料,装置③可用于实验室制备少量O2的发生装置 | |
| D. | 装置④b口进气可收集H2、N2等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
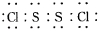 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com