
【题目】2018年4月23日,中国人民海军成立69周年。提到海军就不得不提航空母舰,我国正在建造第三艘航空母舰。镍铬钢抗腐蚀性能强,可用于建造航母。
(1)航母甲板镍铬钢表面涂有一层耐高温的材料聚硅氧烷(结构如图甲所示)。基态Cr原子的价电子排布式为_____________,基态Si原子电子占据最高能级的电子云轮廓图为_____________形,元素C、O、F的电负性由大到小的顺序为_____________。

(2)海洋是元素的摇篮,海水中含有大量F、Cl、Br、I元素。
①OF2的空间构型为_____________,其中O原子杂化方式为_____________杂化。
②KCl晶体中存在的化学键类型有_____________;CaCl2熔点要比KCl的熔点高很多,主要原因为____________________________________________________________________。
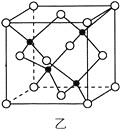
(3)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶胞结构如图乙所示(黑球表示Zn2+,白球表示S2-),Zn2+的配位数为_____________。晶胞边长为a nm、ZnS相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_____________g·cm-3。
【答案】3d54s1 哑铃 F>O>C V形 sp3 离子键 Ca2+半径比K+小,Ca2+所带电荷数比K+多,CaCl2的晶格能更高 4 ![]()
【解析】
(1)依据原子核外电子排布规则写出基态Cr原子的价电子排布式;依据Si的核外电子排布式可知其最高能级为3p能级,3p能级电子云轮廓图为哑铃形;根据C、O、F的非金属性推断其电负性;
(2)①OF2分子的中心原子为O原子,其中含有的孤电子对数为2,σ键数为2,价层电子对数为4,所以OF2的空间构型为V形,其中O原子的杂化方式为sp3杂化;②氯化钾为离子晶体,存在的化学键为离子键;钙离子的半径比钾离子小,钙离子所带电荷数比钾离子多,氯化钙的晶格能更高,所以氯化钙的熔点更高。
(3)通过硫化锌的晶胞结构分析锌离子的周围与之等距离的硫离子,即可知锌离子的配位数;通过硫化锌的晶胞结构可知锌离子的数目为4![]() 1=4,含有硫离子的数目为
1=4,含有硫离子的数目为![]() ,一个晶胞的体积为(a×10-7)3 cm3,由密度公式计算晶体的密度。
,一个晶胞的体积为(a×10-7)3 cm3,由密度公式计算晶体的密度。
(1)Cr为24号元素,核电荷数为24,故基态Cr原子的价电子排布式为3d54s1;Si元素为14号元素,核电荷数为14,核外电子排布式为1s22s22p63s23p2,最高能级为3p能级,3p能级电子云轮廓图为哑铃形;非金属性:F>O>C,则C、O、F的电负性由大到小的顺序为F>O>C。
(2)①OF2分子的中心原子为O原子,其中含有的孤电子对数为2,σ键数为2,价层电子对数为4,所以OF2的空间构型为V形,其中O原子的杂化方式为sp3杂化;②氯化钾为离子晶体,存在的化学键为离子键;钙离子的半径比钾离子小,钙离子所带电荷数比钾离子多,氯化钙的品格能更高,所以氯化钙的熔点更高。
(3)由硫化锌的晶胞结构可知,每个锌离子的周围与之等距离的硫离子有4个,所以锌离子的配位数为4;一个晶胞中含有锌离子的数目为4,含有硫离子的数目为4,一个晶胞的体积为(a×10-7)3 cm3,则晶体的密度为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是日常生活中最常见的金属,其转化关系如图(部分反应物或生成物已略去)。
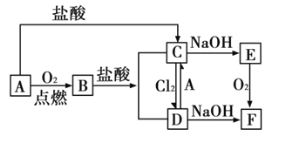
(1)写出![]() 的化学式_____________;溶液
的化学式_____________;溶液![]() 的颜色是______________。
的颜色是______________。
(2)写出下列转化的离子方程式:
①![]() :_________________。
:_________________。
②![]() :__________________。
:__________________。
(3)![]() 转化为
转化为![]() 过程中,可观察到白色沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:________________。
过程中,可观察到白色沉淀迅速变成灰绿色,最后变成红褐色,该反应的化学方程式为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以前实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30—35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。四种盐在不同温度下的溶解度表 (g/100g水)
温度 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | — | — | — | — |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①反应控制在30—35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低 ,为控制此温度范围,通常采取的加热方法为________________;
②加料完毕,保温30分钟,目的_________;
③过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使_________________(填化学式)循环使用,回收得到NH4Cl晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2(g)+B2(g) →2AB(g)的能量变化如图所示,叙述正确的是

A. 该反应是放热反应
B. 加入催化剂,(b-a)的差值减小
C. 每生成2molAB分子吸收bkJ热量
D. 若反应生成AB为液态,吸收的热量小于(a-b)kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,反应2SO2(g)+O2(g)![]() 2SO3(g);△H<0,在不同温度、不同压强(P1>P2) 下达到平衡时,混合气中SO3的体积
2SO3(g);△H<0,在不同温度、不同压强(P1>P2) 下达到平衡时,混合气中SO3的体积![]() (SO3)随温度变化的曲线应为 ( )
(SO3)随温度变化的曲线应为 ( )
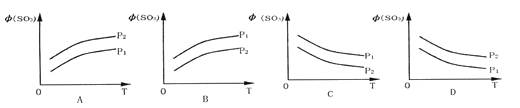
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌被广泛应用于医药领域和工农业生产。工业上由氧化锌矿![]() 主要成分为ZnO,另含
主要成分为ZnO,另含![]() 、
、![]() 、CuO等
、CuO等![]() 生产
生产![]() 的一种流程如图:
的一种流程如图:
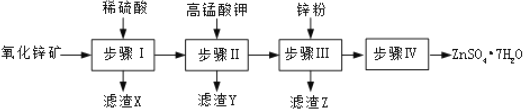
![]() 步骤Ⅰ的操作是______,滤渣A的主要成分是______。
步骤Ⅰ的操作是______,滤渣A的主要成分是______。
![]() 步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是______。
步骤Ⅰ加入稀硫酸进行酸浸时,需不断通入高温水蒸气的目的是______。
![]() 步骤Ⅱ中,在pH约为
步骤Ⅱ中,在pH约为![]() 的滤液中加入高锰酸钾,生成
的滤液中加入高锰酸钾,生成![]() 和
和![]() 两种沉淀,该反应的离子方程式为______。
两种沉淀,该反应的离子方程式为______。
![]() 步骤Ⅲ过滤后所得滤液中含有的金属阳离子有______。
步骤Ⅲ过滤后所得滤液中含有的金属阳离子有______。
![]() 已知硫酸锌的溶解度与温度之间的关系如下表:
已知硫酸锌的溶解度与温度之间的关系如下表:
温度 | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度 |
|
|
|
|
|
|
从硫酸锌溶液中获得硫酸锌晶体的实验操作为______、______、过滤。烘干操作需在减压低温条件下进行,原因是______。
![]() 取
取![]() g
g![]() 加热至不同温度,剩余固体的质最变化如图所示。
加热至不同温度,剩余固体的质最变化如图所示。
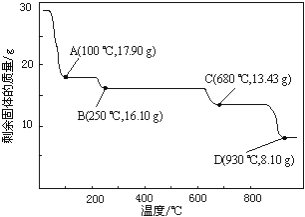
分析数据,![]() 时所得固体的化学式为______。
时所得固体的化学式为______。
![]()
![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物①在一定条件下可以制备②,下列说法错误的是
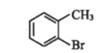 ①→
①→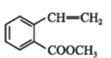 ②
②
A.①不易溶于水
B.①的芳香族同分异构体有3种(不包括①)
C.②在碱性条件下的水解是我们常说的皂化反应
D.②中所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5O-+CO32-
B. 甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-![]() NH4++2Ag↓+3NH3+3H2O+HCOO-
NH4++2Ag↓+3NH3+3H2O+HCOO-
C. 乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2++2OH-![]() Cu2O↓+3H2O+CH3COO-
Cu2O↓+3H2O+CH3COO-
D. 向小苏打溶液中加入醋酸:CO32-+2CH3COOH=CO2↑+H2O+2CH3COO-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com