
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,xA+yB![]() zC的反应达到平衡。
zC的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是__________________;
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向_____________移动;
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不发生移动,则A是_____________态物质。
(4)若加热后C的质量分数减少,则正反应是_________(填“放热”或“吸热”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A和2 mol B放入2 L密闭容器中发生反应:2A(g)+B(g)![]() 2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
A. 4 s内,v(B)=0.075 mol/(L·s)
B. 4 s后平衡状态下,c(A)∶c(C)=2∶1
C. 达到平衡状态时,若只升高温度,则C的物质的量浓度增大
D. 达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,作为信息产业和机电工业的重要基础功能材料,磁性材料广泛应用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要成分为MnO2)和黄铁矿(主要成分为FeS2)为主要原料制备碳酸锰的主要工艺流程如下:

已知:几种金属离子沉淀的pH如下表。
Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
完全沉淀的pH | 9.2 | 3.7 | 7.8 | 10.4 |
回答下列问题:
(1)为了提高溶浸工序中原料的浸出效率,采取的措施不合理的有________。
A.搅拌 B.适当升高温度
C.研磨矿石 D.加入足量的蒸馏水
(2)溶浸过程中主要产生的离子为Fe3+、Mn2+、SO42-,请写出主要反应的离子方程式:___________;浸取后的溶液中含有少量Fe2+、Cu2+、Ca2+,则在加入石灰调节溶液的pH从而使铁元素被完全沉淀前,加入适量的软锰矿目的是______________________,加入石灰调节溶液pH的范围为____________________。
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质,故滤渣主要是________(填化学式)和CaF2。若测得滤液中c(F-)为0.01mol·L-1,则滤液中残留c(Ca2+)为________mol·L-1[已知:Ksp(CaF2)=1.46×10-10]。
(4)有人认为净化工序中使用NaF会引起污染,建议用(NH4)2CO3代替NaF,但是用(NH4)2CO3代替NaF的缺点是______________________________________。
(5)如图为黄铁矿的质量分数对锰浸出率的影响,仅据图中信息,黄铁矿的质量分数应保持在________%左右。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol·L-1FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压数值):

(1)用KSCN溶液检验出Fe3+的现象是_______________________________________。
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应: _____________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有________性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:

①NaCl溶液的浓度是________ mol·L-1。
②Ⅳ中检测Cl2的实验方法:______________________________________________。
③与Ⅱ对比,得出的结论(写出两点):_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生按照课本实验要求,用50 mL 0.5 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是

A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯内填满碎纸条的作用是固定小烧杯
D. 酸或碱的物质的量越大,所测中和热的数值越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有关物质的量浓度的配制下列说法正确的是___
A.称取2.0gNaOH固体:先在托盘各放1张滤纸,然后在右盘加2g砝码,左盘加NaOH固体
B.容量瓶上标有温度和容积使用前要检查是否漏水
C.称取16.0gCuSO4 固体在500mL容量瓶中加水溶解后定容,可配得0.20mol/L的CuSO4溶液
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再慢慢注入浓硫酸
E.配制溶液时,俯视容量瓶刻度线造成浓度偏高
F.溶液转移定容时,溶液未冷却至室温造成浓度偏低
(2)海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(每一步所加试剂均过量):

现有下列仪器,请按要求填写以下空白:
Ⅰ.步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,图中还缺少的玻璃仪器是___。
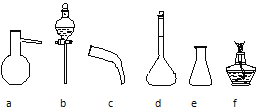
Ⅱ.如何检验步骤③操作后碘化钠滤液中的碘离子___,步骤⑤所需的操作名称是__。
Ⅲ.写出步骤④的化学反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代高科技领域使用的新型陶瓷材料氮化硼(BN),用天然硼砂(Na2B4O710H2O)经过下列过程可以制得。
天然硼砂![]() 硼酸(H3BO3)
硼酸(H3BO3)![]() B2O3
B2O3![]() BN
BN
(1)天然硼砂所含的元素中属于同一周期且原子半径是(用元素符号填写)___>___,由天然硼砂中的三种元素形成的某种离子化合物的电子式为______。
(2)与硼元素性质最相似的元素的原子的最外层电子排布为_______,该原子核外充有电子的轨道共有____个。
(3)试写出天然硼砂与硫酸反应的化学方程式_______,制得的氮化硼有不同的结构,其中超硬、耐磨、耐高温的一种属于____晶体。制取氮化硼的反应必须在密闭的耐高温容器中进行:B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g)+Q(Q<0)
2BN(s)+3H2O(g)+Q(Q<0)
(4)若反应在5L的密闭容器中进行,经2分钟反应炉内固体的质量减少60.0g,则用氨气来表示该反应在2分钟内的平均速率为_____,达到平衡后,增大反应容器体积,在平衡移动过程中,逆反应速率的变化状况为______。
(5)为提高生产效率,使反应速率加快的同时,化学平衡向多出产品的方向移动,可以采取的措施有_________,生产中对尾气的处理方法正确的是(填序号)_____。
A.直接排出参与大气循环 B.冷却分离所得气体可以循环使用
C.全部用来进行循环使用 D.冷却分离所得液体可作化工原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。工业上常以废铁屑(含有SiO2、Al2O3、MgO、Fe2O3等杂质)为原料制备氯化铁。其生产流程如图:

已知:氢氧化物的Ksp下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
Ksp | 1.0×10-36 | 1.6×10-14 | 2.0×10-33 | 1.2×10-11 |
请回答下列问题:
(1)物质X最好选用下列物质中的____(选填序号),加入X的目的是_________。
A.KMnO4 B.FeCl3 C.H2O2 D.HNO3
(2)滤液Ⅰ加入NaOH溶液的目的是调节溶液的pH。已知滤液Ⅰ中c(Fe3+)为1.0mol·L-1,c(Al3+)为0.03mol·L-1,当Fe3+沉淀完全时(c(Fe3+)为1×10-5mol·L-1),Al3+是否已经开始沉淀,请通过计算说明______________。
(3)写出滤渣1加NaOH溶液发应的离子方程式_____________________。
(4)滤渣2中加过量盐酸的目的是_____________________________。
(5)FeCl3具有净水作用,但易腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
①FeCl3净水的原理是________。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________。
②FeCl3在溶液中分三步水解:Fe3++H2O![]() Fe(OH)2++H+ K1,Fe(OH)2++H2O
Fe(OH)2++H+ K1,Fe(OH)2++H2O![]() Fe(OH)2++H+ K2,Fe(OH)2++H2O
Fe(OH)2++H+ K2,Fe(OH)2++H2O![]() Fe(OH)3+H+ K3,以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_______。
Fe(OH)3+H+ K3,以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_______。
③通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为xFe3++yH2O![]() Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)_____。
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)_____。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com