
【题目】氨在国民生产中占有重要的地位。工业合成氨的反应为:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
(1)反应进行到2小时时放出的热量为____________kJ。
(2)此条件下该反应的化学平衡常数K=____________(保留两位小数)。
(3)有两个密闭容器A和B,A容器保持恒容,B容器保持恒压,起始时向容积相等的A、B中分别通入等量的NH3气体,均发生反应:2NH3(g)![]() 3H2(g)+N2(g)。则:
3H2(g)+N2(g)。则:
①达到平衡所需的时间:t(A)_____t(B),平衡时,NH3的转化率:a(A)______a(B) (填“>”、“=”或“<”)。
②达到平衡后,在两容器中分别通入等量的氦气。A中平衡向_________移动,B中平衡向_________移动。(填“向正反应方向”、“向逆反应方向”、“不”)。
(4)在三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数[φ(NH3)]随时间变化的曲线图所示.下列说法中正确的是_____(填字母,下同)。
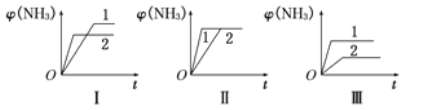
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
【答案】 27.72 0.15 < < 不 向正反应方向 B
【解析】(1). 由方程式N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol可知,每消耗1mol氮气时,反应放出的热量为92.4kJ,当反应进行到2h时,消耗氮气的物质的量为(1.5-1.2)mol=0.3mol,反应放出的热量为0.3mol×92.4kJ/mol=27.72kJ,故答案为:27.72;
2NH3(g) △H=-92.4kJ/mol可知,每消耗1mol氮气时,反应放出的热量为92.4kJ,当反应进行到2h时,消耗氮气的物质的量为(1.5-1.2)mol=0.3mol,反应放出的热量为0.3mol×92.4kJ/mol=27.72kJ,故答案为:27.72;
(2). 由表中数据可知,反应进行到3h和4h时,氨气的物质的量不变,说明3h和4h时均为平衡状态,则此条件下该反应的化学平衡常数K=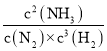 =
=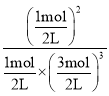 =0.15,故答案为:0.15;
=0.15,故答案为:0.15;
(3). ①. 有两个密闭容器A和B,A容器保持恒容,B容器保持恒压,起始时向容积相等的A、B中分别通入等量的NH3,发生反应2NH3(g)![]() 3H2(g)+N2(g),该反应为气体物质的量增大的可逆反应,A容器保持恒容,反应达到平衡时A容器中压强增大,B容器保持恒压,则A容器与B容器相比,A容器相当于增大压强,A中反应速率快,达到平衡需要的时间短,即达到平衡时所需的时间:t(A)<t(B),对于2NH3(g)
3H2(g)+N2(g),该反应为气体物质的量增大的可逆反应,A容器保持恒容,反应达到平衡时A容器中压强增大,B容器保持恒压,则A容器与B容器相比,A容器相当于增大压强,A中反应速率快,达到平衡需要的时间短,即达到平衡时所需的时间:t(A)<t(B),对于2NH3(g)![]() 3H2(g)+N2(g),增大压强,平衡逆向移动,NH3的转化率减小,即a(A)<a(B),故答案为:<;<;
3H2(g)+N2(g),增大压强,平衡逆向移动,NH3的转化率减小,即a(A)<a(B),故答案为:<;<;
②. 达到平衡后,在两容器中分别通入等量的氦气,A容器保持恒容,则A容器中各物质的浓度不变,平衡不移动,B容器保持恒压,则通入氦气时B容器的体积增大,对于B容器,相当于减小压强,平衡向正反应方向移动,故答案为:不;向正反应方向;
(4). A. 若图Ⅰ表示不同压强对反应的影响,因压强越大,反应速率越快,反应达到平衡所需的时间越短,所以P2>P1,但对于可逆反应N2(g)+3H2(g)![]() 2NH3(g),增大压强,平衡正向移动,NH3的体积分数增大,即压强越大,氨气的体积分数越大,图象与事实不符,故A错误;B. 催化剂可以加快反应速率,使用催化剂1时达到平衡所需的时间更短,说明催化剂1的催化性能比催化剂2要好,催化剂不能使平衡移动,所以使用不同的催化剂时,氨气的体积分数不变,图象与事实相符,故B正确;C. 若图III表示不同温度对反应的影响,因温度越高,反应速率越快,反应达到平衡所需的时间越短,所以T1>T2,但N2(g)+3H2(g)
2NH3(g),增大压强,平衡正向移动,NH3的体积分数增大,即压强越大,氨气的体积分数越大,图象与事实不符,故A错误;B. 催化剂可以加快反应速率,使用催化剂1时达到平衡所需的时间更短,说明催化剂1的催化性能比催化剂2要好,催化剂不能使平衡移动,所以使用不同的催化剂时,氨气的体积分数不变,图象与事实相符,故B正确;C. 若图III表示不同温度对反应的影响,因温度越高,反应速率越快,反应达到平衡所需的时间越短,所以T1>T2,但N2(g)+3H2(g)![]() 2NH3(g)是放热反应,升高温度,平衡逆向移动,氨气的体积分数减小,即温度越高,氨气的体积分数越小,图象与事实不符,故C错误;答案选B。
2NH3(g)是放热反应,升高温度,平衡逆向移动,氨气的体积分数减小,即温度越高,氨气的体积分数越小,图象与事实不符,故C错误;答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。

(1)反应Ⅰ的离子方程式为_____________,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得到AgCl固体1.435g;
③另取25.00mL溶液A,调节pH为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00mL。通过计算确定该样品的化学式为___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。

(1)向苦卤中通入Cl2是为了提取溴,发生反应的离子方程式为________________。
(2)富集溴一般先用空气和水蒸气吹出单质溴,再用SO2的水溶液将其还原吸收,发生反应的化学方程式为______________________。也可用纯碱吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1 mol Br2时,转移的电子为________ mol。
(3)下列有关海水综合利用的说法错误的是____。
A.粗盐可采用除杂和重结晶等过程提纯
B.电解饱和食盐水可制得金属钠
C.工业生产常选用Ca(OH)2作为沉淀剂
D.海水提镁涉及到复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的量热计中,将100mL0.50mol/L CH3COOH溶液与100mL0.55mol/LNaOH溶液混合,温度从25.0℃升高到27.7℃。已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J·℃-1,生成溶液的比热容为4.184J·g-1·℃-1,两溶液的密度均近似为lg/mL.下列说法错误的是
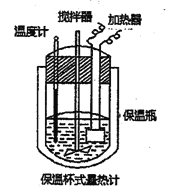
A. 若量热计的保温瓶绝热效果不好,则所测△H偏大
B. 该实验测得反应放出的热量为2665.7J
C. 该实验测得的中和热ΔH为-45.2kJ/mol
D. 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用右图所示装置去含CN-,Cl-废水中的CN-时,控制溶液PH为9-10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 石墨作阳极,铁作阴极
B. 阳极的电极反应式:Cl-+2OH--2e-=ClO-+H2O
C. 阴极的电极反应式:2H2O+2e-=H2↑+2OH-
D. 除去CN-的反应:2 CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可采用NaCl(s)+NaHSO4(s)→Na2SO4+HCl↑制备HCl,下列气体的制备与上述反应装置相同的是
A. 氧气:2H2O2![]() 2H2O+O2↑
2H2O+O2↑
B. 氢气:2Al+6HCl→2AlCl3+3H2↑
C. 氯气:KClO3(s)+6HCl(浓)![]() KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
D. 氧气:2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com