
 CO2������Ҫ�������壬��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�����ش����壮
CO2������Ҫ�������壬��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�����ش����壮 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
| n(H2) |
| n(CO2) |
| ��c |
| ��t |
 CH3OH��g��+H2O��g�����ʴ�Ϊ��CO2��g��+3H2��g��
CH3OH��g��+H2O��g�����ʴ�Ϊ��CO2��g��+3H2��g�� CH3OH��g��+H2O��g����
CH3OH��g��+H2O��g���� CH3OH��g��+H2O��g��
CH3OH��g��+H2O��g��
| ||
| 3min |
 CH3OH+H2O�� 0.25 mol?L-1?min-1��
CH3OH+H2O�� 0.25 mol?L-1?min-1��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ˮ���Ʊ������ɱ�ϩ��ˮ��Ӧ�Ʊ��� |
| B���ɸ��ͺ�Ũ��������������ըҩ���ɼױ���Ũ������TNTըҩ |
| C�����ȴ���������ȥ�ƻ���ϩ���ɱ�ϩ������1��2-������� |
| D�����Ҵ���Ũ���Ṳ�������ѣ����Ҵ���Ũ���Ṳ������ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
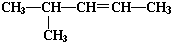
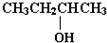
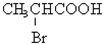
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ�л���A�ķ��ӣ������еĹ����ŵ�������
��ͼ�л���A�ķ��ӣ������еĹ����ŵ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ������ | Ԫ�ر�� | |||||||
| A | B | C | D | E | F | G | H | |
| ԭ�Ӱ뾶��nm�� | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| ����ϼ� | +6 | +4 | +5 | +5 | +4 | +7 | ||
| ��ͻ��ϼ� | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
| A��CΪ��Ԫ�� |
| B��A��B��ͬ����Ԫ�� |
| C��F��H�ļ����ӵĵ��Ӳ�ṹ��ͬ |
| D��Ԫ��G�������е�λ���ǵڶ����ڵڢ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com