
【题目】—氯甲烷是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
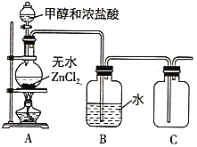
(1)某小组同学在实验室用如图所示装置模拟催化法制备和收集一氯甲烷。
①装置B的主要作用是_____。
②以无水ZnCl2为催化剂,圆底烧瓶中发生反应的化学方程式为____。如果实验时圆底烧瓶加热时间过长,最终在瓶底得到一种白色物质,该物质的化学式是____。
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mLc1mol/LNaOH溶液充分吸收,以甲基橙作指示剂,用c2mol/L盐酸标准液对吸收液进行滴定,最终消耗V2mL盐酸,则所收集CH3Cl的物质的量为_____mol。(已知:2CH3Cl+3O2=2CO2+2H2O+2HCl)
(2)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子。相关数据如下表:
化学键 | C-Cl | C-Br |
键能/(kJ·mol-1) | 330 | 276 |
化合物 | AgCl | AgBr |
Ksp | 1.8×10-10 | 5×10-13 |
①CH3X通入AgNO3的乙醇溶液中,除有沉淀生成外,还生成硝酸甲酯,请写出硝酸甲酯的结构简式:_____。
②设计实验证明HBr是强酸:____(简要说明实验操作、现象和结论)
③CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中的键能和Ksp数据解释原因:____。
【答案】除去HCl气体 CH3OH+HCl![]() CH3Cl+H2O Zn(OH)2(或ZnO) (c1V1-c2V2)×10-3 CH3ONO2 常温下,测0.1mol/L的HBr溶液的pH=1或测NaBr溶液的pH=7等(合理即可) C-Br键的键能小,更容易断裂,同时溴化银的溶度积更小,更容易形成溴化银沉淀
CH3Cl+H2O Zn(OH)2(或ZnO) (c1V1-c2V2)×10-3 CH3ONO2 常温下,测0.1mol/L的HBr溶液的pH=1或测NaBr溶液的pH=7等(合理即可) C-Br键的键能小,更容易断裂,同时溴化银的溶度积更小,更容易形成溴化银沉淀
【解析】
(1)①氯化氢易挥发,所以要用水除去一氯甲烷中的氯化氢;
②甲醇与浓盐酸在氯化铝作催化剂的条件下发生取代反应生成一氯甲烷和水,氯化锌加热时间过长会水解生成氢氧化锌或氧化锌;
③根据题意,一氯甲烷燃烧产生氯化氢,根据与之反应的氢氧化钠的物质的量可求得氯化氢的物质的量,进而确定一氯甲烷的物质的量;
(2)根据题意,CH3X通入AgNO3的乙醇溶液中,能生成硝酸甲酯和AgX;
①根据有机酸酯类比写出硝酸甲酯的结构简式;
②强酸在水中完全电离,据此设计实验;
③根据沉淀的溶解平衡以及键能参数可知,键能小的化学键更易断裂,并且形成沉淀时,优先形成溶度积小的,据此答题。
(1)①氯化氢易挥发,所以要用水除去一氯甲烷中的氯化氢,所以装置B的主要作用是除去氯化氢气体;
②甲醇与浓盐酸在氯化锌作催化剂的条件下发生取代反应生成一氯甲烷和水,反应的化学方程式为CH3OH+HCl![]() CH3Cl+H2O;加热时间过长会导致氯化锌水解生成氢氧化锌或氧化锌沉淀,化学式为Zn(OH)2或ZnO,
CH3Cl+H2O;加热时间过长会导致氯化锌水解生成氢氧化锌或氧化锌沉淀,化学式为Zn(OH)2或ZnO,
③根据题意,与氯化氢反应的氢氧化钠的物质的量为c1V1×10-3mol-c2V2×10-3mol,所以一氯甲烷燃烧产生氯化氢的物质的量为c1V1×10-3mol-c2V2×10-3mol,则一氯甲烷的物质的量为(c1V1-c2V2)×10-3mol;
(2)①硝酸甲酯的结构简式为:CH3ONO2;
②若HBr为强酸,则HBr在水中能够完全电离,并且其形成的强碱盐不会水解,据此可设计实验为:常温下,测0.1mol/L的HBr溶液的pH=1或测NaBr溶液的pH=7等(合理即可);
③依据表中数据可知,C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀,所以先出现淡黄色溴化银沉淀;
故答案为:C-Br键的键能小,更容易断裂,同时溴化银的溶度积更小,更容易形成溴化银。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. Ba(HCO3)2溶液与少量的NaOH溶液反应:Ba2++HCO![]() +OH-=BaCO3↓+H2O
+OH-=BaCO3↓+H2O
B. 次氯酸钙溶液中通入过量的二氧化碳 Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
C. 用氨水吸收少量二氧化硫 OH-+SO2=HSO3-
D. 硫酸与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙炔衍生物分子M的结构简式及M在稀硫酸作用下的水解反应如图所示。下列有关说法不正确的是( )
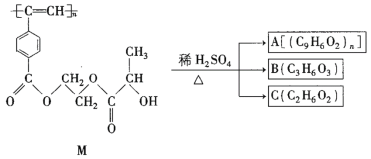
A. M与A均能使酸性高锰酸钾溶液和溴水褪色
B. B中含有羧基和羟基两种官能团,能发生消去反应和酯化反应
C. A、B、C各1mol分别与金属钠反应,放出气体的物质的量之比为1:2:2
D. 1molM与热的烧碱溶液反应,可消耗2nmolNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水资源的利用具有广阔的前景。从海水中提取Br2与MgCl26H2O的流程如图:

(1)海水淡化的方法有蒸馏法、___(任写一种)等,考虑成本及效益试剂①可选用___。
(2)比较溶液中Br2的浓度:溶液2___溶液4(填“>”或“<”)。
(3)鼓入空气与水蒸气将Br2吹出,吹出的气体用SO2吸收,其化学方程式是__。
(4)从MgCl2溶液获得MgCl26H2O晶体的主要操作包括____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓是一种低熔点高沸点的稀有金属,有“电子工业脊梁”的美誉,被广泛应用到光电子工业和微波通信工业;镓(Ga)与铝位于同一主族,金属镓的熔点是29.8℃,沸点是2403℃。
(1)工业上利用Ga(l)与NH3(g)在1000℃高温下合成半导体固体材料氮化镓(GaN),同时生成氢气,每生成lmol H2时放出10.3 kJ热量。写出该反应的热化学方程式__________________。
(2)在密闭容器中,充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。
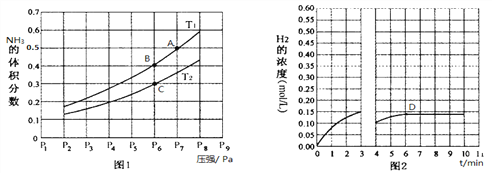
① 图1中A点和C点化学平衡常数的大小关系是:KA_____KC,(填“<”、“=”或“>”),理由是__________________________________________________。
② 该反应在T1和P6条件下至3min时达到平衡,此时改变条件并于D点处重新达到平衡,H2的浓度随反应时间的变化趋势如图2所示(3~4 min的浓度变化未表示出来),则改变的条件为__________(仅改变温度或压强中的一种)。
(3)若用压强平衡常数Kp表示,此时B点对应的Kp=__________(用含P6的式子表示)(Kp为压强平衡常数,用平衡分压代替平衡浓度计算,气体平衡分压=总压×气体体积分数)
(4)电解精炼法提纯镓的具体原理如下:以粗镓(含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH溶液为电解质。在电流作用下使粗镓溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是_________。
②阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,写出GaO2-在阴极放电的电极反应式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84消毒液”是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒,某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用,请回答下列问题:
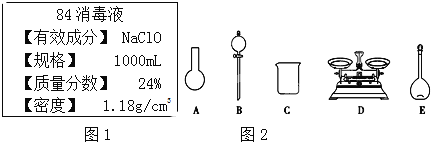
(1)此“84消毒液”的物质的量浓度约为______mol/L(计算结果保留一位小数)。
(2)某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)=___mol/L。
(3)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是______(填仪器序号),还缺少的玻璃仪器是_______。
②下列操作中,容量瓶不具备的功能是_____(填仪器序号)。
a.配制一定体积准确浓度的标准溶液 b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液 d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需称取称量NaClO固体的质量为______g。
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是______。(填序号)。
A.定容时俯视刻度线 B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容 D.定容时水多用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如图所示。下列说法不正确的是
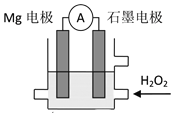
A.该电池正极的电极反应式:2H++H2O2+2e-=2H2O
B.石墨电极上发生还原反应
C.溶液中H+向石墨电极移动
D.电池工作时,电子从Mg电极经导线流向石墨电极,再由石墨电极经电解质溶液流向Mg电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是( )
A.用粘土焙烧制的红陶,陶器显红色的原因可能是含有![]()
B.氢氧化铝、小苏打可作胃酸的中和剂
C.烟花中添加了含铁、铂元素的化合物会更加绚丽缤纷
D.水玻璃暴露在空气中会发生变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述不正确的是( )
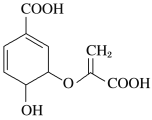
A. 分子中含有4种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1 mol 分枝酸最多可与2 mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com