
A��B��C��D��E��λ�ڶ����ڵ�����Ԫ�ء���֪�������ȶ��ԣ�HmD��HmC���� ��
��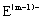 ������ͬ�ĵ��Ӳ�ṹ����A��B��ͬһ���ڣ��ڸ�������������Ԫ���У�A��ԭ�Ӱ뾶���B�����Ӱ뾶��С����A��B������֮����D��������3��������������Ϣ����Ӧ����ѧ�����ش��������⣺
������ͬ�ĵ��Ӳ�ṹ����A��B��ͬһ���ڣ��ڸ�������������Ԫ���У�A��ԭ�Ӱ뾶���B�����Ӱ뾶��С����A��B������֮����D��������3��������������Ϣ����Ӧ����ѧ�����ش��������⣺
(1) HmDm�ĵ���ʽ___________________��
(2)  ��
��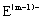 �Ļ�ԭ��ǿ��˳��Ϊ��_________����֤���仹ԭ��ǿ�������ӷ���ʽΪ_________________________________________________________��
�Ļ�ԭ��ǿ��˳��Ϊ��_________����֤���仹ԭ��ǿ�������ӷ���ʽΪ_________________________________________________________��
(3) ��E�ĵ���ͨ��A��D�γɵĻ������ˮ��Һ�У������ӷ���ʽΪ��
_________________________________________________________________��
(4) �����£��������ʵ���Ũ�ȵ�HmC��Һ��A������������Ӧ��ˮ������Һ�������ϣ�д���÷�Ӧ�����ӷ���ʽ ���ڸ���Һ�������к��еĻ�ѧ��������
(5) ��A��B��C��E�����У���������ת����ϵ����_____________����Ԫ�ط��ţ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ҩƷ��ǩ���йط�������ȷ����
| ѡ�� | A | B | C | D | ||||||
| ��Ʒ��ǩ |
 | ҩƷ��������
|
 |
 | ||||||
| ���� | ���Լ�Ӧװ��������ϸ��ƿ�� | ��ҩƷ������Ƥ��ֱ�ӽӴ� | �����������ֽ� | ������Ũ��Ϊ18��4mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴ӦA��g��+ 2 B��g��  3C��g��+ 4 D��g�� �������ֲ�ͬ����µķ�Ӧ�������£����з�Ӧ���е�������
3C��g��+ 4 D��g�� �������ֲ�ͬ����µķ�Ӧ�������£����з�Ӧ���е�������
A��v��A��= 0.15 mol/��L��min �� B��v��B��= 0.5 mol/��L��min��
C��v��C��= 0.4 mol/��L��min�� D��v��D��= 0.02 mol/��L��s����Դ:ѧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�RO ��R���ɷ�����Ӧ��RO
��R���ɷ�����Ӧ��RO ��5R����6H��== 3R2��3H2O�����й���RԪ�ص������У���ȷ����
��5R����6H��== 3R2��3H2O�����й���RԪ�ص������У���ȷ����
A��Ԫ��Rλ�����ڱ��еڢ�A��
B��RO �е�Rֻ�ܱ���ԭ
�е�Rֻ�ܱ���ԭ
C��R2�ڳ��³�ѹ��һ��������
D����1 mol RO ����÷�Ӧ����ת�Ƶĵ��ӵ����ʵ���Ϊ5 mol
����÷�Ӧ����ת�Ƶĵ��ӵ����ʵ���Ϊ5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1 mol A2��1 mol B2ͨ��һ�ݻ�������ܱ������У���һ���¶Ⱥʹ��������£�������Ӧ��2A2(g)��B2(g)  2A2B(g)����Ӧ�ﵽƽ��ʱA2BΪ0.3 mol������ʱ����0.5 mol A2��0.5 mol B2�������´ﵽƽ���A2B�����ʵ���
2A2B(g)����Ӧ�ﵽƽ��ʱA2BΪ0.3 mol������ʱ����0.5 mol A2��0.5 mol B2�������´ﵽƽ���A2B�����ʵ���
A����0.15 mol
B������0.3 mol
C������0.15 mol
D������0.15 mol����0.3 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ʹ0.1mol/L��NaHCO3��Һ��c(H+)��c(CO32-)��c(HCO3-)������
A��ͨ�������̼���� B�������������ƹ���
C��ͨ���Ȼ������� D�����뱥��ʯ��ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������Т�©����������ƿ����������ƿ������ƽ���ݷ�Һ©�����ζ��ܣ���ȼ�ճף����������ʷ������( )
A���٢ۢ� B���٢ڢ� C���٢ۢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ���ǣ� ��
 A�������£�44g��ȩ�����������Ļ�����к��е�̼ԭ����ĿΪ2NA
A�������£�44g��ȩ�����������Ļ�����к��е�̼ԭ����ĿΪ2NA
 B����״���£�22.4L �״��к��е���ԭ����Ϊ1.0NA
B����״���£�22.4L �״��к��е���ԭ����Ϊ1.0NA
 C��ʳ���к������ᣬ��������Ҵ����������õ�
C��ʳ���к������ᣬ��������Ҵ����������õ�
 D��ú����ˮ������Ӧ�Ƴ�ˮú����ˮú������Ҫ�ɷ�ΪCO��H2
D��ú����ˮ������Ӧ�Ƴ�ˮú����ˮú������Ҫ�ɷ�ΪCO��H2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com