
����Ŀ���ۺ��Ȼ��������ǽ���AlCl3��A1(OH)3֮���һ��ˮ�������߷��Ӿۺ�����Ʊ�ԭ����Ҫ�����ӹ���ҵ�ķ����������ң�����Ҫ��Al2O3��Al������SiO2�����ʡ��ۺ��Ȼ������������������£�
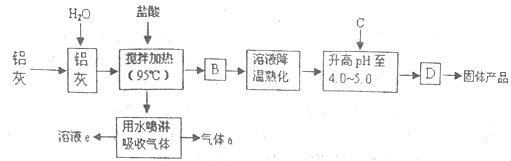
��1����Ӧ�и���Ʒa��______���û�ѧʽ��ʾ����
��2������pH��4.0��4.5��Ŀ����______��
��3�����������п�ѭ��ʹ�õ�������______���û�ѧʽ��ʾ����
��4��Ϊʹ�õ��ľ���ϴ���������������ʹpH���ߵ�C���ʿ�ѡ��______�����ţ���
a��NaOHb��Alc����ˮd��A12O3e��NaAlO2
��5���ۺ��Ȼ�������Ļ�ѧʽ�ɱ�ʾΪ[A12(OH)nCl6-nH2O]m��ʵ����Ϊ�ⶨn��ֵ���������²�����
�ٳ�ȡag���壬�Ƴɷ�ĩ���������������ٱ仯ʱ���õ�bg���˹��̿����õ�������������______��
a.������ b.���� c.�в� d.�Թ�
����ȡa g���壺��A�Լ��ܽ��������AgNO3��Һ������C������ϴ�ӡ���ɡ�����Ϊcg�����Լ�AΪ______�����������ƣ���C����Ϊ______����������ƣ�������ۺ������n��ֵ_____ ��
���𰸡�H2 �ٽ�AlCl3��ˮ�⣬ʹ�������� HCl b��d b��c ���� ���� (861b-102c)/143.5b
��������
���������Ʊ��ۺ��Ȼ��������������ܽ����ң�Al2O3+6HCl=2AlCl3+3H2O��2Al+6HCl=2AlCl3+3H2����SiO2���������ᣬ����AlCl3��Һ��pH��4.0~5.0��ʹAlCl3����ˮ�⣬���õ��ۺ����Ȼ������ۺ��Ȼ�������{[A12(OH)nCl6-nH2O]m}������Ӧ������Al(OH)3��AlCl3���ɴ˷�����
(1)�����м�������������950C���з�Ӧ2Al+6HCl=2AlCl3+3H2����ͬʱ����ӷ���HCl���壬��˲�����H2�л���HCl���壬��ˮ�������������е�HCl�����Ը���Ʒa��H2��
(2)��Ϊ�ۺ��Ȼ��������ǽ���AlCl3��A1(OH)3֮������ʣ�AlCl3����Һ�з���ˮ������Al(OH)3��Al3++3H2O![]() Al(OH)3+3H+��������Һ��pH��4.0~5.0��Ŀ���ǣ��ٽ�AlCl3��ˮ�⣬ʹ����������
Al(OH)3+3H+��������Һ��pH��4.0~5.0��Ŀ���ǣ��ٽ�AlCl3��ˮ�⣬ʹ����������
(3)�����м�������������950C��������H2�л�������ӷ�������HCl���壬��ˮ��������õ�����Һe��Ϊϡ������Һ���������ѭ��ʹ�á��������������п�ѭ��ʹ�õ����ʵĻ�ѧʽΪHCl��
(4)�����c������Ϊ�˴ٽ�AlCl3��ˮ�ⷴӦ��Al3++3H2O![]() Al(OH)3+3H+��Al��Al2O3����������H+��������Һ��pH��2Al+6H+=2Al3++3H2����Al2O3+6H+=2Al3++3H2O��Ϊ�������µ����ʣ�c����Ӧѡ��Al��Al2O3����ѡb��d��
Al(OH)3+3H+��Al��Al2O3����������H+��������Һ��pH��2Al+6H+=2Al3++3H2����Al2O3+6H+=2Al3++3H2O��Ϊ�������µ����ʣ�c����Ӧѡ��Al��Al2O3����ѡb��d��
(5)�پ����Ƴɷ�ĩҪ���в��н������飬���ȹ�������һ��ʹ����������ѡbc���ڸ�ʵ��Ŀ���Dzⶨa g������Cl-�����ʵ������ܽ⾧����Լ�Ӧ��ѡ��������Һ�������ܽ⾧��Ҳ������Cl-���ʵ����IJⶨ��������AgNO3��Һ��Ϊ�˽������е�Cl-ת��ΪAgCl����������c�����ǹ��������õ�c g������AgCl������c gAgCl�����ʵ���=![]() =
=![]() mol���ۺ��Ȼ�������[A12(OH)nCl6-nH2O]m������Ӧ��Al(OH)3��AlCl3���ƣ����Լ��Ⱦ������������AlCl3ˮ����ȫ����Al(OH)3������Al(OH)3���ȷֽ⣬���������������ٱ仯ʱ�����õ�b g������Al2O3�����a g��������Ԫ�����ʵ���=
mol���ۺ��Ȼ�������[A12(OH)nCl6-nH2O]m������Ӧ��Al(OH)3��AlCl3���ƣ����Լ��Ⱦ������������AlCl3ˮ����ȫ����Al(OH)3������Al(OH)3���ȷֽ⣬���������������ٱ仯ʱ�����õ�b g������Al2O3�����a g��������Ԫ�����ʵ���=![]() =
=![]() mol�����Ծۺ��Ȼ�������{[A12(OH)nCl6-nH2O]m}����Ԫ������Ԫ�����ʵ���֮��=2:(6-n)=
mol�����Ծۺ��Ȼ�������{[A12(OH)nCl6-nH2O]m}����Ԫ������Ԫ�����ʵ���֮��=2:(6-n)= ![]() :
:![]() �����n=
�����n=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������Ĺ�������ʾ��ͼ���£�

���������գ�
��1������ˮ���������A��B�����ʣ�������A��Դ��ʯ��Ҥ������д��A��B�Ļ�ѧʽ��
A_____________________ B_____________________��
��2��ʵ�����ᴿ���ε�ʵ���������Ϊ��_________
ȡ����________�� ���� ��________��______ �� ��ȴ�ᾧ �� _______ �� ��� ��
��3����ҵ��������Ĺ��������У���ͨ��������ͨ������̼��ԭ����________________��
��4��̼�ữʱ������������____________________________________��̼�ữ����ˣ���ҺD����Ҫ�ijɷ���____________����д��ѧʽ����
��5����Ʒ�����к���̼�����ơ�����ü��ȷֽ�ķ����ⶨ������̼�����Ƶ�������������֪����Ʒ����Ϊm1�����Ⱥ��������Ϊm2����������̼�����Ƶ����������ɱ�ʾΪW(NaHCO3)=_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0.0500 mol��L-1H2C2O4(��Ԫ����)��Һ�ζ� 25.00 mL 0.100 0 mol L-1NaOH��Һ���õζ���������ͼ������˵����ȷ���ǣ� ��

A. �����ʾ��Һ�У�c(H+)+c(H2C2O4)+ c(HC2O4-)=c(OH-)
B. �����ʾ��Һ�У�c(HC2O4-)+c(C2O42-)=c(Na+)
C. �����ʾ��Һ�У�c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. �ζ������п��ܳ��֣�c(Na+) > c(C2O42-) =c(HC2O4-)>C(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)+3B(g)![]() 2C(g)+2D(g)���ڲ�ͬ����²�÷�Ӧ���ʣ��䷴Ӧ����������
2C(g)+2D(g)���ڲ�ͬ����²�÷�Ӧ���ʣ��䷴Ӧ����������
A. ��(D)=0��4 mol / (L��s)
B. ��(C)=0��5 mol / (L��s)
C. ��(B)=0��6 mol / (L��s)
D. ��(A)=0��15 mol / (L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú�ͭ�����Ĵ�п�Ʊ�����п��������ʡ���������ͼ���й��������£�

���� | Cu(OH)2 | Zn(OH)2 | Fe(OH)3 | ZnS | CuS |
Ksp | 5.0��10��20 | 2.0��10��16 | 4.0��10��38 | 1.2��10��23 | 8.5��10��45 |
��ش��������⣺
��1����п�е�ͭ������ϡ��Һ��Ӧ�Ļ�ѧ����ʽΪ__________________________��ͼ�д�������XҪ�ܹ�������ɫ��ѧ˼�룬���貹������______���ѧʽ����
��2������ҺI��c(Cu2��)Ϊ0.05mol��L��1������ҺII��c(Fe3��)��____mol��L��1��
��3��������A��Zn��ȡ9.61 g����C�ܽ���������500mL 2 mol��L��1ϡ�����У����ռ�����״����2.24L�����壬��������Һ�м���2 mol��L��1NaOH��Һ�������ɳ������ʱ������������Ϊ_____g��������A����һ�����ʣ�ȡ���ֹ���C���Թ��У�������������г�����ζ���壬��÷�Ӧ�����ӷ���ʽΪ________________________��
��4����Һ������Ũ����____________�����ˡ�ϴ�ӡ�������õ��ϴ���������п���壻��Һ�������Ʊ�ZnS��ʵ��ѡ����ǣ�NH4��2S��Һ������Na2S��Һ��Ϊ��Ӧ������Ǻ����Ƶõ�ZnS���н϶�����ʣ����������____________���ѧʽ����
��5������п���������Ըɵ�صĸ������ɵ�ز�ʹ��ʱ�����ڸ�����������Һ�Ӵ��������Էŵ練Ӧ��2NH4����Zn��2NH3��H2����Zn2������ɵ����Զ����١�д��Ǧ���ز�ʹ��ʱ���������Ϸ����Էŵ�Ļ�ѧ����ʽ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪��Ti(s) +2Cl2(g) = TiCl4(l) ��H = ��804.2 kJ ��mol��1��
2Na(s) +Cl2(g) = 2NaCl(s) ��H = ��882.0 kJ ��mol��1
Na(s) = Na(l) ��H =2.6 kJ ��mol��1
��д����Һ̬�������Ȼ����û����ѵ��Ȼ�ѧ����ʽ__________________________��
��2����֪����һ������㶨Ϊ2L���ܱ������г���4mol A��1mol B���������·�Ӧ��4A(g)��B(s) ![]() 3C(s)��4D(g)���÷�Ӧ�и����ʵ�Ħ����������λg��mol��1������һ������һ�������¸÷�Ӧ2���Ӵﵽƽ�⡣
3C(s)��4D(g)���÷�Ӧ�и����ʵ�Ħ����������λg��mol��1������һ������һ�������¸÷�Ӧ2���Ӵﵽƽ�⡣
�ٲ��ܹ�˵���÷�Ӧ�Ѵﵽƽ����ǣ�________��
A�������£������ڵ�ѹǿ���ٱ仯
B�������£������ڻ��������ܶȲ��ٱ仯
C��һ�������£�D������������ֲ���
D��һ�������£���λʱ��������4molA��ͬʱ����1 mol B
��ƽ�����D��Ũ��Ϊ0.3mol��L��1����ӷ�Ӧ��ʼ��ƽ��ʱ��A��ƽ����Ӧ����Ϊ________��Bת����Ϊ________��
��3���û���̿��ԭ�����Դ�����������йط�ӦΪ��2NO(g)+C(s) ![]() N2(g)+CO2(g)����H����ij�ܱ���������һ�����Ļ���̿��NO����t���·�Ӧ���й�������ͼ��
N2(g)+CO2(g)����H����ij�ܱ���������һ�����Ļ���̿��NO����t���·�Ӧ���й�������ͼ��
NO | N2 | CO2 | |
��ʼŨ��/molL��1 | 0.10 | 0 | 0 |
ƽ��Ũ��/molL��1 | 0.04 | 0.03 | 0.03 |
����t���£��÷�Ӧ��ƽ�ⳣ��Ϊ________��������λ��Ч���֣���
��ƽ��������¶ȣ��ٴδﵽƽ�⣬���������NO��N2��CO2��Ũ��֮��Ϊ2:1:1����÷�Ӧ��
��H________0(�����������������������ʱNO��ת����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ��������У���ȷ����(����)
A. HClO������̿����ʹijЩ��ɫ������ɫ��˵�����߾���������
B. ���ȷֱ�ʢ��NaHCO3�͵����֧�Թܣ��Թܵײ���������٣�˵�����߾���������
C. ������ǯ��סһС����ɰֽ��ϸ��ĥ���������ھƾ����ϼ��ȣ��ۻ����Һ̬����������
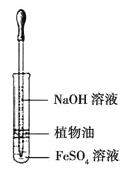
D. ����ͼװ�ù۲� Fe(OH)2 ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧʵ�顱���߽����ã������������ϡ���ɫ��ѧ���������

��ʵ�����ռ���������ͼ����ʾװ��
��ʵ���������������Ʒ�Ӧ��ʵ��ʱ����ͼ����ʾװ��
��ʵ�������ò������ֱ�պȡŨ�����Ũ��ˮ��������HCl��Ӧ������ε�ʵ��
��ʵ�����в���ͼ����ʾװ�ý���ͭ��ϡ����ķ�Ӧ
A. �ڢۢ� B. �٢ڢ�
C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ�����pH=3��CH3COOH��Һ��������������ȷ���ǣ� ��
A. c(H+)= c(CH3COO��)+ c(OH��)
B. ��������CH3COONa�����c(CH3COO��)����
C. ����Һ����ˮ�������c(H+)��1.0��10��11mol��L
D. ������pH =11��NaOH��Һ��Ϻ���Һ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com