
【题目】(1)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,反应的离子方程式是_______________.
(2)在碘和淀粉形成的蓝色溶液中通入SO2气体,发现蓝色逐渐消失,反应的离子方程式是_______________.
(3)对比(1)和(2)实验所得的结果,将Cl-、I-、SO2按还原性由强到弱顺序排列为_______________.
(4)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O.
①当有0.2mole-转移时被氧化的HCl的质量是_______________;
②如果将20mL12molL-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将_______________.
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L.
【答案】(1)2I-+Cl2═I2+2Cl-;(2)I2+SO2+2H2O═2I-+SO42-+4H+;
(3)SO2>I->Cl-;(4)①7.3g; ②D
【解析】
试题分析:(1)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,证明有I2生成,离子方程式为:2I-+Cl2═I2+2Cl-;(2)在碘和淀粉形成的蓝色溶液中通入SO2气体,发现蓝色逐渐消失,证明I2与SO2发生氧化还原反应,离子方程式为:I2+SO2+2H2O═2I-+SO42-+4H+;(3)在实验(1)的反应中,碘元素化合价升高,被氧化,I-作还原剂,I2为氧化产物;氯元素化合价降低,被还原,Cl2作氧化剂,Cl-为还原产物;故还原性:I->Cl-;在实验(2)的反应中,碘元素化合价降低,被还原,I2作氧化剂,I-为还原产物;硫元素化合价升高,被氧化,SO2作还原剂,SO42-为氧化产物;故还原性:SO2>I-;故答案:SO2>I->Cl-;(4)①氯元素由-1价升高为0价,当有5mol Cl2生成时,被氧化HCl为10mol,转移电子的物质的量为10mol,因此当有0.2mole-转移时被氧化的HCl为0.2mol,质量为![]() ;②20mL 12molL-1的浓盐酸的物质的量为:
;②20mL 12molL-1的浓盐酸的物质的量为:![]() ;假设HCl全部参加反应,则
;假设HCl全部参加反应,则![]() ,故生成氯气的物质的量为
,故生成氯气的物质的量为![]() ,收集到氯气在标准状况下的体积为:
,收集到氯气在标准状况下的体积为:![]() 。但是实际上0.24mol的HCl并未全部参加反应,原因有二,第一,浓盐酸易挥发;第二,随着反应进行,浓盐酸逐渐变为稀盐酸,而稀盐酸不与二氧化锰反应。因此,实际上收集到的氯气在标准状况下的体积<1.68L,故答案D。
。但是实际上0.24mol的HCl并未全部参加反应,原因有二,第一,浓盐酸易挥发;第二,随着反应进行,浓盐酸逐渐变为稀盐酸,而稀盐酸不与二氧化锰反应。因此,实际上收集到的氯气在标准状况下的体积<1.68L,故答案D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】NaHCO2和Na2O2按2:1的个数之比混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分是
A.只有 Na2CO3 B.NaHCO3和Na2CO3
C.NaOH和Na2CO3 D.Na2O2和NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氯及其化合物的说法错误的是
A.工业上电解熔融的氯化钠可以制备钠
B.工业上用Cl2和石灰乳为原料制造漂白粉
C.工业上电解饱和氯化镁溶液可制取金属镁
D.工业上常用H2在Cl2中燃烧生成的氯化氢溶于水来制取盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①0.01mol/LNaOH溶液的pH= 。
②100mL 0.1mol/L H2SO4溶液与100mL 0.4mol/L的KOH溶液混合后,pH= 。
(2)①已知一溶液有4种离子:X+、![]() 、H+、OH-下列分析结果肯定错误的是( )。
、H+、OH-下列分析结果肯定错误的是( )。
A.CY->CX+>CH+>COH- B.CX+>CY->COH->CH+
C.CH+>CY->CX+>COH- D.COH->CX+>CH+>CY-
②把0.02mol·L-1CH3COOH溶液和0.01mol·L-1NaOH溶液以等体积混合,则混合液中粒子浓度关系正确的是( )
A.C(CH3COO-)<C(Na+)
B.C(CH3COOH)>C(CH3COO-)
C.2C(H+)=C(CH3COO-)-C(CH3COOH)
D.C(CH3COOH)+C(CH3COO-)=0.01mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨:N2(g)+3H2(g)![]() 2NH3(g) △H<0,氨又可以进一步制各硝酸,在工业上一般可进行连续生产。请回答下列问题:
2NH3(g) △H<0,氨又可以进一步制各硝酸,在工业上一般可进行连续生产。请回答下列问题:

若有68g氨气经催化氧化完全生成NO(g)和H2O(g)所放出的热量为___________KJ。
(2)合成氨反应达到平衡后,某时刻改变下列选项中的__________条件,在达到新平衡的过程中逆反应速率始终增大。
a.升温 b.缩小容积 c.增大c(N2) d.使用催化剂
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成氨反应的影响。实验结果如下图所示:(图中T表示温度,横轴表示起始时H2的物质的量,纵轴表示平衡时NH3的体积分数)
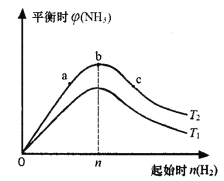
图像中T1和T2的关系是:T1____________T2 (填“>”“<”或“=”)。
比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是_______________(填字母)。
③若容器容积为1L,b点对应的起始时n(H2)=0.30mol,测得平衡时H2的转化率为60%,则平衡时c(N2)为_________________mo1·L-1。(已知反应物的物质的量按n(H2):n(N2)=3:1投料时,平衡时NH3的体积分数最大)
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同温度(T)、不同时间段内工业合成氨反应中N2的转化率,得到数据如下表所示:
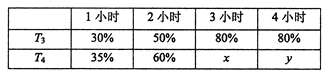
上表中x、y的大小关系为x_____________y。(填“>”“=”“<”“≥”或“≤”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①现有11g CO2和5.5g N2O的物质的量之比为 ,摩尔质量之比为 ,氧原子的个数之比为 .
(2)质量相等的两种物质SO2和SO3,两种物质中硫元素质量之比为 ___________ ,分子物质的量之比为 ___________ ,所含氧原子个数之比为 ___________ .
(3)0.2L 0.5mol/L Al2(SO4)3溶液和0.5L 0.5mol/L Al2(SO4)3溶液所含SO42-离子浓度之比为 ___________ ,SO42-离子数目之比为 ___________ .
(4)20.6g NaR含有Na+0.2mol,则NaR的摩尔质量为 ___________ ,则含R 8.0g的NaR的物质的量为 ___________ mol.
(5)实验室用二氧化锰与浓盐酸反应制取氯气,反应方程式如下:
MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
若0.1molMnO2与足量的浓盐酸充分反应,则有 __________ mol HCl被氧化,转移电子的物质的量为 __________ mol,产生的Cl2在标准状况下的体积为 __________ L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述中正确的是( ) 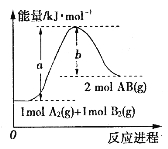
A.该反应的△H=(b-a)KJ·mol-1
B.每生成2个AB分子吸收(a-b)KJ热量
C.该反应中反应物的总键能大于生成物的总键能
D.断裂1mol A-A键和1mol B-B键,放出a KJ能量 、
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境、保护地球已成为人类共同的呼声。下列措施不利于环境保护的是( )
A. 推广使用无铅汽油 B. 提倡使用太阳能
C. 推广使用无磷洗衣粉 D. 提倡个人使用大批量汽车
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com