
【题目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。
请回答下列问题。
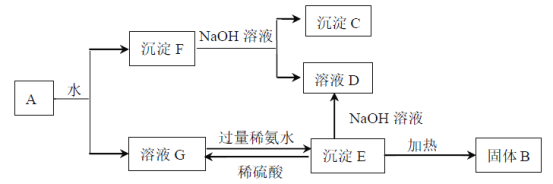
(1)图中涉及分离溶液与沉淀的方法是______________________________。
(2)B、C、D、E4种物质的化学式为:B___________、C___________、D___________、E___________。
(3)沉淀F与NaOH溶液反应的离子方程式为_________________________________。溶液G与过量稀氨水反应的化学方程式为____________________________________。
【答案】过滤 Al2O3 Fe2O3 NaAlO2 Al(OH)3 Al2O3+2OH-= 2AlO2-+H2O Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+3(NH4)2 SO4
【解析】
Al2(SO4)3易溶于水,Al2O3、Fe2O3难溶于水,所以沉淀F是Al2O3、Fe2O3, G是Al2(SO4)3溶液;
Al2O3与氢氧化钠溶液反应生成偏铝酸钠,Fe2O3与氢氧化钠溶液不反应,所以沉淀C是Fe2O3、D是偏铝酸钠溶液;Al2(SO4)3与过量氨水反应生成氢氧化铝沉淀和硫酸铵,则E是Al(OH)3,Al(OH)3加热分解为Al2O3;Al(OH)3与氢氧化钠反应生成偏铝酸钠溶液。
(1)固体与液体分离用过滤法,图中涉及分离溶液与沉淀的方法是过滤。
(2)根据以上分析,B是氧化铝,化学式是Al2O3;C是氧化铁,化学式是Fe2O3;D是偏铝酸钠,化学式是NaAlO2;E是氢氧化铝,化学式是Al(OH)3。
(3)沉淀F中的Al2O3与NaOH溶液反应生成偏铝酸钠,反应的离子方程式为Al2O3+2OH-= 2AlO2-+H2O。G是Al2(SO4)3溶液,与过量稀氨水反应生成氢氧化铝沉淀和氯化铵,反应的化学方程式为Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+3(NH4)2 SO4。


科目:高中化学 来源: 题型:
【题目】某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料![]() ,其工艺流程如图所示:
,其工艺流程如图所示:
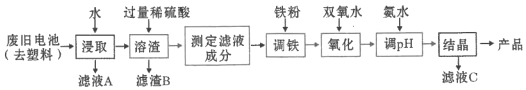
(1)碱性锌锰电池的工作原理:________![]() ________
________![]() ________
________![]() ________
________![]() ________(配平方程式),其中的电解质溶液是
________(配平方程式),其中的电解质溶液是![]() 溶液。滤液
溶液。滤液![]() 中主要溶质的电子式为______。
中主要溶质的电子式为______。
(2)已知![]() 中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将![]() 价锰的化合物全部还原成
价锰的化合物全部还原成![]() ,写出该反应的离子方程式________。
,写出该反应的离子方程式________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式![]() 相符合。
相符合。
①写出“调铁”工序中可能发生反应的离子方程式________,________。
②若“测定滤液成分”结果为![]() ,
,![]() ,滤液体积为
,滤液体积为![]() ,“调铁”工序中,需加入的铁粉质量为________
,“调铁”工序中,需加入的铁粉质量为________![]() (忽略溶液体积变化,用含
(忽略溶液体积变化,用含![]() 、
、![]() 的代数式表示)。
的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是把![]() 氧化为
氧化为![]() ;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
(6)从滤液![]() 中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将8.96 L氯化氢气体溶于水形成100 mL溶液,然后与足量的铁屑反应。
(1)所得盐酸溶液的物质的量浓度是多少________?
(2)参加反应的铁的质量是多少________?
(3)标况下生成氢气的体积是多少________?
(4)将生成的氯化亚铁配成400 mL溶液,此溶液中氯化亚铁的物质的量浓度是多少________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用18.4 mol/L的浓H2SO4来配制500mL0.2 mol/L的稀H2SO4。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥托盘天平⑦药匙。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时不需要使用的有_____________(填代号),还缺少的仪器是______________________。
(2)经计算,需浓H2SO4的体积为___________,量取浓硫酸时应选用___________(填序号)(选填①10mL、②50mL、③100mL三种规格)的量筒。
(3)将所配制的稀H2SO4进行测定,发现浓度小于0.2 mol/L。请你分析配制过程中可能引起浓度偏低的原因是___________(填字母)。
a.定容时俯视标线 b.烧杯和玻璃棒没有洗涤
c.加蒸馏水不慎超过刻度线 d.容量瓶使用前内壁沾有水珠
e.定容时仰视标线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物(如图)由 W、X、Y、Z 四种短周期元素组成,其中 W、Y、Z 分别位于三个不同周期,Y 核外最外层电子数是 W 核外最外层电子数的二倍;W、X、Y 三种简单离子的核外电子排布相同。下列说法不正确的是

A.原子半径:W < X < Y < Z
B.X 与 Y、Y 与 Z 均可形成具有漂白性的化合物
C.简单离子的氧化性: W X
D.W 与 X 的最高价氧化物的水化物可相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“双线桥”标出电子转移的方向和数目,并分别指出 氧化剂和氧化产物。
(1)Fe+CuSO4=FeSO4+Cu ________ 氧化剂是 ____________氧化产物是_____________,
(2)3CO+Fe2O3![]() 3CO2+2Fe ________ 氧化剂是 ____________氧化产物是_____________,
3CO2+2Fe ________ 氧化剂是 ____________氧化产物是_____________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X、Y、Z三种元素,已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
②X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤Z的单质溶于X2Y中,所得溶液具有漂白作用。
请完成下列问题:
(1)请写出Z-的的离子结构示意图_____________。
(2)请写出Z单质溶于X2Y中发生反应的化学方程式_____________。
(3)请写出Z单质与NaOH反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒是地壳中含量第21丰富元素,是人体必需的微量元素,对治疗糖尿病和癌症及保护心血管等具有潜在的药理学作用。工业上用含三价钒![]() 为主的某石煤为原料(含有
为主的某石煤为原料(含有![]() 、CaO等杂质),钙化法焙烧制备
、CaO等杂质),钙化法焙烧制备![]() ,其流程如下:
,其流程如下:
![]()
已知:+5价钒在溶液中的主要存在形式与溶液pH的关系如下表。
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 |
|
|
|
|
(1)焙烧:向石煤中加生石灰焙烧,将![]() 转化为
转化为![]() 的化学方程式是________________。
的化学方程式是________________。
(2)酸浸:![]() 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的
难溶于水,可溶于盐酸。若焙砂酸浸时溶液的![]() ,
,![]() 溶于盐酸的离子方程式是________________。
溶于盐酸的离子方程式是________________。
(3)转沉:将浸出液中的钒转化为![]() 固体,其流程如下:
固体,其流程如下:
![]()
①浸出液中加入石灰乳的作用是____________________________________。
②向![]() 溶液中加入
溶液中加入![]() 溶液,控制溶液的
溶液,控制溶液的![]() 。当
。当![]() 时,
时,![]() 的产量明显降低,原因是_______________________________________。
的产量明显降低,原因是_______________________________________。
(4)实验室以![]() 为原料还可以合成用于制备
为原料还可以合成用于制备![]() 的氧钒(IV)碱式碳酸铵晶体,过程如下:
的氧钒(IV)碱式碳酸铵晶体,过程如下:
![]()
①步骤ⅱ可在如图装置(气密性良好)中进行。已知:![]() 能被
能被![]() 氧化。
氧化。
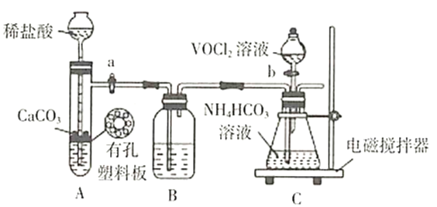
药品填装完成后的实验操作是________(填“活塞a”、“活塞b”的操作顺序),装置B中的试剂是________。
②测定氧钒(IV)碱式碳酸铵晶体粗产品中钒的含量。
称量4.246g样品于锥形瓶中,用20mL蒸馏水与30mL硫酸混合溶解后,加![]() 的
的![]() 溶液至稍过量,充分反应后继续加1%
溶液至稍过量,充分反应后继续加1%![]() 溶液至稍过量,再用尿素除去过量的
溶液至稍过量,再用尿素除去过量的![]() ,最后用
,最后用![]() 的
的![]() 标准溶液滴定至终点,消耗体积为30.00mL(滴定反应:
标准溶液滴定至终点,消耗体积为30.00mL(滴定反应: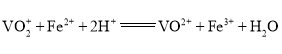 )。
)。
![]() 溶液的作用是________________,粗产品中钒的质量分数为________________(精确到小数点后两位)。
溶液的作用是________________,粗产品中钒的质量分数为________________(精确到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在铝表面除去氧化膜,物理方法可用_________,化学方法可将其浸入氢氧化钠溶液,发生反应的化学方程式为:_________;
(2)将除去氧化膜的铝迅速用蒸馏水清洗干净,立即插入硝酸汞溶液片刻,发生反应的离子方程式为:__________________;取出铝片用滤纸吸去表面溶液,铝片上出现的“黑斑”是_________;
(3)将此铝放置于空气中,“黑斑”边会长出“白毛”,此物质是_________.
(4)此实验证明了(________)
A.氧化铝都是十分坚硬的晶体 B.铝是较活泼的金属,可以被空气中氧气氧化
C.铝表面的氧化膜有保护作用 D.铝是很不活泼的金属,不可以被氧气氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com