
【题目】CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是( ) 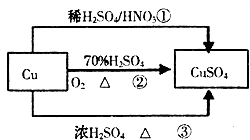
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②<③
D.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
【答案】D
【解析】解:A.Cu与混酸反应,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子反应为:3Cu+8H++2NO3﹣=3Cu2++2NO↑+4H2O,从方程式知,硝酸根离子由硝酸提供,氢离子由硝酸和硫酸提供,所以硝酸为2mol时,硫酸为3mol,用混酸中H2SO4与HNO3物质的量之比最好为3:2,故A正确;
B.相对于途径①、③,途径②的优点:制取等质量胆矾需要的硫酸少、途径2无污染性气体产生,故B正确;
C.生成等量的硫酸铜,三个途径中①②参加反应的硫酸的物质的量相等,而③生成SO2 , 消耗更多的硫酸,则①=②<③,故C正确;
D.途径②中硫酸只表现为酸性,没有被还原,故D错误.
故选D.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上常用高炉来进行炼铁,其原理如下。
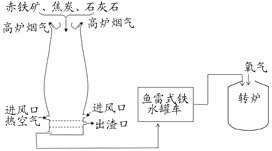
(1)用CO和赤铁矿(Fe2O3)炼铁的化学反应方程式是_________。
(2)请从A或B两题中任选一个作答,若两题都作答,按A计分。
A | B |
用含氧化铁160t的赤铁矿炼铁,理论上可以制得纯铁_____t 。 | 工业上也常用主要成分为四氧化三铁的磁铁矿做炼铁原料。四氧化三铁中铁元素的质量分数计算式为______×100%。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙是中学常见的三种气体单质,相互间反应可制得化肥B.其转化关系如图1所示:
(1)将B中所含元素填写在如表的恰当位置中(用元素符号表示)
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ||||||||
2 | ||||||||
3 |
(2)已知反应一是放热反应,画出能量关系示意图.
(3)为加快反应一的速率,可采取的措施有:适当升高温度、选用恰当的催化剂、增大某一反应物的浓度和 .
(4)方法一的化学方程式是 .
(5)用方法二也能制得B:甲和丙反应的产物与A反应即可,这两种方法更好的是(填“方法一”或“方法二”),理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,然后乙烯再与溴水反应。
请你回答下列问题。
(1)甲同学的实验中与乙烯有关的化学方程式为:______________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生加成反应,其理由是________。(填写序号)
①使溴水褪色的反应未必是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质未必是乙烯
④使溴水褪色的物质就是乙烯
(3)乙同学推测此乙烯中必定含有一种杂质气体是________,它与溴水反应的化学方程式是_______________。在验证过程中必须全部除去。除去该杂质的试剂可用________。
(4)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用硫酸铝酸性溶液制备可溶性的碱式硫酸铝[Ala(SO4)b(OH)c],并用它对烟气进行脱硫处理的过程如图1: 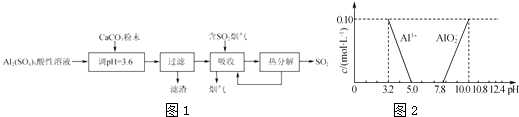
(1)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Ala(SO4)b(OH)c . 过滤时所用的玻璃仪器有、和烧杯,滤渣的主要成分为(填化学式).
(2)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将(填“增大”“减小”或“不变”).
(3)Ala(SO4)b(OH)c中a、b、c的代数关系式为 .
(4)已知在常温下溶液中Al3+、AlO2﹣的浓度与溶液pH的关系如图2所示.为确定碱式硫酸铝的组成,进行如下实验: ①取2.18g碱式硫酸铝样品在空气中灼烧至恒重,样品质量减少了0.36g.
②另取2.18g碱式硫酸铝溶于水,调节溶液的pH到5.0~7.8.
③将②产生的沉淀过滤、洗涤、灼烧至恒重,称量剩余固体为1.02g.
请计算样品中Al3+和SO42﹣的物质的量之比(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年11月首架C919打飞机总装下线,标志着我国跻身飞机研制先进国家行列. ①机身蒙皮使用的是第三代铝锂合金材料.下列不属于铝锂合金性质的是(填字母).
a.密度大 b.硬度大 c.抗腐蚀
②飞机轮胎属于橡胶制品.下列材料可用来合成橡胶的是(填字母).
a.石英砂 b.石灰石 c.异戊二烯
③机体先进复合材料的使用率达12%.下列属于复合材料的是(填字母).
a.钛合金 b.玻璃钢 c.普通陶瓷.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
①质子数相同的粒子一定属于同种元素; ②电子数相同的粒子不一定是同一种元素; ③一种元素只能有一种质量数;④某种元素的相对原子质量取整数,就是其质量数。⑤质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子;⑥同位素的性质几乎完全相同;
A.①③④⑥ B.①②④⑤ C.②③⑤⑥ D. ②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应mA(g)+nB(s)pC(g)+qD(g)反应过程中,其他条件不变时,D的百分含量与温度(T)或压强(P)关系如图所示,反应达平衡后,下列叙述正确的是( ) 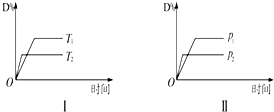
A.升高温度,平衡正移
B.使用催化剂,D的百分含量增加
C.m<p+q
D.B的颗粒越小,反应速率越快,有利于平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com