
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
18 8 |
18 8 |
| A、36 mol |
| B、20 mol |
| C、16 mol |
| D、20 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 反应1 |
| 反应2 |
| C2H5OHNaOH |
| 反应3 |
 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCN溶液和NaOH溶液不等体积混合后一定存在c(H+)-c(OH-)=c(CN-)-c(Na+) |
| B、等温下,等浓度的CH3COONa溶液和NaCN溶液的pH,后者大 |
| C、常温下,pH相同的CH3COOH溶液和HCN溶液分别加水稀释相同的倍数时,前者pH的变化小 |
| D、溶液中由水电离出的c(H+),前者是后者的10m-n倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电过程中,Li向负极区移动 |
| B、正极的电极反应式:LixC6+xe-=xLi+Li1-xC6 |
| C、电子流动方向:负极→外电路→正极→有机电解液→负极 |
| D、充电时阳极电极反应式:LiCoO2-xe-=Li1-xCoO2+x Li |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、①③④⑤ |
| C、①③⑤ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
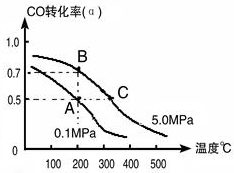
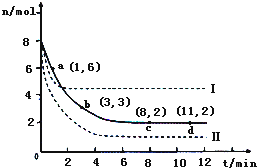
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com