
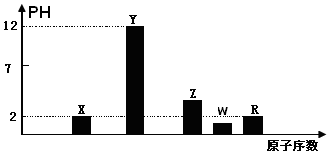


���� I��������X��Y��Z��W��R�Ƕ���������Ԫ����ԭ������������������������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.01mol��L-1����Һ��PH��Y��ӦPH=12��˵��Y���ƣ�X��ӦPH=2��X�ǵ���Z��ӦPH��2������Z���ף�W��ӦPH��2������W��S��R��ӦPH=2ԭ�������������R��Cl��
��1��Cl��ԭ�ӽṹ����3�����Ӳ㡢����������Ϊ7��
��2��Ԫ��Y��W�γɵ�Y2W2�ͻ�������Na2S2��
��3��X������������Ӧ��ˮ����������̬�⻯�ﷴӦ��������泥�
II����1��A���ǽ�����Խǿ��Խ�����������ϣ�
B����ۺ���������Կ�˵��̼������Ԫ�طǽ��������ǿ����
C���ǽ�����Խǿ���⻯��Խ�ȶ���
��2�������̿�֪��COS���������Ʒ�Ӧ������ԭ���غ㣬A��ҺӦ���Ǻ�C�����Σ�����AΪNa2CO3��������Һ��������Na2S2O3�����壬��ԭ���غ㣬����aӦ�����������Դ������
��� �⣺I��������X��Y��Z��W��R�Ƕ���������Ԫ����ԭ������������������������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.01mol��L-1����Һ��PH��Y��ӦPH=12��˵��Y���ƣ�X��ӦPH=2��X�ǵ���Z��ӦPH��2������Z���ף�W��ӦPH��2������W��S��R��ӦPH=2ԭ�������������R��Cl��
��1��Ԫ��R�����ڱ��е�λ���ǣ��������ڵڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
��2��Ԫ��Y��W�γɵ�Y2W2�ͻ�������Na2S2�к��л�ѧ��������Ϊ�����Ӽ����Ǽ��Թ��ۼ����ʴ�Ϊ�����Ӽ����Ǽ��Թ��ۼ���
��3��X������������Ӧ��ˮ����������̬�⻯������ӷ�Ӧ����ʽΪH++NH3=NH4+���ʴ�Ϊ��H++NH3=NH4+��
II����1��A��S��H2�������Ϸ�Ӧ��C��H2���ϸ����ף�����˵��̼������Ԫ�طǽ��������ǿ����ϵΪ��S��C����A��ȷ��
B�����ԣ�H2SO3��H2CO3�����������ۺ����ᣬ����˵��̼������Ԫ�طǽ��������ǿ������B����
C���ȶ��ԣ�CH4��H2S����˵��̼������Ԫ�طǽ��������ǿ����ϵΪ��S��C����C��ȷ��
�ʴ�Ϊ��AC��
��2�������̿�֪��COS���������Ʒ�Ӧ������ԭ���غ㣬A��ҺӦ���Ǻ�C�����Σ�����AΪNa2CO3��������Һ��������Na2S2O3�����壬��ԭ���غ㣬����aӦ����������
���ʻ���COS���ĵ���ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��������������֪��A��Na2CO3������aӦ������������ϵ��ӡ�ԭ�ӡ�����غ��֪��Ӧ��Ϊ2S2-+5H2O$\frac{\underline{\;\;��\;\;}}{\;}$S2O32-+4H2+2OH-����ӦIΪCOS+4NaOH=Na2S+Na2CO3+2H2O���ʴ�Ϊ��COS+4NaOH=Na2S+Na2CO3+2H2O��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɣ�Ϊ��Ƶ���㣬�����ᡢ����Һ��pH�ƶ�Ԫ�ء�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���


 ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
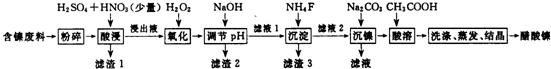
| ��1 | ��2 | |||
| ���� | ��ʼ������pH | ������ȫ��pH | ���� | 20��ʱ�ܽ��ԣ�H2O�� |
| Fe3+ | 1.1 | 3.2 | CaSO4 | �� |
| Fe2+ | 5.8 | ����8.8 | NiF | ���� |
| Al3+ | 3.0 | 5.0 | CaF2 | ���� |
| Ni2+ | 6.7 | 9.5 | NiCO3 | KSP=9.60��10-6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����90mL1.00mol/L��NaCl��Һ����������ƽ��ȡ5.3gNaCl���� | |
| B�� | ʹ������ƿʱ���ȼ������Ƿ�©ˮ��Ȼ��ϴ�����ø��T��ʹ�� | |
| C�� | ����10mL��Ͳ��ȡ8.58mL����ˮ | |
| D�� | ��������Һ���ݺ����·�תҡ�Ⱥ���Һ���½������ˮ����Һ��Һ����̶������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+ Cl- K+ SO42- | B�� | Na+ NO3 - OH - CO3 2- | ||
| C�� | Ba2+ Cl- NO3 - SO4 2- | D�� | K+ Na+ Cl- SO4 2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�м�������Na���壬ƽ�������ƣ�c��H+������ | |
| B�� | ��ˮ�м���ϡ��ˮ��ƽ�������ƶ���c��OH-������ | |
| C�� | ��ˮ�м��������������ƹ��壬c��H+������Kw���䶯 | |
| D�� | ��ˮ���ȣ�Kw����pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| X | Y |
| Z |
| A�� | ��̬�⻯��ķе㣺X��Y��Z | |
| B�� | ��������ϼۣ�Y��X | |
| C�� | X��Y��Z������������Ӧˮ�����У�Z��������ǿ | |
| D�� | ��X��Y��Z��ԭ������֮�͵���25�������Ƕ��Ƿǽ���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��ҺA�е�������ΪFe2+��Fe3+��H+ | |
| B�� | ����Ʒ��Cu��OԪ�ص�������Ϊ10��l | |
| C�� | V=448 | |
| D�� | �ܽ���Ʒʱ����H2SO4�����ʵ���Ϊ0.04 mo1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4Lˮ����NA��ˮ���� | |
| B�� | 1mol/LNa2C03��Һ�к���Na+��ĿΪ2NA | |
| C�� | ���³�ѹ�£�22.4L02�к���2NA����ԭ�� | |
| D�� | 169O2��O3�Ļ�������к���ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2H2��g��+O2��g��=2H2O��l����H1 | B�� | C��s��+$\frac{1}{2}$O2��g��=CO��g����H2 | ||
| C�� | HCl��aq��+NaOH��aq��=NaCl��aq��+H2O�� l ����H3 | D�� | C6H12O6��s��+6O2��g��=6CO2��g��+6H2O�� l ����H4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com