
【题目】等体积,不同浓度的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量浓度之比是
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。

(1)写出下列仪器的名称:b. ___________。
(2)仪器c使用前必须_________________。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是_________。
(4)用质量分数为98%、密度为1.84 g/cm3的浓H2SO4来配制480 mL、0.3 mol·L-1的稀H2SO4。
①装置Ⅱ是某同学转移溶液的示意图,图中的错误是_____________________。除了图中给出的的仪器外,为完成实验还需要的仪器有:___________________。
②根据计算得知,需量取该浓H2SO4的体积为_______________mL。
(5)下列操作,会使所配制的溶液浓度偏大的是____________。
①容量瓶中原来含有少量蒸馏水;
②在未降至室温时,立即将溶液转移至容量瓶定容
③定容转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度
④定容时俯视刻度线;
⑤用量筒量取98%的硫酸时俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素![]() 的原子序数依次增大。
的原子序数依次增大。![]() 是由这些元素组成的二元化合物,常温常压下
是由这些元素组成的二元化合物,常温常压下![]() 为液体,其余均为无色气体。
为液体,其余均为无色气体。![]() 的摩尔质量为
的摩尔质量为![]() 的2倍,
的2倍,![]() 是元素
是元素![]() 的单质,是绿色植物光合作用产生的无色气体,
的单质,是绿色植物光合作用产生的无色气体,![]() 物质能使湿润的红色石蕊试纸变蓝,
物质能使湿润的红色石蕊试纸变蓝,![]() 能使品红溶液褪色。上述物质的转化关系如图所示。下列说法正确的是
能使品红溶液褪色。上述物质的转化关系如图所示。下列说法正确的是

A. ![]() 与
与![]() 均为酸性氧化物B.
均为酸性氧化物B. ![]() 的含氧酸是一种强酸
的含氧酸是一种强酸
C. 沸点:![]() D. 原子半径:
D. 原子半径:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2(g)+I2(g) ![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | c |
下列判断不正确的是
A. HI的平衡浓度:a=b>0.004,c=0.008 B. 平衡时,H2的转化率:丁>甲
C. 平衡时,乙中H2的转化率大于20% D. 丙中条件下,该反应的平衡常数K=0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取氢氧化钠的工艺流程示意图如下:
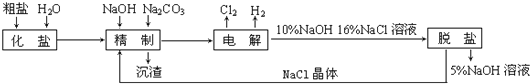
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为_______________________,与电源负极相连的电极附近,溶液pH值_____________(选填:不变、升高或下降)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为_______________________,_______________________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是___________(选填a、b、c,多选扣分)
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为____________(选填a,b,c多选扣分)
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过__________、冷却、___________(填写操作名称)除去NaCl
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和![]() ,相应的化学方程式为______________________。
,相应的化学方程式为______________________。
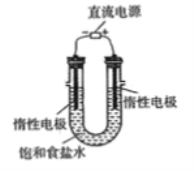
(7)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2____________(填“>”、“=”或“<”)2L,原因是_____________________。
(8)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4→ZnSO4+H2↑、MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
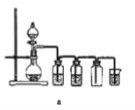
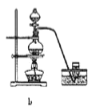
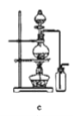
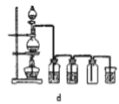
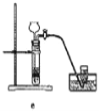
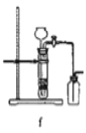
据此,制备并收集干燥、纯净Cl2的装置是______(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的问题常涉及化学知识,下列过程不涉及化学变化的是( )
A. 用食醋除去暖瓶内的水垢
B. 鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀
C. 碘单质遇淀粉变蓝
D. 用75%的乙醇溶液进行皮肤消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的氢气在氯气中燃烧,所得混合物用200mL 3.00mol∕L的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.15mol。(忽略溶液体积的变化)
(1)求原NaOH溶液的质量分数(保留两位小数);___________
(2)所得溶液Cl-中的物质的量浓度;__________
(3)所用氯气和参加反应的氢气的物质的量之比。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B代表不同的物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度。(说明: ![]() 不稳定,不考虑)
不稳定,不考虑)
请填写下列空白:
(1)写出化学式:A1___________、A2__________、B1___________、B2___________。
(2)已知, ![]() ,则
,则![]() 和
和![]() 等体积混合组成溶液中离子浓度由大到小的顺序为______________________。
等体积混合组成溶液中离子浓度由大到小的顺序为______________________。
(3)B1溶液中水的电离程度小于B2溶液中水的电离程度,原因是_________________。
(4)常温下,若B1、B2两种溶液的pH=5,则两溶液中由水电离出的氢离子的物质的量浓度之比为________。
(5)常温下, ![]() 的
的![]() 溶液的
溶液的![]() ,则
,则![]() 的电离平衡常数Ka_______________。
的电离平衡常数Ka_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com