
下列各组物质中,酸性由强到弱排列顺序错误的是( )
|
| A. | HClO4 H2SO4 H3PO4 | B. | HClO4 HClO3 HClO2 |
|
| C. | H2SO4 H2SO3 H2CO3 | D. | HClO HBrO4 HIO4 |
考点:
比较弱酸的相对强弱的实验.
专题:
化学键与晶体结构.
分析:
非金属元素的最高价含氧酸中,非金属的非金属性越强其最高价含氧酸的酸性越强;对于同一种元素的含氧酸来说,该元素的化合价越高,其含氧酸的酸性越强.
解答:
解:A.P、S、Cl元素处于同一周期,且非金属性逐渐增强,且这几种酸都是其相应的最高价含氧酸,所以酸性逐渐减弱,故A不选;
B.这几种酸都是氯元素的不同含氧酸,氯元素的化合价越高其酸性越强,所以这几种酸的酸性逐渐减弱,故B不选;
C.硫酸的酸性比亚硫酸强,亚硫酸的酸性比碳酸的强,所以这几种酸的酸性逐渐减弱,故C不选;
D.高溴酸的酸性比高碘酸强,且高溴酸和高碘酸都是强酸,次氯酸是弱酸,所以酸性由强到弱的顺序是HBrO4 HIO4
HClO,故D选;
故选D.
点评:
本题考查酸性强弱的比较,注意非金属的非金属性强弱决定其最高价含氧酸的酸性强弱,但不决定其低价含氧酸的酸性强弱,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A.B C.D.E.F六种物质的转化关系如图所示(反应条件和部分产物未标出)
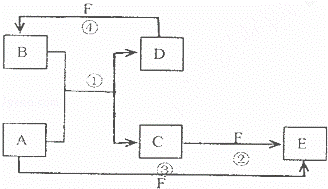
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A D反应都有红棕色气体生成,则A为 ,反应④的化学方程式为 .
(2)若A为常见的金属单质,D F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 .
(3)若A.D.F都是短周期非金属元素单质,且A.D所含元素同主族,A.F所含元素同周期,则反应①的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
|
| A. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3﹣+OH﹣=CaCO3↓+H2O |
|
| B. | 工业制漂白粉的反应:Cl2+Ca(OH)2=Ca2++Cl﹣+ClO﹣+H2O |
|
| C. | 用铜作电极电解饱和食盐水:2Cl﹣+2H2O=2OH﹣+Cl2↑+H2↑ |
|
| D. | 铜片跟稀硝酸反应:Cu+NO3﹣+4H+=Cu2++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
用价层电子对互斥理论预测H2O和CH4的立体结构两个结论都正确的是( )
|
| A. | 直线形,三角锥形 | B. | V形,三角锥形 |
|
| C. | 直线形,正四面体形 | D. | V形,正四面体形 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对Na、Mg、Al的有关性质的叙述正确的是( )
|
| A. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | B. | 第一电离能:Na<Mg<Al |
|
| C. | 电负性:Na>Mg>Al | D. | 还原性:Na>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,若有64gCu被氧化,则被还原的HNO3的质量是( )
|
| A. | 168g | B. | 42g | C. | 126g | D. | 60g |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应N2(g)+3H2(g)⇌2NH3(g)△H<0.下列研究目的和图示相符的是()
A B C D
研究
目的 温度(T)对反应的影响(T2>T1) 压强(p)对平衡常数的影响 温度(T)对反应的影响 压强(p)对反应的影响(p2>p1)
图示 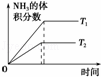
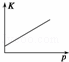
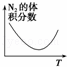
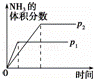
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既价廉又环保.

(1)工业上可用组成为K2O•M2O3•2RO2•nH2O的无机材料纯化制取的氢气
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为
②常温下,不能与M单质发生反应的是 (填序号)
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气来的方法有多种
①高温热分解法
已知:H2S(g)⇌H2(g)+1/2S2(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为cmol•L﹣1测定H2S的转化率,结果见右图.图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率.据图计算985℃时H2S按上述反应分解的平衡常数K= ;说明随温度的升高,曲线b向曲线a逼近的原因:
;说明随温度的升高,曲线b向曲线a逼近的原因:
②电化学法
该法制氢过程的示意图如右.反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中发生反应的化学方程式为 .反应后的溶液进入电解池,电解总反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A的分子式为C11H16,经测定数据表明,分子中除含苯环外不再含有其他环状结构,且苯环上只有一个侧链,符合此条件的烃的结构有( )
|
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com