

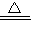 CaCl2+2NH3↑+2H2O,
CaCl2+2NH3↑+2H2O,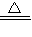 CaCl2+2NH3↑+2H2O;B;有白烟生成;碱石灰;湿润的红色石蕊;红色变为蓝色.
CaCl2+2NH3↑+2H2O;B;有白烟生成;碱石灰;湿润的红色石蕊;红色变为蓝色.

科目:高中化学 来源: 题型:
 氨是重要的化工原料,实验室制取氨气的化学方程式为
氨是重要的化工原料,实验室制取氨气的化学方程式为
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 7 | 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氨是重要的化工原料,实验室制取氨气的化学方程式为________,如图所示,A、B、C是气体收集装置,其中可用来收集氨气的是________.当两根分别蘸有浓氨水和浓盐酸的玻璃棒靠近时,会观察到的现象是________.在实验室,干燥氨时,通常是将制得的氨通过________,以除去其中的水蒸气;为检验氨气是否收集满,往往取________试纸置于试管口处,当颜色由________ 时,表明已经收集满氨气.
氨是重要的化工原料,实验室制取氨气的化学方程式为________,如图所示,A、B、C是气体收集装置,其中可用来收集氨气的是________.当两根分别蘸有浓氨水和浓盐酸的玻璃棒靠近时,会观察到的现象是________.在实验室,干燥氨时,通常是将制得的氨通过________,以除去其中的水蒸气;为检验氨气是否收集满,往往取________试纸置于试管口处,当颜色由________ 时,表明已经收集满氨气.查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com