
| A、《京都议定书》针对六种温室气体进行削减,包括二氧化碳(CO2)、甲烷(CH4)、氧化亚氮(N2O)、氢氟碳化物(HFCs)、全氟碳化物(PFCs)及六氟化硫(SF6).科学研究发现,同条件下等体积的甲烷产生的温室效应远远强于二氧化碳的.那么等质量的二氧化碳产生温室效应比甲烷的强 |
| B、合成高学科王效、稳定、廉价的太阳能光电转化材料,是开发利用太阳能的关键 |
| C、稀土元素都是长周期元素,稀土资源是国家战略性资源 |
| D、环境问题的最终解决要依靠科技进步,通常利用沉淀反应除去污水中的重金属离子 |


科目:高中化学 来源: 题型:
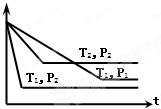 已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )| A、T1>T2,P1>P2,m+n>x,正反应放热 |
| B、T1<T2,P1<P2,m+n<x,正反应吸热 |
| C、T1>T2,P1<P2,m+n<x,正反应放热 |
| D、T1<T2,P1>P2,m+n>x,正反应吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向燃料煤中加入生石灰,可以减少对大气的污染 |
| B、用双氧水清洗伤口,可以杀菌消毒 |
| C、只用淀粉溶液就能检验出食盐中是否加碘 |
| D、随意丢弃废旧电池,会对环境造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
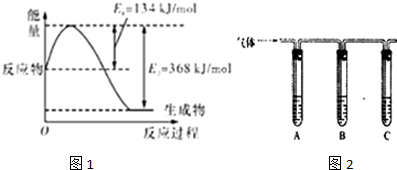
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 试管B中加1%品红溶液; 试管C中加 | 若 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO 当加入AgNO3溶液后,溶液颜色变浅 |
| B、合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施 |
| C、反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D、对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、XYZ |
| B、X3YZ |
| C、XYZ2 |
| D、X2YZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
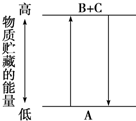
| A、A-→B+C和B+C-→A两个反应吸收或放出的能量不等 |
| B、A-→B+C是放热反应 |
| C、A具有的能量高于B和C具有的能量总和 |
| D、A-→B+C是吸热反应,则B+C-→A必然是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ca2+、CO32- |
| B、Na+、Ca2+、HCO3- |
| C、H+、SO42-、OH- |
| D、H+、Na+、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com