
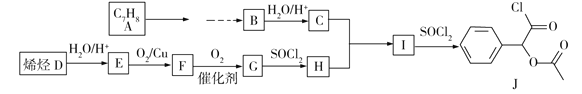
【题目】某化学小组以烯烃D和芳香烃A为原料合成医药中间体J的路线如下(部分产物和条件省略):
已知:RCN![]() RCOOH
RCOOH![]() RCOCl
RCOCl![]() RCOOR1
RCOOR1
回答下列问题:
(1)标准状况下,烯烃D的密度为1.25 g·L1。则D的结构简式为________。A的名称是____________。
(2)G所含官能团名称是____________;D→E的反应类型是____________。
(3)写出C+H→I的化学方程式:________________________。
(4)J的分子式为____________。
(5)B的同分异构体中,同时符合下列条件的结构有____________种。
①有4个碳原子在同一条直线上;
②含有—NH2和—OH且都与苯环直接相连。
【答案】CH2=CH2 甲苯 羧基 加成反应 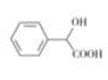 +CH3COCl→
+CH3COCl→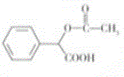 +HCl C10H9O3Cl 10
+HCl C10H9O3Cl 10
【解析】
芳香烃A为甲苯(![]() ),由J的结构简式,结合已知可推出I为
),由J的结构简式,结合已知可推出I为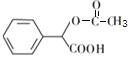 ;根据已知C+H→I,H为CH3COCl,标准状况下,烯烃D的密度为1.25 g·L-1,烯烃D的相对分子质量为28,则烯烃D为乙烯(CH2=CH2),乙烯和水加成生成E为乙醇(C2H5OH),乙醇催化氧化生成F为乙醛(CH3CHO),乙醛进一步氧化生成G为乙酸(CH3COOH),乙酸发生已知中的反应生成H为CH3COCl;C为
;根据已知C+H→I,H为CH3COCl,标准状况下,烯烃D的密度为1.25 g·L-1,烯烃D的相对分子质量为28,则烯烃D为乙烯(CH2=CH2),乙烯和水加成生成E为乙醇(C2H5OH),乙醇催化氧化生成F为乙醛(CH3CHO),乙醛进一步氧化生成G为乙酸(CH3COOH),乙酸发生已知中的反应生成H为CH3COCl;C为![]() ,结合已知反应,可推知B为
,结合已知反应,可推知B为![]() ,据此解答。
,据此解答。
(1)烯烃D的摩尔质量为1.25 g·L-1×22.4 L·mol-1=28 g·mol-1。则D的结构简式为CH2=CH2;A为![]() ,名称是甲苯,
,名称是甲苯,
故答案为:CH2=CH2;甲苯;
(2)G为CH3COOH,所含官能团名称是羧基;乙烯和水加成生成的E为C2H5OH,则D→E的反应类型是加成反应,
故答案为:羧基;加成反应;
(3)C为![]() ,H为CH3COCl,I为
,H为CH3COCl,I为 ,C+H→I为取代反应,化学方程式为:
,C+H→I为取代反应,化学方程式为:![]() +CH3COCl→
+CH3COCl→ +HCl,
+HCl,
故答案为:![]() +CH3COCl→
+CH3COCl→ +HCl;
+HCl;
(4)由J的结构简式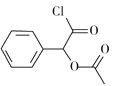 可知,其分子式为C10H9O3Cl,
可知,其分子式为C10H9O3Cl,
故答案为:C10H9O3Cl;
(5)B为![]() ,B的同分异构体中,符合①有4个碳原子在同一条直线上,则具有
,B的同分异构体中,符合①有4个碳原子在同一条直线上,则具有![]() 结构的碳骨架;②含有—NH2和—OH且都与苯环直接相连,说苯环上同时连有-C
结构的碳骨架;②含有—NH2和—OH且都与苯环直接相连,说苯环上同时连有-C![]() CH、—NH2和—OH三个取代基,根据定一移一分析,共有10种不同结构,
CH、—NH2和—OH三个取代基,根据定一移一分析,共有10种不同结构,
故答案为:10。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】次氯酸钾是―种白色粉末,极易溶于冷水,遇热水则分解,在空气中极不稳定,受热后迅速自行分解。工业上生产次氯酸押的流程如下:
![]()
下列说法正确的是
A. 步骤Ⅰ、Ⅱ发生的反应均为非氧化还原反应
B. 步骤Ⅱ采取的方法是加入足量水以制得Ca(OH)2溶液
C. 步骤Ⅲ氧化时,氯气是氧化剂,Ca(OH)2是还原剂
D. 步骤Ⅵ的操作包括蒸发浓缩,冷却结晶、在空气中晾干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也可用作熏蒸剂、防腐剂、消毒剂、还原剂等。
(1)SO2性质多变,若将SO2气体通入氢硫酸中,能看到的现象为:__________,该反应中SO2表现出______性;若将SO2气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中SO2表现出__________性。
(2)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2CaSO4·2H2O碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
余石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如下图所示。下列说法不正确的是( )

A.整个过程实现了光能向化学能的转换
B.过程Ⅱ有O-O单键生成并放出能量
C.过程Ⅲ发生的化学反应为:2H2O2 ═ 2H2O + O2↑
D.整个过程的总反应方程式为:2H2O ═ 2H2↑ + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
CH2=CH2+Br2 → BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃脱水生成乙醚
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
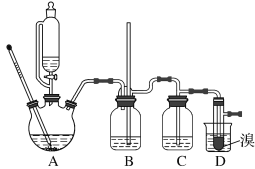
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132. | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是________(填正确选项前的字母)。
a .引发反应 b. 加快反应速度 c. 防止乙醇挥发 d. 减少副产物乙醚生成
(2)在装置C中应加入________(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a .水 b .浓硫酸 c .氢氧化钠溶液 d .饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是_______________________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”或“下”)。
(5)若产物中有少量未反应的Br2,最好用________(填正确选项前的字母)洗涤除去。
a 水 b 氢氧化钠溶液 c 碘化钠溶液 d 乙醇
(6)若产物中有少量副产物乙醚,可用________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是_______________________;但又不能过度冷却(如用冰水),其原因是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2-氯丁烷与乙醇溶液共热发生消去分子的反应
C. 甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D. 邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是药物合成中的一种重要中间体,下面是H的一种合成路线:
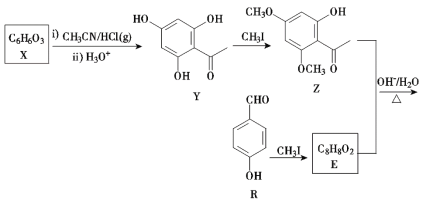
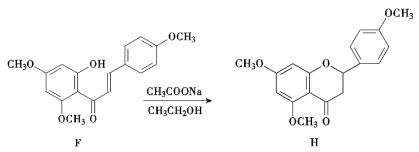
回答下列问题:
(1)X的结构简式为_______,其中所含官能团的名称为______;Y生成Z的反应类型为_______。
(2)R的化学名称是________。
(3)由Z和E合成F的化学方程式为__________________。
(4)同时满足苯环上有4个取代基,且既能发生银镜反应,又能发生水解反应的Y的同分异构体有________种,其中核磁共振氢谱上有4组峰,峰面积之比为1∶2∶2∶3的同分异构体的结构简式为________(一种即可)。
(5)参照上述合成路线,以乙醛和![]() 为原料(其他试剂任选),设计制备肉桂醛(
为原料(其他试剂任选),设计制备肉桂醛(![]() )的合成路线_______________。
)的合成路线_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素衍生物Q是合成抗肿瘤、抗凝血药的中间体,其合成路线如下。

已知:
I、
II、![]()
(1)A的分子式为C6H6O,能与饱和溴水反应生成白色沉淀。
① 按官能团分类,A的类别是_________。
② 生成白色沉淀的反应方程式是_________。
(2)A→B的反应方程式是_________。
(3)D→X的反应类型是_________。
(4)物质a的分子式为C5H10O3,核磁共振氢谱有两种吸收峰,由以下途径合成:

物质a的结构简式是_________。
(5)反应ⅰ为取代反应。Y只含一种官能团,Y的结构简式是_________。
(6)生成香豆素衍生物Q的“三步反应”,依次为“加成反应→消去反应→取代反应”,其中“取代反应”的化学方程式为_________。
(7)研究发现,一定条件下将香豆素衍生物Q水解、酯化生成 ![]() ,其水溶性增强,更有利于合成其他药物。请说明其水溶性增强的原因:______。
,其水溶性增强,更有利于合成其他药物。请说明其水溶性增强的原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1807年化学家戴维电解熔融氢氧化钠制得钠:4NaOH![]() O2↑+4Na+2H2O;后来盖吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOH
O2↑+4Na+2H2O;后来盖吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOH![]() Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
A. 戴维法制钠,阳极的电极反应式为:2OH-+2e-═H2↑+O2↑
B. 盖吕萨克法制钠原理是利用铁的金属性比钠的强
C. 若用戴维法与盖吕萨克法制得等量的钠,两方法转移电子总数相等
D. 若用戴维法与盖吕萨克法制得等量的钠,戴维法转移电子总数较少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com