
【题目】下列试剂中,一次就能鉴别出MgSO4、NH4Cl、KNO3三种溶液的是( )
A.AgNO3溶液
B.BaCl2溶液
C.NaOH溶液
D.CuCl2溶液
科目:高中化学 来源: 题型:
【题目】下列关于化学键的有关说法中正确的是( )。
A.化学键存在于原子之间,也存在于分子之间
B.两个原子之间的相互作用叫作化学键
C.离子键是阴、阳离子之间的相互吸引力
D.化学键通常指相邻原子之间强烈的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程不涉及化学反应的是
A. 含活性炭、细铁、食盐及蛭石等的暖手宝,在被使用时会发热
B. 用活性炭口罩防护空气中的粉尘等有害物质
C. 汽车排气管安装尾气催化转化装置
D. 通过煤的气化获得水煤气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀厂曾采用有氰电镀工艺,处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,在酸性条件下CNO-继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率。
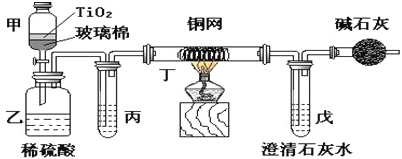
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200 mL(其中CN-的浓度为0.05 molL-1倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)甲中反应的离子方程式为________________________,乙中反应的离子方程式为________________________。
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等。丙中加入的除杂试剂是饱和食盐水,其作用是_____________________,丁在实验中的作用是______________,装有碱石灰的干燥管的作用是______________________________。
(3)戊中盛有含Ca(OH)20.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于__________。该测得值与工业实际处理的百分率相比总是偏低,简要说明可能原因之一_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习小组进行如下实验。
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化)。限选试剂和仪器:0.20mol/LH2C2O4 溶液、0.010mol/L KMnO4 溶液(酸性)、蒸馏水、 试管、量筒、秒表、恒温水浴槽
(1)上述实验①②是探究 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a 为 ;乙是实验需要测量的物理量,则表 格中“乙”应填写 。
【测定 H2C2O4·xH2O 中 x 值】 已知:M(H2C2O4)=90g/mol
称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液。
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000 mol·L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式
(3)某学生的滴定方式(夹持部分略去)如下,最合理的是 (选填 a、b)。


(4)由右图可知消耗 KMnO4 溶液体积为 mL;
(5)滴定过程中眼睛应注视_________________;
(6)通过上述数据,求得 x= 。以标准 KMnO4 溶液滴定样品溶液的浓度,未用 标准 KMnO4 溶液润洗滴定管,引起实验结果 (偏大、偏小或没有影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.化学反应除了生成新物质外,还伴随着能量的变化
B.放热反应一定不需要加热即可发生
C.需要加热才能发生的化学反应一定是吸热反应
D.化学反应中的能量变化都表现为热量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成:
2H2(g)+O2(g)=2H2O(l) △H1=-572kJ·mol-1
2HI(g)=H2(g)+I2(g) △H2=+10kJ·mol-1
2H2SO4(l)=2SO2(g)+2H2O(l)+O2(g) △H3=+462kJ·mol-1
则得
SO2(g)+I2(g)+2H2O(I)=2HI(g)+H2SO4(I) △H=_______kJ·mol-1
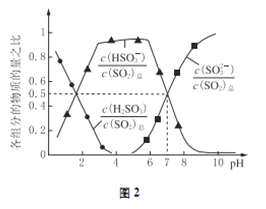
(2)氧化锌吸收法。配制ZnO悬浊液,在吸收塔中封闭循环脱硫。测得pH、吸收效率η随时间t的变化如图1所示;溶液中部分微粒与PH的关系如图2所示。
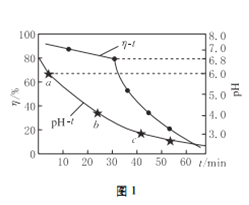
①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、________________。
②图1中的pH-t曲线ab段发生的主要化学方程式为___________________
③pH=7时,溶液中![]() =________
=________
(3)如图3所示,利用惰性电解电解含SO2的烟气回收S及H2SO4,以实现废物利用。
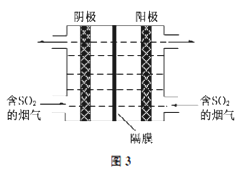
①阴极的电极反应式为_____________。
②每处理含19.2g SO2的烟气,理论上回收S、H2SO4的物质的量分别为______、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中一定属于放热反应的是 (填序号)。
①H2SO4与Ba(OH)2溶液反应 ②Mg与CH3COOH溶液反应 ③燃烧反应 ④复分解反应 ⑤C与CO2反应 ⑥Na2O2与水反应 ⑦胆矾受热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应能量变化的叙述中正确的是( )。
①如果反应物的总能量低于生成物的总能量,该反应一定是吸热反应 ②只要是在点燃条件下进行的反应就一定是吸热反应 ③只要是在常温常压下进行的反应就一定是放热反应 ④燃烧反应一定是放热反应 ⑤化合反应都是放热反应,分解反应都是吸热反应
A.①④ B.①②③ C.③⑤ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com