
25℃时对于pH=1的盐酸,下列叙述不正确的是
| A.c(H+)= c(Cl-)+ c(OH-) |
| B.c(H+)·c(OH-)=1.0×10—14 |
| C.由水电离出的c(H+)=1.0×10-13mol?L-1 |
| D.与pH=13的NaOH溶液混合后,混合溶液一定呈中性 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
有浓度为0.1 mol?L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol?L-1,b mol?L-1,c mol?L-1,其大小顺序为__________。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为
n1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为____________。
(4)与锌反应开始时产生氢(气)的速率分别为v1、v2、v3,其大小关系为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列对于溶液中的问题叙述正确的是( )
| A.向冰醋酸中加水至配成醋酸稀溶液的过程H+的浓度逐渐减小 |
| B.在稀溶液中:H+(aq) + OH-(aq) = H2O(l); △H=-57.3kJ/mol,则含1 mol HClO的稀溶液和含1 mol KOH的稀溶液完全反应放出的热量等于57.3 kJ |
| C.常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等 |
| D.常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温下,水的电离达到平衡:H2O H+ + OH-。下列叙述正确的是
H+ + OH-。下列叙述正确的是
| A.将水加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH-)= c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中
c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
| A.加少量烧碱溶液 | B.降低温度 | C.加少量冰醋酸 | D.加水 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ①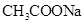 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④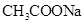 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于0.1mol·L-1 Na2SO3溶液,正确的是( )
| A.升高温度,溶液的pH降低 |
| B.c(Na+)=2c(SO32—)+ c(HSO3—)+ c(H2SO3) |
| C.c(Na+) + c(H+) = 2c(SO32—)+ 2c(HSO3—) + c(OH—) |
| D.加入少量NaOH固体,c(SO32—)与c(Na+)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
A.将0.2mol/L某强碱弱酸盐NaA溶液与0.1mol/L盐酸等体积混合,混合后溶液显碱性,则混合溶液中c(HA) >c(Cl-) >c(A-)>c(OH-)
B.相同条件下,向氨水、氢氧化钠溶液中分别加入适量的氯化铵晶体后,两溶液的pH:前者减小,后者增大
C.室温条件下,将pH=3盐酸VaL与pH=11氢氧化钠溶液VbL混合,混合后溶液pH=4,假设混合后忽略体积变化,则Va∶Vb=10∶9。
D.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com