
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成: ①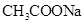 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与 ④
④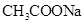 与
与 ,下列各项排序正确的是
,下列各项排序正确的是
| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D. : ①>④>③>② : ①>④>③>② |
B
解析试题分析:A.这几组混合物中都含有醋酸钠,盐酸溶液呈酸性,氢氧化钠溶液呈强碱性,氯化钠溶液呈中性,碳酸氢钠溶液呈弱碱性,所以这几种溶液pH大小顺序是②>④>③>①,故A错误;B.盐酸抑制醋酸根离子水解,氢氧化钠抑制醋酸根离子水解,氯化钠既不抑制也不促进醋酸根离子水解,碳酸氢根离子抑制醋酸根离子水解,但抑制能力小于氢氧根离子,所以溶液中醋酸根离子浓度大小顺序是②>④>③>①,故B正确;C.根据A知,这几种溶液中氢离子浓度大小顺序是②<④<③<①,故C错误;D.根据B知,醋酸根离子浓度越大,根据物料守恒知,醋酸分子的浓度就越小,所以醋酸分子浓度大小顺序是②<④<③<①,故D错误;故选:B.
考点:本题考查了粒子浓度大小的比较,明确物质特点是解本题关键,这几组物质中都含有醋酸钠,所以只比较另外一种物质的性质即可,难度中等。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:单选题
0.1 mol/L NaOH溶液140mL与0.1 mol/L H2SO4 60mL充分混合,若混合前后总体积变化忽略不计,则混合后溶液的pH为
| A.2 | B.3 | C.12 | D.14 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知Ksp[Al(OH)3]=1.3×10-33 mol4·L-4, Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4。现向pH=0浓度均为0.04mol·L-1的Al3+、Fe3+溶液中加入NaOH溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时对于pH=1的盐酸,下列叙述不正确的是
| A.c(H+)= c(Cl-)+ c(OH-) |
| B.c(H+)·c(OH-)=1.0×10—14 |
| C.由水电离出的c(H+)=1.0×10-13mol?L-1 |
| D.与pH=13的NaOH溶液混合后,混合溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:在100℃时,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为( )
| A.1 : 9 | B.10: 1 | C.9 : 1 | D.1: 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列水解的离子方程式正确的是
A.S2-+2H2O H2S+2OH- H2S+2OH- | B.Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| C.CO32-+H2OHCO3-+OH- | D.HS-+H2O H2S↑+OH- H2S↑+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于溶液的酸碱性说法正确的是( )
| A.c(H+)很小的溶液一定呈碱性 |
| B.PH=7的溶液一定呈中性 |
| C.c(OH-)= c(H+)的溶液一定呈中性 |
| D.不能使酚酞试液变红的溶液一定呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
| A.c(NH4+):③ > ② |
| B.pH:① > ② > ③ |
C.Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s) Mg2+ (aq) + 2OH- (aq)向溶解方向移动 Mg2+ (aq) + 2OH- (aq)向溶解方向移动 |
| D.等体积①和③混合溶液中 c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度下,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与pH=1的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为
| A.1∶9 | B.10∶1 | C.9∶1 | D.1∶10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com