
【题目】下图表示的是钢铁在海水中的锈蚀过程,以下有关说法正确的是( )

A. 该金属腐蚀过程为析氢腐蚀
B. 正极为C,发生的反应为氧化反应
C. 在酸性条件下发生的是吸氧腐蚀
D. 正极反应为O2+2H2O+4e-===4OH-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】“世界地球日”即每年的4月22日,是一项世界性的环境保护活动。下列行为中不利于环境保护的是( )
A. 严格履行《京都议定书》,控制温室气体的排放
B. 大量开采煤、石油及天然气以满足工业发展的需要
C. 加强新能源研究,使用压缩天然气、氢气作汽车燃料
D. 研发可降解塑料或代用品,控制白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO![]() 、Fe2+、NH
、Fe2+、NH![]() 、H+和H2O,下列叙述正确的是( )
、H+和H2O,下列叙述正确的是( )
A.该反应说明Fe(NO3)2溶液不宜加酸酸化
B.该反应中氧化剂与还原剂物质的量之比为8∶1
C.若有1 mol NO![]() 发生氧化反应,则转移电子5 mol
发生氧化反应,则转移电子5 mol
D.若将该反应设计成原电池,则负极反应为Fe3++e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键、金属键、离子键和分子间作用力是微观粒子间的不同相互作用,含有上述两种相互作用的晶体是( )
A. SiO2晶体 B. Ar晶体 C. NaCl晶体 D. NaOH晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列叙述正确的是( )

A. Y单质在空气中燃烧生成YO3
B. Z元素的最高价氧化物的水化物酸性最强
C. X的氢化物为H2X
D. Y、Z和W的阴离子半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:I.反应A中,4molHCl被氧化,放出115.6kJ热量。
II.
判断下列说法正确的是( )
A. 反应A的△H>-115.6kJ·mol-1
B. H2O中H—O键比HCl中H—Cl键弱
C. 由II中的数据判断氯元素的非金属性比氧元素强
D. 断开1molH—O键与断开1molH—Cl键所需能量相差31.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO·SiO2, 还含少量Fe2O3、A12O3、SiO2等杂质)通过如下方法制取。
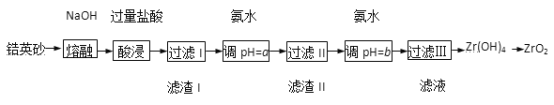
已知:ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
(1)在熔融时NaOH和ZrSiO4发生反应的化学方程式为________________,滤渣I的化学式为_______。
(2)用氨水调pH=a是为了使滤液I的杂质离子_______(填离子符号)完全沉淀,而ZrO2+不沉淀;继续加氨水至pH=b时,所发生反应的离子方程式为____________________________。
(3)过滤III所得滤液含有NH4Cl,向其中加入CaCO3粉末并加热,可得到两种气体。该反应的离子方程式为_______________。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。
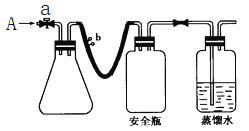
(1)实验原理
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为_____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,反应的离子方程式为_____________________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2 Na2S2O3=2Na1+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是___________________________;
②用注射器抽取某水样20. 00mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入23滴_______作指示剂;
⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点。滴定终点的现象是___________________________。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________ mg L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将_________ (填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.向鸡蛋清溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质变性
B.氨基酸种类较多,分子中都含有-COOH和-NH2
C.纤维素、淀粉和蔗糖等天然高分子化合物在一定条件下都能发生水解
D.油脂皂化反应实质就是酯在碱性环境下发生水解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com