
【题目】当硅原子由1s22s22p63s23p2![]() 1s22s22p63s13p3时,以下认识正确的是
1s22s22p63s13p3时,以下认识正确的是
A. 硅原子由基态转化成激发态,这一过程中吸收能量
B. 硅原子由基态转化成激发态,这一过程中释放能量
C. 转化后位于p能级上的两个电子处于同一轨道,且自旋方向相反
D. 转化后硅原子与磷原子电子层结构相同,化学性质相似
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是

A. 放电时,右槽发生还原反应
B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C. 充电时,每转移1mol电子,n(H+)的变化量为1mol
D. 充电时,阴极电解液pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤] 是抗非典型肺炎(SARS)的指定药物之一,其结构如右所示,有关阿昔洛韦的结构及性质的叙述中正确的是 ( )

①分子中最多有12个原子在同一平面内; ②属于芳香族化合物; ③是一种易溶于水的有机物; ④可以被氧化;⑤可以水解; ⑥可以燃烧; ⑦ 1 mol阿昔洛韦在催化剂作用下, 最多可与5molH2发生加成反应; ⑧分子式是C8H11N5O3
A. ①②③④⑥⑧ B. ②④⑤⑥ C. ③④⑤⑥⑧ D. ④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500![]() 有
有![]() 和
和![]() 的混合溶液分成5等份,取一份加入含
的混合溶液分成5等份,取一份加入含![]()
![]() 硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含![]()
![]() 硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种有机化合物的转换关系:

请回答下列问题;
(1)根据系统命名法,化合物A的名称是____________________。
(2)反应①的反应类型是__________________,反应③的反应类型是_________________________。
(3)化合物E是重要的工业原料,写出由D→E的化学方程式:__________________________。
(4)C2的结构简式是_________________________,F1的结构简式是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熏衣草醇( 结构如图) 可以用于高级化妆品及香水的香料。下列有关熏衣草醇的说法正确的是
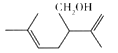
A. 熏衣草醇的分子式为C10H16O
B. 薰衣草醇能发生加成反应和酯化反应
C. 熏衣草醇分子中所有碳原子可能处于同一个平面
D. 熏衣草醇使溴水和酸性KMnO4 溶液褪色的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数。

(1)实验前,先将锌铜合金在稀硫酸中浸泡片刻,其目的是:___________________________________;
(2)实验操作步骤有:①将药品和水装入各仪器中
②连接好装置后,检查气密性
③记录C的液面位置
④将B中剩余固体过滤,洗涤,干燥,称重
⑤待B中不再有气体产生并恢复至室温后,
记录C的液面位置
⑥由A向B滴加足量的稀硫酸
上述实验的正确操作顺序是________________(填序号);记录C的液面位置时,除视线平视外,还应_____________________
(3)B中发生反应的化学方程式为_________________ ;
(4)若实验用锌铜合金的质量为a g,与稀硫酸充分反应后,
B中剩余固体的质量为bg,则锌的质量分数为____________;
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将______(填“偏大”“偏小”或“不受影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据),根据下图回答下列问题:

(1)PCl5分解生成PCl3和Cl2的热化学方程式__________________________;上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.8 mol PCl5,反应达到平衡时还剩余0.6 mol PCl5,其分解率α1等于____________;若反应温度由T1升高到T2,平衡时PCl5的分解率α2,α2____________α1(填“大于”、“小于”或“等于”)。
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是______________________________________。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com